Внимание! Статья адресована врачам-специалистам
MuzychenkoH.P.
Belarusian State Medical University, Minsk
Practical aspects of acne, acne scars
Резюме. Рубцевание является распространенным, однако трудно поддающимся терапии последствием акне. В лечении в основном применяют инвазивные, нефармакологические методы лечения рубцов постакне, которые могут быть показаны не всем пациентам. В этой статье обобщены современные знания о постакне и методах их коррекции.
Ключевые слова: акне, постакне, лечение, контрактубекс.
Медицинские новости. – 2023. – №6. – С. 36–40.
Summary. Scarring is a common but difficult to manage consequence of acne vulgaris. Mostly invasive, non-topical treatments for acne scars are used, which may not be indicated for all patients. In this review, we summarize current knowledge on acne scars and methods for their improvement.
Keywords: acne, acne scars, treatment, contractubex.
Meditsinskie novosti. – 2023. – N6. – P. 36–40.
Акне (аcne vulgaris, вульгарные угри, угревая болезнь) – хроническое полиморфное мультифакторное заболевание волосяных фолликулов и сальных желез (пилосебацейного комплекса), встречающееся у 80–85% подростков и лиц молодого возраста всех национальностей и типов кожи. В последние годы акне наблюдаются у все более молодых пациентов в результате раннего начала пубертатного периода [12]. Заболевание чаще регистрируется у девочек в возрасте 12 лет и младше и у мальчиков в возрасте 15 лет и старше [7, 10]. В большинстве случаев физиологическое течение подростковых акне легкой степени обычно не превышает 4–5 лет, однако более тяжелые клинические формы могут персистировать и до 30–40 лет. У 26% женщин и 12% мужчин клинические проявления угревой болезни могут сохраняться в возрасте 40–49 лет [1, 2].
У мужчин, как правило, акне возникают позже и протекают тяжелее. Для женщин характерно более продолжительное течение заболевания. Угревую болезнь в полной мере можно отнести к группе социально значимых заболеваний. Даже акне легкой степени тяжести могут сопровождаться выраженными психологическими проблемами, вызывать значительный эмоциональный стресс, что снижает качество жизни и имеет серьезные психосоциальные последствия. Широкая распространенность, тенденция к торпидному течению и развитию резистентных к традиционным методам лечения форм объясняют медицинскую и социальную значимость этой проблемы.
Этиопатогенез акне
Акне относится к мультифакторным дерматозам, в основе патогенеза которого – гиперпродукция и качественное изменение состава кожного сала, фолликулярный гиперкератоз, воспаление и патологическое размножение Propionibacterium acnes.
Усиление секреции кожного сала происходит за счет увеличения синтеза андрогенов гонадами или надпочечниками (абсолютная гиперандрогения) или повышения чувствительности рецепторов себоцитов и кератиноцитов к низким уровням андрогенов (относительная или периферическая гиперандрогения). Относительная гиперандрогения встречается гораздо чаще, чем абсолютная, и может быть обусловлена повышением активности 5?-редуктазы, обеспечивающей периферическую конверсию тестостерона в активный метаболит дигидротестостерон; снижением синтеза глобулина, связывающего половые гормоны, и повышением свободной фракции тестостерона в плазме крови; высокой плотностью дигидротестостероновых рецепторов в ядрах клеток. Повышение уровня инсулина в крови также оказывает влияние на продукцию глобулина, связывающего половые гормоны, обусловливая гиперандрогенные состояния [8, 9]. Гиперандрогения приводит к изменению не только количественного, но и качественного состава кожного сала. Снижение концентрации альфа-ленолевой кислоты себума, являющейся регулятором дифференцировки кератиноцитов, приводит к формированию фолликулярного кератоза и обтурации протока сально-волосяного фолликула. Нарушение эвакуации богатого липидами кожного сала создают благоприятные условия для развития факультативных анаэробов (Propionibacterium acnes и Propionibacterium granulosum), а также сапрофитной и условно-патогенной микрофлоры (Staphylococcus epidermidis, Staphylococcus aureus, Pityrosporum ovale), которые индуцируют каскад иммуноопосредованных воспалительных реакций, что в конечном итоге приводит к формированию клинической картины акне [3, 6, 15].
Экзо- и эндогенные факторы (особенности питания, стрессы, инсоляция, неправильный уход за кожей) также способны влиять на течение патологического процесса и провоцировать рецидивы.
Современной, общепризнанной и наиболее удобной классификацией акне в дерматологической практике является классификация, предложенная Американской академией дерматологии [1]. Согласно ей, различают следующие степени тяжести акне:
– Iстепень – характеризуется наличием комедонов (закрытых и открытых) и до 10 папул,
– IIстепень – комедоны, папулы (много), пустулы – до 10,
– IIIстепень – комедоны, папулы, пустулы, до 30 узлов,
– IVстепень – выраженная воспалительная реакция в глубоких слоях дермы с формированием множественных болезненных узлов и кист.
В зависимости от клинической картины различают:
?комедональные акне,
?папуло-пустулезные акне легкой и средней степени тяжести,
?папуло-пустулезные акне тяжелой степени / нодулярные акне средней степени тяжести,
?нодулярные акне тяжелой степени / конглобатные акне.
Как правило, акне характеризуется рецидивирующим течением и нарастанием тяжести клинических проявлений, что может привести к формированию рубцов постакне. Именно поэтому ведение пациентов требует своевременного и эффективного подхода уже на ранних стадиях дерматоза.
Симптомокомплекс постакне
Сформировавшиеся последствия угревой болезни (постакне) беспокоят пациентов не меньше, чем активные проявления дерматоза, сложно поддаются лечению и нередко являются необратимыми, значительно снижая качество их жизни. Постакне включает в себя симптомокомплекс вторичных изменений, развившихся в результате эволюции различных форм воспалительных акне и сопровождающихся нарушением пигментации и формированием рубцовых изменений кожи [4]. Постакне от легкой до умеренной степени тяжести встречаются у 95% пациентов с акне вне зависимости от клинической формы и степени тяжести дерматоза, при этом у 30% наблюдаются патологические изменения тяжелой степени. Формирование постакне часто является результатом несвоевременного или неадекватного лечения, аутотравматизации, а также манипуляций в процессе ведения длительно существующих воспалительных акне. Однако, могут сформироваться и несмотря на адекватную медикаментозную терапию.
К наиболее часто встречающимся проявлениям постакне относят гиперпигментацию, расширенные поры, неравномерную текстуру кожи, рубцы (рис. 2) [18].
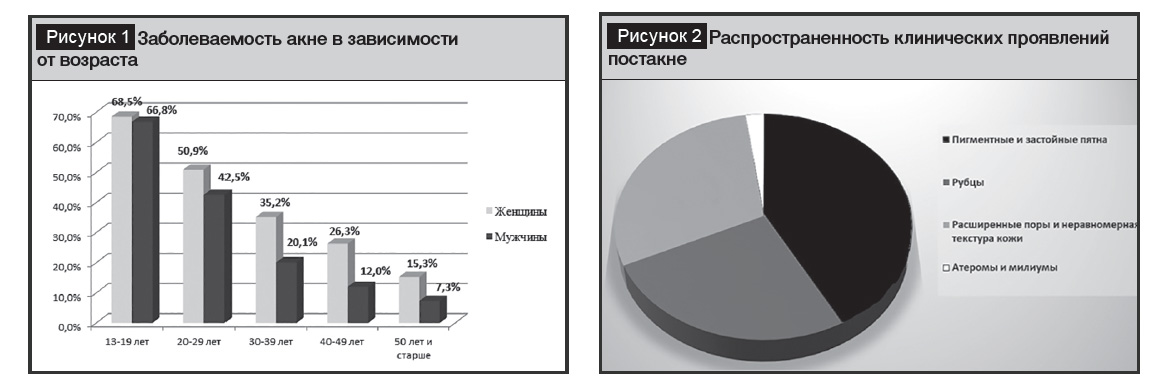
От80 до 90% рубцов постакне формируются в результате ассоциированной потери коллагена (атрофические рубцы), в то время как возникновение келоидных или гипертрофических рубцов (10–20%) связано с избыточным отложением коллагена и снижением активности коллагеназы. Поствоспалительная гиперпигментация формируется в результате местного воздействия медиаторов воспаления (провоспалительных цитокинов, метаболитов арахидоновой кислоты) и активации меланоцитов с последующей передачей меланина кератиноцитам. В основе патогенеза рубцов постакне лежат воспалительные процессы в области сально-волосяных фолликулов. Формирование рубцов обычно проходит через три фазы заживления раны: воспаление, формирование грануляционной ткани и ремоделирование матрикса. В патогенезе формирования постакне решающее значение имеет глубина повреждения: эритема и пигментация являются результатом эпидермальной травматизации, рубцы – дермальной.
Всемирным альянсом по лечению акне (Global Alliance acne treatment) к причинам формирования постакне относят:
– тяжелые формы акне (нодуло-кистозные, шаровидные),
– генетическая детерминированность характера реакции на травму и повреждение (сочетание полиморфизма генов металлопротеиназ, коллагена, факторов роста сосудистого эндотелия и других),
– длительное течение акне,
– аутотравматизация (экскориированные акне),
– несвоевременно начатая или неадекватная терапия,
– отягощенный анамнез по акне новорожденных,
– мужской пол,
– IV–VI фототип кожи [17].
Типы и степень тяжести рубцов
постакне
Атрофические рубцы классифицируются на сколотые («ice-pick», клиновидные, V-образные), прямоугольные («boxcar», U-образные) и закругленные («rolling», M-образные) [16]. Прямоугольные и закругленные рубцы в зависимости от глубины вовлечения дермы подразделяются на поверхностные и глубокие.
Выраженность рубцов постакне имеет решающее значение для выбора метода коррекции (табл. 1) [14].
Таблица 1. Шкала оценки степени тяжести рубцов постакне Гудмана и Барона
|
Оценка
|
Уровень поражения
|
Клинические проявления
|
|
1 балл
|
Макулярный (пятнистый)
|
Эритематозные гипер- или депигментированные плоские рубцы, не меняющие рельеф кожи,
но влияющие на ее цвет
|
|
2 балла
|
Слабый
|
Слабовыраженные и атрофические или гипертрофические рубцы, не различимые на расстоянии 50 см и более, легко маскируемые косметикой или тенью отрастающих щетинистых волос на бороде
у мужчин. При экстрафациальной локализации – маскируются отрастающими волосами
|
|
3 балла
|
Умеренный
|
Умеренные атрофические или гипертрофические рубцы, хорошо заметные на расстоянии 50 см
и более, плохо маскируемые косметикой, тенью отрастающих после бритья волос или естественно растущими волосами при экстрафациальной локализации. При натяжении кожи атрофические рубцы легко сглаживаются
|
|
4 балла
|
Тяжелый
|
Выраженные атрофические или гипертрофические рубцы, хорошо заметные на расстоянии 50 см и более, плохо маскируемые косметикой, тенью отрастающих после бритья волос или естественно растущими волосами при экстрафациальной локализации. При натяжении кожи атрофические рубцы не сглаживаются
|
Методы коррекции постакне
Проблема эффективного лечения постакне является одной из актуальных в современной дерматологии и косметологии. В связи с длительным лечением и частичной эффективностью многих методов, приводящим к разочарованию и фрустрации, приверженность терапии пациентов остается по-прежнему низкой.
В последнее время лечение рубцов постакне стало более результативным благодаря внедрению новых методов, обладающих лучшей эффективностью и безопасностью. При планировании тактики лечения следует учитывать наличие поствоспалительной гиперпигментации, локализацию, тип и глубину расположения рубцов, а также фототип кожи пациента.
В лечении поствоспалительной гиперпигментации используются топические препараты (гидрохинон, меквинол, третиноин и другие ретиноиды, кортикостероиды, гликолевая и азелаиновая кислоты), часто в комбинации с химическими пилингами и фотопротекторами. Возможно применение импульсного света, фракционной микроигольчатой терапии.
Обсуждение запросов пациента имеет важное значение в определении реалистичных ожиданий. Необходимо учитывать способность пациента оценивать потенциальный риск выбранного метода, возможность длительного лечения и его стоимость, социальное положение и требования к работе.
Выбор и объем методов терапии рубцов постакне зависит от их морфологии и степени тяжести. Для уменьшения выраженности рубцов существует целый арсенал методов лечения. Во-первых, важно по возможности уменьшить продолжительность и интенсивность воспаления, что подчеркивает необходимость своевременного лечения угревой болезни. Использование топических ретиноидов эффективно для профилактики формирования рубцов.
В настоящее время в лечении атрофических рубцов широко используют нефармакологические, инвазивные процедуры, которые могут быть доступны не для всех пациентов. В таблице 2 приведены различные топические средства, применяемые в лечении рубцов постакне, с уровнем доказательности по данным Оксфордского центра доказательной медицины [23].
Таблица 2. Топические средства для лечения рубцов постакне
|
Топическое средство
|
Уровень доказательности *
|
|
Адапален 0,3%
Тазаротен 0,1%
Гликолевая кислота 15%
Производные витамина С
Третиноин 0,05%
Такролимус 0,1%
Силиконовый гель + Er YAG лазер
Траниласт + Изотретиноин
Плазменный гель + фракционный CO2 лазер
Лиофилизированный GF + фракционный CO2 лазер
Топическая PRP + микронидлинг
AF -MSC + микронидлинг
Местный инсулин + микронидлинг
Полимолочная кислота + MNRF
Ретиноевая кислота + гликолевая кислота
Ионофорез: Эстриол и Третиноин
|
1b/2b
1b
1b
2b
4
4
1b
1b
1b
2b
2a
2b
2b
2b
4
4
|
Эффективность 0,05% третиноина доказана в лечении келоидных рубцов. Исследований его применения при менее выраженных рубцах постакне немного, однако результативность может быть обусловлена увеличением продукции коллагена и повышением эластичности сосочкового слоя дермы, приводящей к улучшению структуры и упругости кожи.
Пилинги с гликолевой кислотой являются эффективным методом лечения атрофических рубцов постакне, однако для достижения выраженного улучшения необходимо несколько повторных курсов. Наиболее эффективно применение пилинга с 70% гликолевой кислотой. Вместе с тем длительное ежедневное использование крема с низкой концентрацией (15%) гликолевой кислоты в связи с хорошей переносимостью и невысоким риском побочных эффектов может быть рекомендовано пациентам с непереносимостью пилингов [13].
В рандомизированном исследовании доказана эффективность комбинации геля Адапален 0,3% + Бензоилпероксид 2,5% в течение 24 недель в отношении атрофических рубцов и воспалительных акне, что обусловливает важность раннего начала эффективного лечения для предотвращения и уменьшения образования постакне [11].
Применение топических ретиноидов одобрено FDA для лечения акне и фотоповрежденной кожи. Топические ретиноиды активируют дермальные фибробласты, тем самым увеличивая продукцию проколлагена в фотостареющей коже. Кроме того, топические ретиноиды снижают синтез коллагеназы, что может привести к депонированию коллагена в рубцовой ткани. Поскольку фотопо-врежденная кожа и атрофические рубцы постакне имеют общие черты, сопровождаясь разрушением межклеточного матрикса, 0,3% адапален и 0,1% крем тазаротен потенциально могут оказывать положительный эффект в терапии атрофических рубцов [21].
Витамин С способствует регенерации тканей благодаря плейотропной модуляции метаболизма коллагена и может оказывать положительное влияние на атрофические рубцы при акне. Витамин С играет важную роль в процессах самообновления, стимуляции клеточного цикла и генов подвижности фибробластов, а также ингибирует медиаторы воспаления посредством интерлейкина-1? и фактора некроза опухоли ?. Угнетая синтез меланина, тирозиназу и активные формы кислорода, способствует коррекции гиперпигментации.
Поствоспалительные пятна, формирующиеся в результате воспалительного каскада, вызванного акне, и неоваскуляризации, считаются признаком продолжающегося воспаления, которое может завершиться атрофическим рубцеванием. Топический такролимус применяется при воспалительных состояниях в связи с его эффективностью в отношении ингибирования Т-клеток. Он также снижает экспрессию фактора роста эндотелия сосудов (VEGF), оказывая влияние на оба компонента патогенеза поствоспалительных пятен. Таким образом, местное применение 0,1% мази такролимус в течение 5–7 недель является эффективным в профилактике формирования атрофических рубцов [22].
Силиконовый гель применяется для лечения и профилактики в ранние сроки рубцевания гипертрофических и келоидных рубцов, а также в комплексных протоколах коррекции атрофических рубцов. Механизм действия силиконового геля связан с угнетением поступления кислорода к фибробластам и ингибированием в них синтеза коллагена, а также снижением уровня воспалительных цитокинов, повышением активности коллагеназы, препятствующей формированию патологического рубца [17].
Траниласт, N-(3,4-диметоксицин-намоил) антраниловая кислота, используется в качестве противоаллергического препарата и в лечении фиброзных состояний, келоидов и гипертрофических рубцов. Механизм действия обусловлен ингибированием высвобождения медиаторов из тучных клеток, а также синтеза коллагена в фибробластах путем угнетения высвобождения трансформирующего фактора роста (TGF)-?1 из фибробластов рубца. В исследовании A. Weinstein комбинированное применение геля траниласта 8% два раза в день с лечением системным изотретиноином в активной фазе акне приводит к уменьшению количества рубцов и улучшению текстуры кожи [26].
Показана высокая результативность комбинированного лечения атрофических рубцов постакне микронидлинга с внутрикожным введением плазмы обогащенной тромбоцитами (PRP-терапия) [20]. После микронидлинга коллагеновые волокна принимают упорядоченную структуру, а факторы роста PRP усиливают регенерацию.
Полимолочная кислота является эффективным методом лечения объемного дефицита, действует как биостимулятор, стимулируя неоколлагенез и васкуляризацию существующего коллагена. Микроигольчатый RF -лифтинг (фракционное воздействие микроиглами и радиочастотное воздействие) в комбинации с полимолочной кислотой повышает результативность способа лечения [6].
Синергетический эффект ретинальдегида и гликолевой кислоты хорошо изучен и показал высокую эффективность в ретроспективном исследовании B.S. Chandrashekar и соавт. [9]. Применение ретиноевой кислоты сглаживает рубцы постакне и уменьшает поствоспалительную гиперпигментацию, а гликолевая кислота благодаря кератолитической активности снижает выраженность атрофических рубцов.
Раннее применение неинвазивных консервативных методов имеет принципиальное значение в ведении пациентов с постакне, в связи с чем назначение специально разработанных средств будет способствовать профилактике рубцевания и минимизации сформировавшихся после разрешения акнеформных элементов рубцов.
Гель для наружного применения Контрактубекс, содержащий аллантоин (обладает разрыхляющим свойством в эпидермисе, покрывающим рубец), экстракт лука Cerae (вызывает супрессию пролиферации фибробластов и оказывает противовоспалительное и фибринолитическое действие), гепарин (обладает антиоксидантным, противовоспалительным и фибринолитическим свойствами), стимулирует клеточную регенерацию без гиперплазии, ингибирует пролиферацию келоидных фибробластов. Контрактубекс широко используется в противорубцовой терапии с целью уменьшения воспаления и экспрессии трансформирующего фактора роста, стимулирует клеточный апоптоз (табл. 3). В течение многих лет Контрактубекс применяется в хирургии и демонстрирует эффективность в лечении послеоперационных и послеожоговых рубцов [8].
Таблица 3. Активные составляющие геля Контрактубекс
|
Активный компонент
|
Механизм действия
|
|
Аллантоин
|
Выполняет кератолитическое воздействие, то есть растворяет верхний ороговевший слой кожи рубца или шрама. Это вещество ускоряет заживление раны, способствует образованию новой кожи, усиливает способность тканей удерживать воду, повышает их проницаемость для других активных веществ геля, улучшает кровообращение
|
|
Гепарин натрия
|
Оказывает противоаллергическое, противовоспалительное и антипролиферативное (останавливается рост клеток соединительной ткани и улучшается их насыщение водой, что проявляется смягчением жесткой рубцовой ткани) воздействие
|
|
Экстракт лука Cerae (Цепалин)
|
Обеспечивает противовоспалительное и фибринолитическое (растворение кровяных сгустков) воздействие. Луковые вещества уменьшают размножение клеток-фибробластов (клетки соединительной ткани), которые и образуют жесткий и растущий рубец на месте раны
|
Применение препарата возможно только после эпителизации эрозий 2–3 раза в сутки продолжительностью от 4 недель до 3–6 месяцев и более, в зависимости от степени повреждения и возраста рубцовой ткани. Эффективным является применение Контрактубекса в составе комплексной терапии в сочетании с физиотерапевтическими методами (фонофорез, электрофорез).
Выводы:
1. Нет универсальных рекомендаций по оптимизации лечения рубцов постакне. При выборе способа коррекции необходим персонифицированный подход с учетом разновидности постакне-изменений и индивидуальных особенностей и предпочтений пациента. Раннее начало терапии постакне после снижения активности воспалительного процесса является залогом хорошего прогноза профилактики рубцевания.
2. Препарат Контрактубекс является эффективной альтернативой инвазивным и другим консервативным методам коррекции и может быть рекомендован пациентам с угревой болезнью с целью профилактики постакне.
Л И Т Е Р А Т У Р А
1. Адаскевич, В.П. Диагностические индексы в дерматологии / В.П. Адаскевич. – М., 2014. – 344 с.
2. Кунгуров, Н.В. Угревая сыпь как медико-социальная проблема юношества / Н.В. Кунгуров [и др.] // Уральский мед. журнал. – 2003. – №3. – С.4–8.
3. Кутасевич Я.Ф. Микробиоценоз кожи у больных угревой болезнью и пути его коррекции / Я.Ф. Кутасевич [и др.] // Укр. журн. дерматол. дерматол., венерол., косметол. – 2003. – №1. – С.43–47.
4. Монахов С.А. Акне: клиника и терапия. Методическое пособие для врачей. – М., 2013.
5. Adebamowo, C.A. Milk consumption and acne in teenaged boys / C.A. Adebamowo [et al.] // J Am Acad Dermatol. – 2008. – Vol.58, N5. – P.787–793.
6. An M.K., Hong E.H., Suh S.B., Park E.J., Kim K.H. // Dermatol Surg. – 2020. – Vol.46, N6. – P.796–802.
7. Arora, M.K. Role of hormones in acne vulgaris / M.K. Arora, A. Yadav, V. Saini // Clin Biochem. – 2011. – Vol.44, N13. – P.1035–1040.
8. Beuth J., Hunzelmann N., Van Leendert R., et al. // In Vivo. – 2006. – Vol.20, N2. – P.277–283.
9. Chandrashekar B.S., Ashwini K.R., Vasanth V., Navale S. // Indian Dermatol Online J. – 2015. – Vol.6, N2. – P.84–88.
10. Del Prete M. Insulin resistance and acne: a new risk factor for men? / Del Prete M. [et аl.] // Endocrine. – 2012. – Vol.42. – P.555–560.
11. Dréno B., Bissonnette R., Gagné-Henley A., et al. // Am J Clin Dermatol. – 2019. – Vol.20, N5. – P.725–732.
12. Dreno, B. Epidemiology of acne / B. Dreno, F. Poli // 20-th World Congress Dermatology. – 2002. – Ann. Dermatol. Venerol (issue 132).
13. Erbagci Z., Akçali C. // Int J Dermatol. – 2000. – Vol.39, N10. – P.789–794.
14. Goodman G.J., Baron J.A. // J Cosmet Dermatol. – 2006. – Vol.5. – P.48–52.
15. Halvorsen J.A., Stern R.S., Dalgard F., et al. // J Invest Dermatol 2011. – Vol.131. – P.363–370.
16. Jacob C.I., Dover J.S., Kaminer M.S. // J Am Acad Dermatol. – 2001. – Vol.45. – P.109–117.
17. Khamthara J., Kumtornrut C., Pongpairoj K., Asawanonda P. // J Cosmet Laser Ther. – 2018. – Vol.20, N2. – P.96–101.
18. Layton A.M. // Am J Clin Dermotol.2001. – Vol.2. – P.135–141.
19. Самцов А.В. // Акне и акнеформные дерматозы. Монография. – М., 2009. – С.72–73.
20. Liden, S. Clinical evaluation in acne / Liden S., Goransson K., Odsell L. // Acta Derm. Venereol. – 1980. – Vol.89. – P.47–52.
21. Long T., Gupta A., Ma S., Hsu S. // J Cosmet Dermatol. – 2020. – Vol.19, N4. – P.836–844.
22. Loss M.J., Leung S., Chien A., Kerrouche N., Fischer A.H., Kang S. // Dermatol Ther (Heidelb). – 2018. – Vol.8, N2. – P.245–257.
23. Mhatre M., Sharma A., Agrawal S. // J Am Acad Dermatol. – 2022. – Vol.86, N6. – e253–e254.
24. OCEBM Levels of Evidence Working Group. “The Oxford 2011 Levels of Evidence”. Oxford Centre for Evidence-Based Medicine. http://www.cebm.net/ocebm-levels-of-evidence
25. Plewig, G. Acne and Rosacea / G. Plewig, A.M. Kligman. – Berlin, 2000. – 744 p.
26. Tan, J. Prospective Study of Pathogenesis of Atrophic Acne Scars and Role of Macular Erythema / J. Tan [et аl.] // J Drugs Dermatol. – 2017. – Vol.16, N6. – P.566–572.
27. Weinstein A., Koren A., Sprecher E., Zur E., Mehrabi J.N., Artzi O. // Clin Exp Dermatol. – 2020. – Vol.45, N1. – P.41–47.
28. Zaenglein, A.L. Guidelines of care for the management of acne vulgaris / A.L. Zaenglein [et аl.] // J Am Acad Dermatol. – 2016. – Vol.74, N5. – P.945–973.
Медицинские новости. – 2023. – №6. – С. 36-40.
Внимание! Статья адресована врачам-специалистам. Перепечатка данной статьи или её фрагментов в Интернете без гиперссылки на первоисточник рассматривается как нарушение авторских прав.