Внимание! Статья адресована врачам-специалистам
Tonka A.V., Kolomiets N.D., Hanenko O.N.
Belarusian Medical Academy of Postgraduate Education, Minsk
A new method for laboratory assessment
of antibiotic resistance foodborne bacterial pathogens
Резюме. Статья посвящена разработке методологии проведения антибиотикорезистентности бактерий, выделенных из объектов окружающей среды и пищевых продуктов. Лабораторный этап является платформой для формирования единой страновой системы обработки и анализа данных с целью эпидемиологического слежения и своевременного реагирования на новые характеристики патогенов. Разработанный метод испытан в экспериментальных условиях с проведением валидации. Предложено оценку чувствительности/устойчивости изолята к антибактериальным препаратам проводить с определением пороговой, нижней пороговой, верхней пороговой, минимальной ингибирующей и субингибирующей концентраций.
Ключевые слова: ингибирующая концентрация, пищевые бактериальные патогены, антибиотикорезистентность, оценка риска.
Медицинскиеновости. – 2023. – №5. – С. 67–71.
Summary. The article is devoted to the development of a methodology for testing the antibiotic resistance of bacteria isolated from environmental objects and food products. The laboratory stage is a platform for the formation of a unified country data processing and analysis system for the purpose of epidemiological monitoring and timely response to new characteristics of pathogens. The developed method was tested under experimental conditions with validation. It is proposed to evaluate the sensitivity/resistance of an isolate to antibacterial drugs with the determination of a threshold concentration, a lower threshold concentration, an upper threshold concentration, a minimum inhibitory concentration and asubinhibitory concentration.
Keywords: inhibitory concentration, foodborne bacterial pathogens, antibiotic resistance, risk assessment.
Meditsinskie novosti. – 2023. – N5. – P. 67–71.
Микроорганизмы пищевого происхождения, устойчивые к противомикробным препаратам (УПП), являются глобальной проблемой безопасности не только в сфере пищевых продуктов, но и в целом для общественного здравоохранения [1, 2]. Применение противомикробных препаратов в животноводстве может увеличивать риск возникновения устойчивых возбудителей бактериальных инфекций пищевого происхождения у людей прежде всего через контаминированные продукты животного происхождения. При тяжелых инфекциях у человека, вызванных УПП бактериями, лечение антибиотиками может быть менее эффективным или даже безуспешным [3, 4].
Эквивалентность оценки риска устойчивости к противомикробным препаратам между странами с различной политикой в области УПП должна быть установлена с использованием научно обоснованных оценок риска. Руководство Комиссии Кодекса Алиментариус по анализу риска устойчивости к противомикробным препаратам микроорганизмов пищевого происхождения рекомендует подход, требующий количественной оценки [5]. Однако в настоящее время руководящие принципы Кодекса по анализу риска УПП сложны, трудоемки и не являются жизнеспособным вариантом для оценки воздействия антибиотикорезистентных пищевых бактериальных патогенов на здоровье человека. Для учета страновых различий и расчета сопоставимых региональных оценок риска необходимы более гибкие и простые методы исследований и оценки, которые смогут применяться на практике и быстро прогнозировать риски для здоровья человека при выявлении изменений в антибиотикорезистентности бактерий, выделенных из окружающей среды.
Цель исследования – разработать эффективный метод проведения лабораторного этапа эпидемиологического слежения за антибиотикорезистентностью пищевых бактериальных патогенов.
Материалы и методы
Работа выполнялась на кафедре эпидемиологии и микробиологии Белорусской медицинской академии последипломного образования в рамках задания «Разработать и внедрить метод оценки риска формирования антибиотикорезистентности пищевых бактериальных патогенов» задания 06.02. «Разработать и внедрить методы оценки и управления риском здоровью, ассоциированным с остаточным количеством антибактериальных препаратов в пищевой продукции» (подпрограммы «Безопасность среды обитания человека» ГНТП «Научно-техническое обеспечение качества и доступности медицинских услуг», 2021–2025 годы).
Для изучения состава контаминирующей микробиоты проведены санитарно-микробиологические исследования 55 образцов продовольственного сырья и пищевых продуктов животного происхождения (мясо, рыба, птица) и других групп продовольственного сырья и пищевых продуктов.
Идентификация изолятов выделенных микроорганизмов выполнена с применением пестрых биохимических рядов, тест-систем для идентификации, в том числе коммерческих тест-систем API 20E для энтеробактерий, APIListeriaи с использованием автоматического микробиологического анализатора «VITEK 2 Compact» (bioMérieux, Франция).
Определена чувствительность эпидемически значимых микроорганизмов к антибактериальным препаратам (АБП). Исследования осуществляли с помощью диско-диффузионного метода на агаре Мюллера – Хинтона, методом последовательных разведений в бульоне Мюллера – Хинтона и методом пограничных концентраций на автоматическом биохимическом анализаторе «VITEK 2 Compact».
Полученные данные валидированы, обработаны с использованием методов статистики, адекватных поставленным задачам и объемам выборочных совокупностей.
Результаты и обсуждение
Из 55 проб пищевых продуктов животного происхождения выделено, идентифицировано и охарактеризовано 68 бактериальных изолятов. К представителям порядка Enterobacteriales относились33,8% (CI95% 28,1–39,5)выделенных бактерий, в том числе условно-патогенные бактерии родовEscherichia, Hafnia, Klebsiella, Serratia, Citrobacter. Основными выделенными патогенными микроорганизмами являлись Listeria monocytogenes, Salmonella spp.,Proteus spp. и Staphylococcus aureus. Удельный вес патогенных бактерий из выделенных и охарактеризованных культур составил 41,2% (CI95% 35,2–47,2) [6].
Проведены исследования МИК ранее нами выделенных из пищевых продуктов и окружающей среды и идентифицированных изолятов, в том числе и с использованием коммерческих вариантов метода микроразведений в бульоне с модификацией нами данного метода.
Предлагаемый методпроведения исследования предназначен для обеспечения лабораторного этапа эпидемио-логического слежения за распространением приобретенной резистентности к антибиотикам у пищевых бактерий и включает:
1. видовую идентификацию, характеристику и оценку эпидемиологической значимости выделенных микроорганизмов с целью отбора изолятов, подлежащих эпидемиологическому слежению за распространением резистентности бактерий к антибиотикам;
2. выбор лабораторного метода исследования и спектра тестируемых антибиотиков;
3. определение чувствительности микроорганизмов к антибиотикам и оформление документации по результатам полученной информации о характеристике чувствительности/устойчивости изолята к антибиотикам.
Отбор изолятов, подлежащих эпидемиологическому слежению за распространением резистентности к антибиотикам и изолированных из пищевых продуктов животного происхождения и среды технологического окружения, проводится на основании определения категории эпидемиологической значимости и уровня приоритета для мониторирования в соответствии с алгоритмом на рисунке 1.

Критерий значимости (Кз) – характеристика изолята, выделенного в лаборатории, устанавливающая категорию эпидемиологической значимости.
Критерий значимости 1 (Кз1) присваивается микроорганизму, выделенному из продовольственного сырья и(или) пищевых продуктов животного происхождения. Критерий значимости 2 (Кз2) присваивается микроорганизму, выделенному из среды технологического окружения пищевых производств. Критерий значимости 3 (Кз3) присваивается микроорганизму, выделенному из окружающей среды (вода, почва, воздух, морские отложения).
Если изолят соответствует Кз1 или Кз1+Кз2, Кз1+Кз3, его следует отнести к категории «наиболее значимых микроорганизмов». Если исследуемый микроорганизм соответствует Кз2 или Кз2+Кз3, его следует отнести к категории «значимых микроорганизмов». При соответствии только Кз3 – микроорганизм следует отнести к категории «менее значимых микроорганизмов». Микроорганизм, отнесенный к категории «наиболее значимых» или «значимых», ранжируется на следующем этапе по факторам приоритетности.
Фактор приоритетности (Фп) – видовая характеристика, устанавливающая приоритетность проведения выявления вторичной антибиотикорезистентности у изолята, выделенного в лаборатории.
Фактор приоритетности 1 (Фп1) присваивается микроорганизму, который по данным научной литературы с большой вероятностью имеет сформированную устойчивость к группам антибиотиков, потенциально применимых для лечения инфекционных болезней, вызванных этим возбудителем. Фактор приоритетности 2 (Фп2) присваивается микроорганизму, который вызывает серьезные инфекционные заболевания у людей, при этом имеется ограниченный перечень лекарственных препаратов для их лечения. Фактор приоритетности 3 (Фп3) присваивается микроорганизму, который еще не имеет устойчивости к группам антибиотиков, потенциально применимых для лечения инфекционных болезней, вызванных этим возбудителем, но есть доказательства передачи данных бактерий либо их генов устойчивости человеку из нечеловеческих источников.
Если изолят относится к виду бактерий, который имеет в характеристике фактор Фп1 или совокупность факторов Фп1+Фп2 либо Фп2+Фп3, для него устанавливается высокий уровень приоритета оценки антибиотикорезистентности. При наличии у изолята фактора Фп2 или Фп3 – умеренный уровень. Для изолятов с отсутствием всех факторов приоритетности устанавливается низкий уровень для проведения исследований по выявлению формирования антибиотикорезистентности.
Для проведения лабораторных исследований на постоянной основе отбираются штаммы микроорганизмов, получившие 3 балла в соответствии с алгоритмом (см. рис. 1). Микроорганизмы, получившие 2 или 1 балл, могут исследоваться дополнительно, например, при проведении выборочных целевых программ эпидемиологического слежения.
Выбор метода исследования чувствительности микроорганизмов к антибиотикам определяется этапом мониторинга. На предварительном этапе допускается проведение оценки чувствительности изолятов к антибиотикам диско-диффузионным методом. Определение чувствительности на основном этапе проводится с использованием макро- или микрометода последовательных разведений, градиен-тного метода, полуавтоматических и автоматических устройств. Планшетные тест-системы (коммерческие варианты метода микроразведений в бульоне) являются наиболее предпочтительными.
Использование унифицированных методов определения чувствительности и подходов к интерпретации результатов является необходимым условием для формирования единой системы обработки, анализа, составления отчетов и обмена данными. Получение информации о характеристике чувствительности/устойчивости изолята к антибиотикам проводится на основании следующих данных:
– пороговой концентрации (ПК) – значение ингибирующей концентрации антибиотика, используемой для отнесения изолятов к имеющим или не имеющим фенотипически выявляемых механизмов резистентности; пороговые значения антибиотиков выражаются в числовых значениях более нуля (мг/л) в соответствии с рекомендациями EUCAST. Допускается использовать специальное пороговое значение при интерпретации данных, для которых пороговые значения не определены;
– нижней пороговой концентрации (НПК) – самой низкой концентрации антибиотика из диапазона концентраций, используемой при исследовании чувствительности к антимикробным препаратам в лаборатории методом последовательных разведений; самая низкая концентрация антибиотика должна находиться в диапазоне от «0,002» до «4096» (мг/л) и быть меньше верхней пороговой концентрации; рекомендуется предусмотреть, чтобы НПК входила в диапазон субингибирующей концентрации;
– верхней пороговой концентрации (ВПК) – самой высокой концентрации антибиотика из диапазона концентраций, используемой при исследовании чувствительности к антимикробным препаратам в лаборатории методом последовательных разведений; самая высокая концентрация антибиотика должна находиться в диапазоне от «0,002» до «4096» (мг/л) и быть больше НПК;
– минимальной ингибирующей концентрации (МИК) – значение концентрации антибиотика (мг/л), полученное в результате определения чувствительности рассматриваемого изолята, при которой in vitro полностью подавляется видимый рост бактерий. Значение МИК должно находиться между «0,002» и «4096». Если при проверенной НПК рост изолята не наблюдается, значение МИК должно быть указано как ниже или равное НПК. Если рост все еще наблюдается при проверенной ВПК, значение МИК следует указывать как большее, чем проверенная ВПК;
– ингибирующей концентрации (ИК) – значение МИК антибиотика (мг/л), равное от ½ ПК и более;
– субингибирующей концентрации (СИК) – значение концентрации антибиотика (мг/л), равное от ¼ ПК до 1/16 ПК и менее.
Пример разметки планшета и оценки чувствительности изолята E. сoliмикрометодом серийных разведений представлен на рисунке 2.

Проведена валидация метода на основе серии исследований чувствительности изолята E. coli, выделенного из пищевого продукта. Для испытания выбран антибиотик ампициллин в соответствии с рекомендуемым перечнем антибиотиков. Диапазон концентраций, отобранных для испытания, рассчитан с учетом пороговой концентрации (ПК) таким образом, чтобы можно было оценить результат в пределах от 1/16 ПК до 4 ПК. Для ампициллина значение ПК равно значению ингибирующей концентрации антибиотика, используемой для отнесения изолятов к имеющим или не имеющим фенотипически выявляемых механизмов резистентности, ПК для ампициллина в отношении изолята E. coliравна 8 мг/л. Верхняя пороговая концентрация (ВПК), используемая при исследовании чувствительности изолята E. coliк ампициллину в лаборатории методом последовательных разведений, равна 4 ПК – 32 мг/л. Нижняя пороговая концентрация (НПК), используемая при исследовании чувствительности изолята E. coliк ампициллину в лаборатории методом последовательных разведений, равна 1/16 ПК – 0,5 мг/л. Двойные серийные разведения, основанные на 1 мг/л, готовили в бульоне Мюллера – Хинтона.
После инкубирования планшетов в течение 24 чассов при температуре 37 °С проводился учет наличия/отсутствия роста в лунках с различной концентрацией антибактериального агента и установлением значения МИК с использованием лупы с увеличительным зеркалом. Результаты серии измерений получены в условиях внутрилабораторной воспроизводимости. Проведено 12 измерений в двух повторностях двумя операторами (xia и xiв).
В ходе исследования оценивали показатели прецизионности: стандартное отклонение воспроизводимости Sr (промежуточной прецизионности) и максимальную расширенную неопределенность U.
За окончательный результат измерения принимали среднее арифметическое значение двух результатов значения ПК (мг/л) параллельных измерений, рассчитанное по формуле
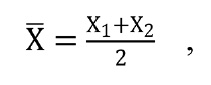
где Х1 – результат первого параллельного измерения, Х2 – результат второго параллельного измерения.
Значения результатов измерений, переведенные в log10, их квадраты разности приведены в таблице 1.
Таблица 1. Расчет стандартного отклонения воспроизводимости
|
Индекс образца
|
Индекс фактора оператора
|
Результат измерений,
преобразованный в log10
|
Стандартное отклонение
воспроизводимости
|
|
i
|
xiA
|
xiB
|
yiA=log10 (xiA)
|
yiB=log10 (xiB)
|
(yiA-yiB)2/2
|
|
1
|
4
|
3
|
0,602
|
0,477
|
0,0078
|
|
2
|
3
|
4
|
0,477
|
0,602
|
0,0078
|
|
3
|
4
|
3
|
0,602
|
0,477
|
0,0078
|
|
4
|
2
|
4
|
0,301
|
0,602
|
0,0453
|
|
5
|
4
|
3
|
0,602
|
0,477
|
0,0078
|
|
6
|
4
|
4
|
0,602
|
0,602
|
0
|
|
7
|
3
|
4
|
0,477
|
0,602
|
0,0078
|
|
8
|
6
|
3
|
0,778
|
0,477
|
0,0453
|
|
9
|
3
|
4
|
0,477
|
0,602
|
0,0078
|
|
10
|
4
|
2,5
|
0,602
|
0,398
|
0,0208
|
|
11
|
3
|
4
|
0,477
|
0,602
|
0,0078
|
|
12
|
4
|
4
|
0,602
|
0,602
|
0
|
Оценку стандартного отклонения воспроизводимости Sr (промежуточной прецизионности) проводили по формуле
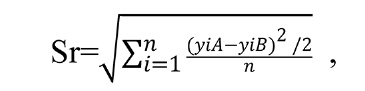
где yn – результат измерений, преобразованный в log10 МИК (мг/л); i – индекс образца, i=1, 2, 3, … n (n=12); A, B – индекс фактора оператора, A или B.
Оценку неопределенности измерения проводили согласно ISO 29201:2012. Расширенную неопределенность U с коэффициентом охвата 2 (приблизительно соответствующим доверительному интервалу 95%) рассчитывали по формуле
U=2 Sr ,
где Sr – стандартное отклонение воспроизводимости (промежуточной прецизионности), log10 МИК (мг/л).
Значения показателя прецизионности и максимальной расширенной неопределенности при уровне доверия р=0,95 приведены в таблице 2.
Таблица 2. Расчет стандартного отклонения воспроизводимости
|
Показатель
|
МИК, мг/л
|
log10 (МИК, мг/л)
|
|
Стандартное отклонение воспроизводимости
|
0,12
|
-0,92
|
|
Максимальная расширенная неопределенность
|
0,24
|
-0,62
|
В соответствии с ГОСТ Р 54502-2011/ISO/TS 19036:2006 «Микробиология продуктов питания и кормов для животных. Руководство по оценке неопределенности при количественных определениях» полученная оценка расширенной неопределенности относится к единичному измерению и может быть использована как максимальная оценка неопределенности для результата измерения, получаемого в соответствии с валидируемым методом.
Таблица 3. Результаты исследования чувствительности изолята E.сoli к антибиотикам
|
Антибиотик для тестирования
|
ПК, мг/л
|
НПК, мг/л
|
ВПК, мг/л
|
МИК, мг/л
|
Диапазон МИК
|
|
Ампициллин
|
8
|
0,5
|
32
|
2
|
1/4 ПК
|
|
Цефотаксим
|
2
|
0,125
|
8
|
1
|
1/2 ПК
|
|
Цефтазидим
|
4
|
0,25
|
16
|
0,5
|
1/8 ПК
|
|
Хлорамфеникол
|
8
|
0,5
|
32
|
8
|
ПК
|
|
Ципрофлоксацин
|
0,5
|
0,03
|
2
|
2
|
4 ПК
|
|
Колистин
|
2
|
0,125
|
8
|
0,5
|
1/4 ПК
|
|
Гентамицин
|
2
|
0,125
|
8
|
0,25
|
1/8 ПК
|
|
Триметоприм-
сульфаметоксазол
|
4
|
0,25
|
16
|
<0,25
|
<1/16 ПК
|
|
Тигециклин
|
0,5
|
0,03
|
2
|
0,06
|
1/8 ПК
|
|
Цефепим
|
4
|
0,25
|
16
|
1
|
1/4 ПК
|
|
Имипенем
|
4
|
0,25
|
16
|
2
|
1/2 ПК
|
|
Эртапенем
|
0,5
|
0,03
|
2
|
0,25
|
1/2 ПК
|
Примечание: ВПК – верхняя пороговая концентрация, НПК – нижняя пороговая концентрация, ПК – пороговая концентрация, МИК – минимальная ингибирующая концентрация.
Для формирования единой системы обработки и анализа данных необходима единая форма представления отчетов. В таблице 3 представлен пример оформления полученных результатов по определению чувствительности изолята E. сoliк антибиотикам.
Заключение
Основными этапами нового метода лабораторной оценки антибиотикорезистентности возбудителей из группы пищевых бактериальных патогенов являются: определение категории эпидемиологической значимости и уровня приоритета выделенных микроорганизмов для мониторирования; отбор изолятов, подлежащих эпидемиологическому слежению за распространением резистентности к антибиотикам; выбор лабораторного метода проведения оценки чувствительности на предварительном этапе; определение антибиотикорезистентности на основном этапе с использованием макро- или микрометода последовательных разведений, градиентного метода, полуавтоматических и автоматических устройств, при этом планшетные тест-системы являются наиболее предпочтительными; проведение оценки характеристики чувствительности/устойчивости изолята к антибиотикам на основании определения пороговой концентрации, нижней пороговой концентрации, верхней пороговой концентрации, минимальной ингибирующей концентрации, ингибирующей концентрации и субингибирующей концентрации; представление результатов исследования путем внесения данных по единой форме отчета; формирование единой системы обработки и анализа данных.
По итогам проведенных исследований разработана и утверждена инструкция по применению [7]. Полученные данные являются необходимым источником для создания и осуществления страновых стратегий борьбы с растущей антибиотикорезистентностью в здравоохранении, пищевой безопасностью, выявления факторов риска и предотвращения вспышек инфекционных заболеваний.
Л И Т Е Р А Т У Р А
1. Caniça M. [et al.] // Trends Food Sci. Technol. – 2019. – Vol.84. – P.41–44.
2. Rincón-Gamboa S.M. [et al.] // Foods. – 2021. – Vol.10. – P.1731.
3. Medalla F. [et al.] // Emerg. Infect. Dis. – 2016. – Vol.23. – P.29–37.
4. Melzer M., Petersen I. // J. Infect. – 2007. – Vol.55. – P.254–259.
5. Guidelines for risk analysis of foodborne antimicrobial resistance. CAC/GL 77-2011 // Food and Agriculture Organization of the United Nations and World Health Organization, Rome. – 2011.
6. Тонко О.В., Коломиец Н.Д., Ханенко О.Н., Семашко Д.А. Оценка формирования антибиотикорезистентности пищевых бактериальных патогенов Здоровье и окружающая среда: сб. науч. тр. / редкол.: С.И. Сычик [и др.]. – Минск, 2022. – С.269–277.
7. Инструкция по применению 017-1221. Метод оценки риска формирования антибиотикорезистентности у бактерий, выделенных из продовольственного сырья и пищевых продуктов: утв. постановлением Гл. гос. санитар. врача Респ. Беларусь 28.01.2022. – Минск, 2022. – 22 с.
Медицинские новости. – 2023. – №5. – С. 67-71.
Внимание! Статья адресована врачам-специалистам. Перепечатка данной статьи или её фрагментов в Интернете без гиперссылки на первоисточник рассматривается как нарушение авторских прав.