Внимание! Статья адресована врачам-специалистам
TrisvetovaE.L.
Belarusian State Medical University, Minsk
Antihypertensive therapy for polymorbidity in clinical practice
Реферат. У пациентов с артериальной гипертензией часто встречается полиморбидность, увеличивающая риск развития осложнений и ухудшающая прогноз жизни. Выбор рациональной терапии, влияющей на разные механизмы артериальной гипертензии и на патогенез других выявленных заболеваний пациента, важен в практической деятельности. Применение фиксированных комбинаций антигипертензивных препаратов позволяет сохранить комплаентность к лечению, избежать полипрагмазии и уменьшить число нежелательных реакций лекарственных средств. Фиксированная комбинация ингибитора АПФ (лизиноприл) и блокатора кальциевых каналов (амлодипин) эффективна для контроля артериального давления, органопротекции и влияет на симптомы и течение других заболеваний (ишемическая болезнь сердца, хроническая обструктивная болезнь легких, нефропатия, неалкогольная жировая болезнь печени) пациента.
Ключевые слова: артериальная гипертензия, лечение, полиморбидность, фиксированная комбинация, ингибитор АПФ, блокатор кальциевых каналов.
Медицинские новости. – 2020. – №12. – С. 31–36.
Summary. In patients with arterial hypertension, polymorbidity is common, increasing the risk of complications and worsening the prognosis of life. The choice of rational therapy that affects different mechanisms of arterial hypertension and the pathogenesis of other identified diseases of the patient is important in practice. The use of fixed combinations of antihypertensive drugs allows you to maintain compliance with treatment, avoid polypharmacy and reduce the number of adverse drug reactions. The fixed combination of an ACE inhibitor (lisinopril) and a calcium channel blocker (amlodipine) is effective for blood pressure control, organoprotection, and affects the symptoms and course of other diseases (coronary heart disease, chronic obstructive pulmonary disease, nephropathy, non-alcoholic fatty liver disease) of the patient.
Keywords: arterial hypertension, treatment, polymorbidity, fixed combination, ACE inhibitor, calcium channel blocker.
Meditsinskie novosti. – 2020. – N12. – P. 31–36.
Артериальная гипертензия (АГ) на протяжении десятилетий является одним из наиболее распространенных заболеваний среди взрослого населения во всем мире. Результаты эпидемиологических исследований показали, что в странах с низким, средним или высоким уровнем дохода распространенность АГ одинакова и составляет 30–45% [1]. Достижением множества клинических исследований являются доказательства, свидетельствующие о том, что снижение артериального давления (АД) значительно уменьшает преждевременную заболеваемость и смертность [2, 3]. Изменение образа жизни, применение лекарственных средств для контроля АД позволяют снизить риск развития неблагоприятных сердечно-сосудистых событий и существенно улучшить прогноз у пациентов с АГ.
При выборе антигипертензивной терапии учитывают сердечно-сосудистый риск, наличие факторов риска, поражение органов, опосредованное АГ, и влияние препаратов на течение других заболеваний. При полиморбидности клинические проявления и патогенез одновременно существующих патологий у одного пациента увеличивают риск развития осложнений и летальность у пациентов с АГ.
Коморбидность, мультиморбидность, полиморбидность
В настоящее время существует множество терминов для обозначения нескольких заболеваний, протекающих одновременно у одного пациента [4, 5]. Наиболее точно суть проблемы отражают термины «коморбидность» и «мультиморбидность». Коморбидность – это множественные заболевания у индивидуума, связанные с доказанным единым патогенетическим механизмом. Термин «коморбидность» предложил американский эпидемиолог A.R. Feinstein в 1970 году, считая, что наличие любого сопутствующего заболевания, появившееся или существующее, помимо текущего заболевания, следует обозначать как коморбидное [6]. В дальнейшем появился термин «мультиморбидность», который применяют при наличии у индивидуума нескольких синхронно протекающих заболеваний в различных фазах и стадиях своего развития [7].
Л.Б. Лазебник и соавт. для обозначения нескольких заболеваний у одного пациента предложили обобщающее понятие «полиморбидность», выделяя коморбидность (наличие сопутствующих заболеваний, связанных единым патогенетическим механизмом) и мультиморбидность (наличие множественных заболеваний, не связанных патогенетическими механизмами, доказанными на настоящий момент). Вместе с тем авторы считают, что деление полиморбидности на мультиморбидность и коморбидность носит условный характер [4].
По определению Всемирной организации здравоохранения, мультиморбидность – это состояние, включающее наличие двух и более хронических заболеваний, этиопатогенетически не связанных между собой. В среднем у одного человека насчитывают 5,8 заболеваний, в России 44% взрослого населения отвечают указанным критериям [8, 9].
Согласно результатам исследования C. Salisbury и соавт., в случайной выборке из 99 987 человек в возрасте 18 лет и старше, зарегистрированных в 182 клиниках Англии, в 16% случаев выявлено более одного хронического заболевания [10]. Наличие полиморбидности зависело от возраста – чем старше пациент, тем обнаруживали большее количество заболеваний, и социального положения человека – при значительных социальных ограничениях выявляли большее количество болезней (рис. 1).
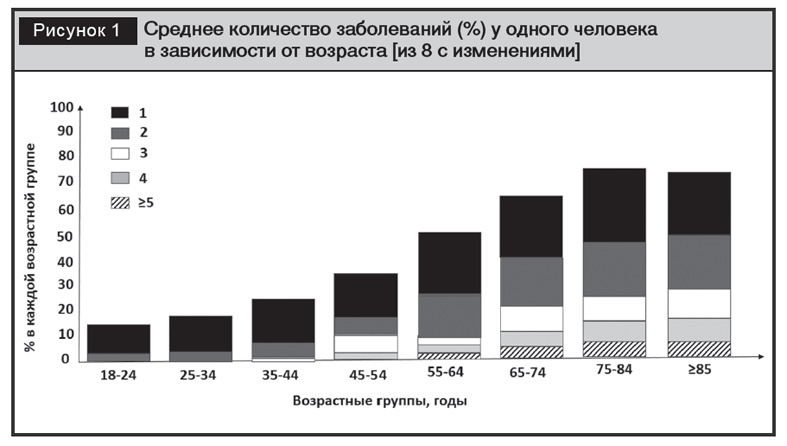
В более позднем ретроспективном исследовании, выполненном в Англии с использованием медицинской документации 403 985 человек в возрасте старше 18 лет, полиморбидность (учитывали два заболевания и более) выявили у 27,2% пациентов [11]. Авторы также отметили увеличение количества заболеваний в старших возрастных группах по сравнению с группами молодого возраста, и в случае худшего социального обеспечения человека.
В исследовании F.G. Schellevis с участием 212 900 человек от 0 до >74 лет полиморбидность выявили в 12,9% случаев, в том числе у мужчин – в 10,9%, у женщин – в 15,9% случаев. Под полиморбидностью авторы понимали наличие более 2 заболеваний у одного пациента [12]. Исследователи отметили, что по сравнению с группой 15–24 года в возрастной группе 25–54 лет количество случаев полиморбидности возросло в 4 раза, а в возрасте 55–65 лет – в 11 раз (рис. 2).
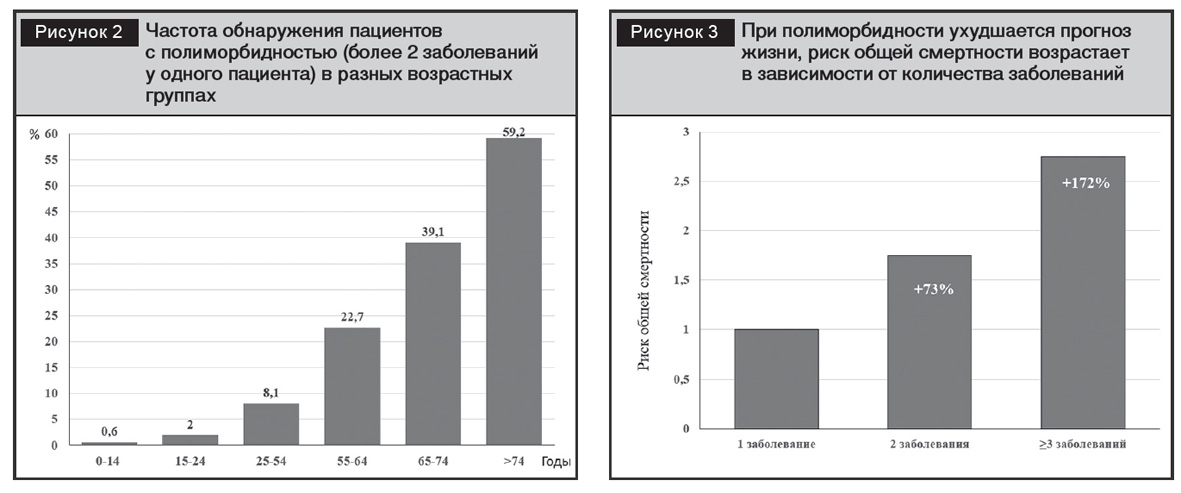
В обзоре статей, опубликованных в базах данных PubMed, Scopus, PsycINFO и Grey, F. Abebe и соавт. представили анализ эпидемиологии полиморбидности в странах со средним и низким уровнем дохода [13]. В 76 найденных исследованиях выявили значительные различия в критериях полиморбидности (от двух до шести заболеваний и более) и распространенности (3,2–90,5%). Наиболее распространены сахарный диабет, АГ, хроническая обструктивная болезнь легких, остеоартрит, сердечно-сосудистые заболевания, рак и депрессия. У женщин, что, вероятно, связано с более частой обращаемостью за медицинской помощью, полиморбидность выявляли чаще по сравнению с мужчинами. Социально-экономический статус, по мнению авторов, не оказывал влияния на полиморбидность.
Известно, что полиморбидность ухудшает качество и прогноз жизни, риск общей смертности возрастает и зависит от количества заболеваний у одного пациента [14] (рис. 3).
Несмотря на то, что для оценки полиморбидности в клинической практике созданы системы и индексы (CIRS, индекс Kaplan – Feinstein, индекс ICED, GIC, CDS, ACG, Charlson и DUSOI), ни один из предложенных методов из-за отсутствия валидизации и стандартизации не применим в оте-чественной клинической практике [15, 16].
Таким образом, существующие показатели полиморбидности значительно варьируют, поскольку выполнение эпидемиологических исследований в связи с отсутствием стандартизированных критериев полиморбидности и использованием различных терминологических понятий вызывает трудности.
В 2017 году общероссийской общественной организацией «Ассоциация врачей общей практики» опубликованы клинические рекомендации «Коморбидная патология в клинической практике» [17]. В Рекомендациях, достаточно компактном документе для практических врачей, обобщен мировой опыт по изучению и курации пациентов с коморбидной патологией.
Артериальная гипертензия и полиморбидность
Артериальная гипертензия, являясь одним из наиболее распространенных хронических заболеваний сердечно-сосудистой системы, относится к факторам риска развития атеросклероза, ишемической болезни сердца (ИБС) и сердечной недостаточности, хронической болезни почек и почечной недостаточности, цереброваскулярных заболеваний, в том числе инсульта и сосудистой деменции.
В исследованиях Е.В. Севостьяновой и соавт. на основе анализа 20 560 историй болезни пациентов с АГ и без АГ изучена структура и степень полиморбидности в зависимости от пола и возраста [18]. В группе с АГ по сравнению с пациентами без АГ часто встречались сердечно-сосудистые заболевания (рис. 4).

Исследователи отметили, что у мужчин с АГ в возрасте 16–39 лет сердечно-сосудистые заболевания встречались чаще на 46%, 40–59 лет – на 36,2%, старше 60 лет – на 9,2% по сравнению с пациентами без АГ. Такая же закономерность и большая частота сердечно-сосудистых заболеваний у пациентов с АГ наблюдалась у женщин (на 42,8%, 39,3% и 9,3% соответственно).
Помимо сердечно-сосудистых заболеваний при АГ у мужчин и женщин отмечена большая частота заболеваний эндокринной, мочеполовой и костно-мышечной системы, органов пищеварения и дыхания, ожирения [17, 18].
Известно, что при АГ отмечена высокая частота встречаемости атеросклероза и его предикторов: атерогенной дислипидемии, гипергликемии, абдоминального ожирения, эндотелиальной дисфункции, связанных общим патогенетическим механизмом – инсулинорезистентностью. В совокупности эти факторы риска, объединенные термином «метаболический синдром», усугубляют атерогенез, способствуют развитию и прогрессированию сердечно-сосудистых заболеваний (ишемическая болезнь сердца, цереброваскулярные заболевания, нефропатия). В случае развития метаболического синдрома в течение последующих 5–10 лет риск появления сахарного диабета возрастает в 5 раз, сердечно-сосудистых заболеваний или внезапной сердечной смерти – в 2 раза [19]. Результаты исследований показали, что гипергликемия и гиперинсулинемия повышают активность ренин-ангиотензин-альдостероновой системы (РААС) и симпатоадреналовой системы (СНС), внося тем самым вклад в развитие АГ. К тому же, адипоциты, основные клетки жировой ткани, также продуцируют альдостерон и их рассматривают как миниатюрную РААС [20].
Помимо сердечно-сосудистых заболеваний у пациентов с АГ часто (в 49,6–63,4% случаев) выявляют хроническую обструктивную болезнь легких (ХОБЛ), увеличивающую инвалидизацию и риск смерти [21, 22]. В настоящее время установлено, что 50% смертей у пациентов с ХОБЛ обусловлено сердечно-сосудистыми заболеваниями [23]. Повышенный риск развития сердечно-сосудистой патологии является результатом системного воспаления при ХОБЛ, потенцирующего действие других факторов риска, таких как эндотелиальная дисфункция и вазоконстрикция, нарушения углеводного и липидного обмена, прогрессирование атеросклероза (рис. 5).
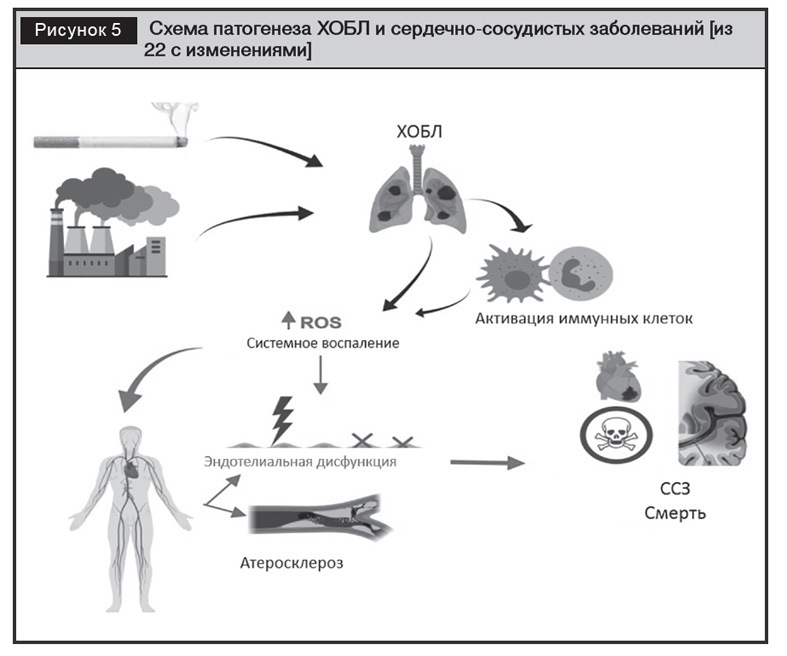
Исследователи отметили особенности суточного профиля АД у пациентов с АГ и ХОБЛ, выражающиеся в высокой вариабельности систолического и диастолического АД и недостаточным снижением в ночное время [24]. Недостаточный контроль АГ из-за трудностей, возникающих при выборе антигипертензивных препаратов у пациентов с АГ и ХОБЛ, обусловливает более выраженное поражение органов, опосредованных АГ, развитие сердечно-сосудистых осложнений.
Так, согласно Роттердамскому проспективному исследованию, в котором участвовали 13 115 человек, при тяжелом обострении ХОБЛ риск возникновения геморрагического или ишемического инсульта повышается в 6,6 раза [25]. Результаты того же исследования, опубликованные годом ранее, свидетельствовали о возрастании риска внезапной сердечной смерти в течение 5 лет с момента диагностики заболевания у пациентов с ХОБЛ с частыми обострениями [26].
У большинства пациентов с АГ, атеросклерозом, сердечно-сосудистыми заболеваниями развивается неалкогольная жировая болезнь печени (НАЖБП), включающая стеатоз, неалкогольный стеатогепатит или цирроз печени (рис. 6).

В многоцентровом проспективном исследовании НАЖБП-DIREG_L_01903 у амбулаторных пациентов НАЖБП обнаружена в 27,9% случаев, в том числе при дислипидемии в 75,9%, при АГ в 69,9%, при гиперхолестеринемии в 86,8% [27]. У пациентов с метаболическим синдромом НАЖБП встречается в 100% случаев и рассматривается как обязательный компонент. Исследователи отмечают у пациентов с АГ и НАЖБП большее повышение риска развития сердечно-сосудистых осложнений по сравнению с пациентами без поражения печени вследствие значительных нарушений эндотелиальной функции, высокой жесткости артериальных сосудов и «увеличения» сосудистого возраста [28].
Таким образом, у пациентов с АГ часто выявляют полиморбидность, включающую заболевания сердечно-сосудистой, респираторной системы, почек, печени, усугубляющую течение заболевания и повышающую риск развития серьезных осложнений, ухудшающую качество жизни и лечебно-диагностический процесс.
Обоснование выбора антигипертензивных препаратов при полиморбидности
Наличие полиорганных изменений и функционального нарушения многих систем у пациентов с АГ и полиморбидностью обосновывает необходимость одновременного назначения не менее 2–3 лекарственных средств по поводу каждого из заболеваний. При расчете минимального назначения по 2 препарата на 5 имеющихся заболеваний пациент должен принимать ежедневно по 10 препаратов, вместе с тем известно, что комплаентность к лечению обратно пропорциональна количеству назначенных медикаментов [17]. Для того, чтобы избежать полипрагмазии, способствующей возрастанию появления нежелательных побочных реакций лекарственных средств, снижения комплаентности и достичь эффективного контроля АГ, необходимо применять комбинации препаратов, влияющих на многие звенья патологических процессов, обусловленных полиморбидностью.
При выборе антигипертензивного препарата необходимо учитывать следующие факторы, влияющие на развитие полиморбидности: генетические, системные метаболические изменения (нарушения липидного, углеводного, минерального обмена, гормонального статуса), анатомическую и физиологическую взаимосвязь, хроническую инфекцию, инволютивные изменения, ятрогенные, социальные, экологические.
Известно, что представители всех пяти основных классов антигипертензивных препаратов, снижающих АД, значительно уменьшают риск развития серьезных сердечно-сосудистых событий. Так, снижение АД систолического на 10 мм рт. ст. и диастолического – на 5 мм рт. ст. уменьшает риск возникновения сердечно-сосудистых осложнений на 20%, общей смертности – на 10–15%, коронарных событий – на 20% и сердечной недостаточности – на 40% [29]. За истекшие годы по результатам, полученным в рандомизированных клинических исследованиях, установлен первый целевой уровень АД <140/90 мм рт. ст., при хорошей переносимости лечения целевым считают второй уровень <130/80 мм рт. ст. с индивидуальным подходом к уровню систолического АД у пожилых людей [30].
Согласно современным рекомендациям по лечению АГ, антигипертензивную терапию направляют не только на достижение целевого уровня АД, но и на уменьшение сердечно-сосудистого риска [30]. Большинству пациентов с АГ и полиморбидностью показана комбинация антигипертензивных лекарственных средств, целесообразным является назначение двух компонентов в одной таблетке.
Рекомендуемая и наиболее часто применяемая фиксированная комбинация включает ингибитор АПФ (ИАПФ) и блокатор кальциевых каналов (БКК) [30, 31].
Препараты класса ИАПФ вызывают замедление и обратное развитие поражения органов, опосредованных АГ: уменьшают гипертрофию левого желудочка, препятствуя его дилатации, и развитие фиброза; уменьшают суммарную толщину интимы и медии сонных артерий; оказывают нефропротективный эффект в виде замедления прогрессирования диабетической и недиабетической нефропатии, оказывают метаболические эффекты в виде усиления распада липопротеидов очень низкой плотности и снижения синтеза триглицеридов, повышения чувствительности клеточных рецепторов к инсулину и усилению потребления глюкозы [31, 32]. Назначение этих препаратов считают обязательным в лечении хронической сердечной недостаточности, поскольку доказано их влияние на прогноз жизни пациентов [29].
Важное место в лечении лиц с АГ и полиморбидностью занимают препараты класса БКК. Дигидропиридиновые БКК особенно эффективны в профилактике инсультов, замедлении прогрессирования коронарного атеросклероза, не связанного с гипотензивным действием, и диабетической нефропатии, у пожилых людей [30]. Препараты проявляют антиаритмическое действие и снижают агрегацию тромбоцитов, что свидетельствует об эффективности при ИБС. БКК у пациентов с АГ и ХОБЛ уменьшают легочную вазоконстрикцию, снижают давление в легочнои? артерии и неспецифическую гиперреактивность бронхов, усиливают бронхолитическии? эффект ?2-агонистов [33, 34]. В крупных рандомизированных клинических исследованиях (ALLHAT, CAPE, CAPARES) доказана эффективность и безопасность применения БКК амлодипина при АГ и ИБС, а также антиатерогенное действие у пациентов с атеросклерозом коронарных и каротидных артерий (PREVENT) [17].
При назначении фиксированной комбинации ИАПФ и БКК наблюдают взаимное потенцирование влияния на гемодинамику, способствующее достижению целевого уровня АД у большинства пациентов, органопротективное (кардио- и нефропротекция) действие комбинации, снижение частоты нежелательных реакций препаратов. Комбинация ИАПФ и БКК не ухудшает чувствительности к инсулину, не оказывает негативного влияния на углеводный и липидный обмен, проявляет профилактические эффекты в отношении нарушений когнитивных функций у пожилых пациентов, не ухудшает кровоток в периферических сосудах при атеросклеротическом поражении, не ухудшает функциональное состояние печени при НАЖБП [17, 28].
Согласно результатам исследований, ИАПФ эффективны при ХОБЛ, поскольку оказывают влияние на бронхиальную обструкцию за счет снижения уровня ангиотензина II, улучшения альвеолярного газообмена, уменьшения легочного воспаления, а также уменьшения вазоконстрикции и снижения давления в легочной артерии [34]. В исследованиях отмечено положительное влияние препаратов класса ИАПФ на конечные точки сердечно-сосудистых осложнений: при применении ИАПФ снижается риск обострения ХОБЛ, частота госпитализаций по поводу обострения и смертность из-за респираторного заболевания [35]. Не отмечено негативное взаимодействие ИАПФ с препаратами, применяемыми при ХОБЛ (?2-агонисты, м-холинергические, антибиотики).
М.В. Стаценко и соавт. в течение 24 недель оценивали влияние комбинации ИАПФ лизиноприла 12,3±5,0 мг/сут и амлодипина 6,2±2,5 мг/сут у пациентов с АГ III стадии и сахарным диабетом 2-го типа, получавших гиполипидемическую и комбинированную сахароснижающую терапию [37]. Результаты лечения свидетельствовали о достоверном снижении офисного АД (систолического – на 22,3%, диастолического – на 12,5%), частоты сердечных сокращений на 9,8%, уровня HbA1С на 1,4% по сравнению с исходными значениями (рис. 7).

Достоверное улучшение показателей центральной гемодинамики в виде снижения среднесуточных, дневных и ночных значении? систолического и диастолического АД, пульсового АД, индекса аугментации в аорте наблюдали после 24 недель лечения. Авторы отметили снижение висцерального жира, по данным биоимпедансометрии, на 13,6% и VAI – на 22,5%, уменьшение доли пациентов с очень высоким уровнем висцерального жира (?%=-36,7, р<0,05).
Таким образом, применение фиксированной комбинации лизиноприла и амлодипина Экватор (ОАО «Гедеон Рихтер», Венгрия) показало высокую антигипертензивную эффективность и способность достоверно улучшать показатели центрального АД, оказывая дополнительное положительное метаболическое действие, без коррекции дозы статинов и сахароснижающих препаратов, снижение активности висцерального ожирения.
В настоящее время фиксированная комбинация лизиноприла и амлодипина Экватор успешно применяется для лечения пациентов с АГ и полиморбидностью. Лизиноприл является активным действующим веществом, не пролекарством, как остальные препараты класса ИАПФ. Препарат не трансформируется в печени и не конкурирует с другими лекарственными средствами за систему цитохрома Р450, не связывается с белками плазмы (кроме АПФ), поэтому его применение не ограничивает назначение других препаратов для лечения сердечно-сосудистых и других заболеваний. Лизиноприл относится к гидрофильным средствам, не проникает в жировую ткань и не нуждается в коррекции дозы в зависимости от массы тела.
Дигидропиридиновый БКК амлодипин за счет блокады кальциевых механизмов вазоконстрикции и атерогенеза усиливает сосудистое воздействие лизиноприла, обусловливая дополнительные антиангинальные, антиспастические и антисклеротические свойства. Амлодипин оказывает выраженное сосудорасширяющее действие, снижает периферическое сосудистое сопротивление, оказывая антигипертензивный эффект, не влияя на сердечную проводимость и/или сократительную способность миокарда. Благодаря 24-часовой продолжительности действия фиксированной комбинации лизиноприла с амлодипином достигается меньшая вариабельность АД в течение суток, что способствует повышению приверженности к лечению пациентов.
При назначении фиксированной комбинации лизиноприла и амлодипина пациентам с АГ и полиморбидностью наблюдают положительные эффекты при заболеваниях, патогенетически связанных – ИБС, метаболический синдром, атеросклероз, хроническая сердечная недостаточность, нефропатия, и заболеваниях других органов – ХОБЛ, НАЖБП.
Заключение
Распространенность полиморбидности, обусловленной многими факторами, возрастает во всем мире и повышает показатели инвалидизации, смертности населения и увеличения побочных нежелательных реакций лекарственных средств. Понимание сложности проблемы лечения пациентов со многими заболеваниями необходимо практическому врачу. Для эффективного контроля АГ, как одного из самых распространенных заболеваний, протекающих с полиморбидностью, решением проблемы является выбор рациональной антигипертензивной терапии, включающей фиксированные комбинации препаратов.
Л И Т Е Р А Т У Р А
1. Chow C.K., Teo K.K., Rangarajan S., et al. PURE Study Investigators. Prevalence, awareness, treatment, and control of hypertension in rural and urban communities in high-, middle-, and low-income countries // JAMA. – 2013. – Vol.310. – P.959–968.
2. Thomopoulos C., Parati G., Zanchetti A. Effects of blood pressure lowering on outcome incidence in hypertension. Overview, meta-analyses, and meta-regression analyses of randomized trials // J. Hypert. – 2014. – Vol.329, N12. – P.2285–2295.
3. Yusuf S., Hawken S., ?npuu S., et al. Effect of potentially modifiable risk factors associated with myocardial infarction in 52 countries (the INTERHEART study): case-control study // Lancet. – 2004. – Vol.364. – P.937–952.
4. Лазебник Л.Б., Ефремов Л.И., Конев Ю.В. Семантические трудности при полиморбидности // Клин. геронтология. – 2015. – Vol.3–4. – P.44–46.
5. Meghani S.H., Dickson V.V., Hammer M.J., et al. Conceptualization and Measurement of Comorbidity: A Review of the Interprofessional Discourse // Nurs Res. Pract. – 2013. – Vol.2013. – P.19782.
6. Feinstein A.R. The pre-therapeutic classification of co-morbidity in chronic disease // J. Chronic Dis. – 1970. – Vol.23, N7. – P.455–468.
7. Jakovljevic M., Ostojic L. Comorbidity and multimorbidity in medicine today: challenges and opportunities for bringing separated branches of medicine closer to each other // Psychiatr. Danub. – 2013. – Vol.1, N1. – P.18–28.
8. van den Bussche H., Schön G., Tina Kolonko T., et al. Patterns of ambulatory medical care utilization in elderly patients with special reference to chronic diseases and multimorbidity-results from a claims data based observational study in Germany // BMC Geriatr. – 2011. – Vol.11. – P.54.
9. Насонов Е.Л., Гордеев А.В., Галушко Е.А. Концепции коморбидности и мультиморбидности в ревматологии. Возможна ли смена парадигм? // Медицина (Алматы). – 2018. – Vol.318, N9. – P.27–31.
10. Salisburi C., Johson L., Purdy S., et al. Epidemiology and impact of multimorbidity in primary care: a retrospective cohort study // Br. J. Gen pract. – 2011. – Vol.61, N582. – e112–e121.
11. Cassel A., Edwards D., Harshfield A., et al. The epidemiology of multimorbidity in primary care: a retrospective cohort study // Br. J. Gen Pract. – 2018. – Vol.669, N68. – e245–e251.
12. Schellevis F.G., Velden J., Lisdonk E. Comorbidity of chronic diseases in general practice // J. Clin. Epidemiol. – 1993. – Vol.46. – P.469–473.
13. Abebe F., Schneider M., Asray B., et al. Multimorbidity of chronic non-communicable diseases in low- and middle-income countries: A scoping review // J. Comorb. – 2020. – Vol.10. – P.2235042X20961919.
14. Nunes B.P., Flores T.R., Mielke G.I., et al. Multimorbidity and mortality in older adults: A systematic review and meta-analysis. Arch of Gerontology and Geriatrics. – 2016. – Vol.67. – P.130–138.
15. Klabunde C.N., Potosky A.L., Legler J.M., et al. Development of a comorbidity index using physician claims data // J. Clin. Epidemiol. – 2000. – Vol.53, N12. – P.1258–1267.
16. Huntley A.L., Johson R., Purdy S., et al. Measures of Multimorbidity and Morbidity Burden for Use in Primary Care and Community Settings: A Systematic Review and Guide // Annals of Family Medicine. – 2012. – Vol.10, N2. – P.134–141.
17. Оганов Р.Г., Денисов И.Н., Симаненков В.И. и др. Коморбидная патология в клинической практике: Клинические рекомендации // Кардиоваскулярная терапия и профилактика. – 2017. – №16 (6). – С.5–56.
18. Севостьянова Е.В., Николаев Ю.А., Митрофанов И.М. и др. Особенности полиморбидности у больных артериальной гипертензией // Артериальная гипертензия. – 2019. – N25 (2). – C.200–208.
19. Kaur J. A comprehensive Review on Metabolic Syndrome // Cardiol Res Pract. – 2014. – Vol.943162.
20. Briones A.M., Cat A.N.D., Callera G.E., et al. Adipocytes produce aldosterone through calcineurin-dependent signaling pathways: implications in diabetes mellitus-associated obesity and vascular dysfunction // Hypertension. – 2012. – Vol.59, N5. – P.1069–1078.
21. Almagro P., Cabrera F.J., Diez J., et al. Comorbidities and short-term prognosis in patients hospitalized for acute exacerbation of COPD. The ESMI study // Chest. – 2012. – Vol.142, N5. – P.1126–1133.
22. Mullerova H., Agusti A., Erqou S., et al. Cardiovascular comorbidity in COPD systematic literature review // Chest. – 2013. – Vol.144. – P.1163–1178.
23. Brassington K., Selemidis S., Bozinovski S., et al. New frontiers in the treatment of comorbid cardiovascular disease in chronic obstructive pulmonary disease // Clin. Sci. (Lond). – 2019. – Vol.133, N7. – P.885–904.
24. Кароли Н.А., Долишняя Г.Р., Ребров А.П. Суточные показатели артериальнои? ригидности у мужчин с различными фенотипами хроническои? обструктивнои? болезни легких в сочетании с артериальнои? гипертензиеи? // Клиницист. – 2015. – №9. – С.37–41.
25. Portegies M.L.P., Lahousse L., Joos G.F., et al. Chronic obstructive pulmonary disease and the risk of stroke. The Rotterdam study // Am. J. Respir. Crit. Care. – 2016. – Vol.193, N3. – P.251–258.
26. Lahousse L., Niemeijer M.N., van Berg M.E., et al. Chronic obstructive pulmonary disease and sudden cardiac death: the Rotterdam study // Eur. Heart J. – 2015. – Vol.36, N27. – P.1754–1761.
27. Драпкина О.М., Ивашкин В.Т. Эпидемиологические особенности неалкогольнои? жировои? болезни печени в России (результаты открытого многоцентрового проспективного исследования наблюдения DIREGL 01903 // Рос. Жур. гастроэнтерологии, гепатологии, колопроктологии. – 2014. – №24. – С.32–38.
28. Стаценко М.Е., Стрельцова А.М., Туровец М.И. Влияние неалкогольнои? жировои? болезни печени на показатели артериальнои? жесткости и риск сердечно-сосудистых осложнении? у пациентов с артериальнои? гипертензиеи? // Архивъ внутреннеи? медицины. – 2020. – №10. – С.296–304.
29. Thomopoulos C., Parati G., Zanchetti A. Effects of blood pressure lowering on outcome incidence in hypertension. 1. Overview, meta-analyses, and meta-regression analyses of randomized trials // J. Hypertens. – 2014. – Vol.32. – P.2285–2295.
30. Williams B., Giuseppe Mancia G., Wilko Spiering W., et al. 2018 ESC/ESH Guidelines for the management of arterial hypertension: The Task Force for the management of arterial hypertension of the European Society of Cardiology (ESC) and the European Society of Hypertension (ESH) // Eur. Heart J. – 2018. – Vol.39, N33. – P.3021–3104.
31. Ettehad D., Emdin C.A., Kiran A., et al. Blood pressure lowering for prevention of cardiovascular disease and death: a systematic review and meta-analysis // Lancet. – 2016. – Vol.387 (10022). – P.957–967.
32. Thomopoulos C., Parati G., Zanchetti A. Effects of blood-pressure-lowering treatment in hypertension: Discontinuations for adverse events attributed to different classes of antihypertensive drugs: meta-analyses of randomized trials // J. Hypertens. – 2016. – Vol.34, N10. – P.1921–1932.
33. Чазова И.Е., Чучалин А.Г., Зыков К.А. и др. Диагностика и лечение пациентов с артериальнои? гипертониеи? и хроническои? обструктивнои? болезнью легких (Рекомендации Российского медицинского общества по артериальной гипертонии и Российского респираторного общества) // Системные гипертензии. – 2013. – №1. – С.5–34.
34. Гуревич М.А., Долгова Е.В., Кузьменко Н.А. Хронические обструктивные заболевания легких, артериальная гипертензия и ишемическая болезнь сердца: особенности патогенеза, клиническои? картины, терапии // РМЖ. – 2016. – №16. – С.1098–1102.
35. Mortensen E.M., Copeland L.A., Pugh M.J., et al. Impact of statins and ACE inhibitors on mortality after COPD exacerbations // Respir. Res. – 2009. – Vol.10. – P.45.
36. Савенков М.П., Иванов С.Н., Иванова С.В. и др. Варианты применения фиксированной комбинации лизиноприла и амлодипина при лечении артериальной гипертонии // РМЖ. – 2010. – №18. – С.106–108.
37. Стаценко М.Е., Деревянченко М.В. Влияние длительнои? антигипертензивнои? терапии на показатели центрального аортального давления и висцерального ожирения у больных артериальнои? гипертензиеи? в сочетании с сахарным диабетом 2-го типа // Рац. фармакотерапия в кардиологии. – 2018. – №14. – С.217–222.
Медицинские новости. – 2020. – №12. – С. 31-36.
Внимание! Статья адресована врачам-специалистам. Перепечатка данной статьи или её фрагментов в Интернете без гиперссылки на первоисточник рассматривается как нарушение авторских прав.