Внимание! Статья адресована врачам-специалистам
Sujayeva V.A.
Republican Scientific and Practical Сenter “Cardiology”, Minsk, Belarus
Some questions of cardiovascular disease prevention taking into account
new Guidelines of European society of Cardiology
Резюме. В 2016 году опубликованы новые Рекомендации Европейского общества кардиологов по сердечно-сосудистой профилактике в клинической практике. В создании данных Рекомендаций приняли участие Европейская Ассоциация по сердечно-сосудистой профилактике и реабилитации, Европейская Ассоциация по сердечно-сосудистой визуализации, Европейская Ассоциация по сердечно-сосудистым чрескожным интервенционным вмешательствам и Европейская Ассоциация по хронической сердечной недостаточности, вследствие чего в настоящих Рекомендациях наиболее полно отражены современные подходы к различным аспектам сердечно-сосудистой профилактики. Подчеркивается не просто важность прекращения курения, соблюдения диеты и рекомендаций по физической активности, но целесообразность перехода к здоровому стилю жизни в целом. Особое внимание уделено дискутабельным вопросам гиполипидемической и антигипертензивной терапии. Таким образом, проблема сердечно-сосудистой профилактики представлена, как комплексная, требующая мультидисциплинарного подхода к ее решению. В статье отдельно рассмотрены вопросы использования некоторых воспроизведенных лекарственных средств (ОАО «Гедеон Рихтер», Венгрия) в проведении сердечно-сосудистой профилактики.
Ключевые слова: сердечно-сосудистые заболевания, сердечно-сосудистая профилактика, факторы риска, дислипидемия, артериальная гипертензия.
Медицинские новости. – 2017. – №2. – С. 39–45.
Summary. New Guidelines of European society of Cardiology on cardiovascular disease prevention in clinical practice were published in 2016. European Association for Cardiovascular prevention and Rehabilitation, European Association of cardiovascular Imaging, European Association of Percutaneous Cardiovascular Interventions , Heart Failure Association took part in creation of these Guidelines, owing to what modern approaches to various aspects of cardiovascular disease prevention are most fully reflected in the present Guidelines. Not only importance of smoking cessation, keeping of a diet and references on physical activity, but also expediency of transition to healthy lifestyle in general is emphasized. Special attention is paid to dyslipidaemia and arterial hypertension which are still objects of scientific discussions. Thus, the problem of cardiovascular prevention is presented how complex, demanding multidisciplinary approach to its decision. In article questions of use of some reproduced medicines of «Gedeon Richter» (Hungary) in performing cardiovascular prevention are separately considered.
Keywords: cardiovascular diseases, cardiovascular prevention, risk factors, dyslipidaemia, arterial hypertension.
Meditsinskie novosti. – 2017. – N2. – P. 39–45.
В Рекомендациях Европейского общества кардиологов (ESC) «2016 European guidelines on cardiovascular prevention in clinical practice» сердечно-сосудистая профилактика определена, как скоординированная совокупность действий, проводимых на популяционном или индивидуальном уровне, целью которых является элиминация или минимизация неблагоприятного влияния сердечно-сосудистых заболеваний (ССЗ) и обусловленной ими нетрудоспособности [25]. Одним из наиболее значимых достижений сердечно-сосудистой профилактики является комплекс мероприя-тий по борьбе с курением, в результате проведения которых на государственном уровне в большинстве европейских стран наметилось снижение смертности от ССЗ: в большинстве европейских стран удельный вес ССЗ не превышает 50% в структуре смертности взрослого населения. Тем не менее не может не обращать на себя внимание диспропорциональный рост в различных европейских регионах распространенности таких факторов риска, как сахарный диабет (СД) и ожирение [25].
В упомянутых Рекомендациях ESC (2016) отмечается, что сердечно-сосу-дистая профилактика должна широко внедряться на популяционном уровне, при этом для пропаганды здорового стиля жизни должны широко использоваться средства массовой информации. Установлено, что в результате широкого внедрения профилактических мероприятий по изменению стиля жизни возможно предотвратить, как минимум, 80% ССЗ и 40% случаев рака [16, 22].
Немаловажным является экономическая эффективность от использования профилактических мероприятий, так как в 2009 году в Евросоюзе расходы, связанные с ССЗ, составили 106 млрд евро, то есть около 9% всех расходов на здравоохранение. Согласно данным Британского института National Institute for Healthcare Excellence (NICE), использование национальных профилактических программ способствует снижению сердечно-сосудистого риска на 1%, что приводит к уменьшению числа случаев ССЗ на 25 000 и сохранению 40 млн евро ежегодно [8].
Над созданием Рекомендаций ESC 2016 года работали несколько профессио-нальных ассоциаций, что подчеркивает необходимость мультидисциплинарного подхода к проведению сердечно-сосудистой профилактики. Важным отличием Рекомендаций 2016 года от предыдущих 2012 года [25] является, с одной стороны, больший акцент на популяционную направленность проводимых профилактических мероприятий, с другой – на необходимость персонифицированного подхода, который заключается в учете индивидуальных особенностей, связанных с женским полом, этнической принадлежностью и молодым возрастом, а также имеющейся патологией у каждого конкретного пациента [25].
Новым направлением сердечно-сосудистой профилактики является следование здоровому образу жизни, что подразумевает целый комплекс долгосрочных мероприятий, начиная от «правильного» питания и заканчивая рациональной физической активностью. Причем важность изменения стиля жизни имеет место не только при проведении вторичной профилактики у лиц, уже имеющих ССЗ, но и при планировании мероприятий первичной профилактики у здоровых лиц. Пропаганда здорового образа жизни на популяционном уровне имеет класс доказанности «IIa» и уровень «В» с позиции медицины, основанной на доказательствах, и должна проводиться на государственном уровне у здоровых и имеющих ССЗ всех возрастов.
Основными модифицируемыми факторами риска на популяционном уровне являются дислипидемия, артериальная гипертензия (АГ) и курение [26]. Уменьшение уровня общего холестерина (ОХ) с помощью статинов [19, 20], улучшение контроля артериального давления (АД), кроме влияния на общий сердечно-сосудистый риск в популяции, имеют также существенный экономический эффект у лиц из группы высокого сердечно-сосудистого риска [24]. Однако по-прежнему проблема состоит в том, что значительная часть пациентов, получающих гиполипидемическую и антигипертензивную терапию, не достигают рекомендованных целевых уровней [7, 10].
Именно на упомянутых аспектах сердечно-сосудистой профилактики – коррекции дислипидемии и лечении АГ – считаем целесообразным остановиться подробнее ниже.
Все современные руководства по профилактике, рекомендуемых объемах и сроках проведения гиполипидемической и антигипертензивной терапии, а также о целевых уровнях ОХ и АД базируются на оценке сердечно-сосудистого риска.
Одним из наиболее широко распространенных подходов в оценке сердечно-сосудистого риска является использование различных шкал, разработанных на основании данных эпидемиологических исследований. Вопрос выбора оптимальной шкалы для оценки сердечно-сосудистого риска являлся предметом дискуссии. Наиболее распространенными являются: Фрамингемская шкала оценки 10-летнего риска развития неблагоприятных сердечно-сосудистых событий, шкалы ASSIGN-SCORE, QRISK 1 и QRISK 2, PROCAM, CUORE, Globorisk [25]. Однако все-таки предпочтение было отдано шкале SCORE (Systemic Coronary Risk Estimation), которая основана на результатах 12 проспективных исследований, проведенных в Европе с 1972 по 1991 год у 117 098 мужчин и 88 080 женщин в возрасте 40–65 лет [9].
Данная шкала позволяет в обычной клинической практике очень быстро, используя лишь уровень АД, ОХ, пол и возраст, оценить 10-летний риск смерти от ССЗ и, что самое важное, в зависимости от риска предложить персонифицированный способ снижения сердечно-сосудистого риска.
В зависимости от эпидемиологической ситуации выделяют страны с низким, высоким и очень высоким риском смерти от ССЗ. Соответственно, предложены две шкалы SCORE: для стран с низким и высоким риском смерти от ССЗ. Шкала SCORE хорошо зарекомендовала себя при скрининговых обследованиях, которые могут проводиться с различной периодичностью как в популяции в целом, так и в отдельных субпопуляциях, например, у лиц с семейной гиперхолестеринемией.
Однако, несмотря на простоту в использовании, шкала SCORE не лишена недостатков. В частности, ее применение в странах с очень высоким риском, к которым относится и Беларусь, может привести к недооценке индивидуального риска у отдельных пациентов (например, у лиц с неблагоприятным наследственным анамнезом ССЗ, пожилых, социально дезадаптированных и т.д.). В то же время индивидуальная переоценка риска может спровоцировать необоснованное назначение медикаментозного лечения.
Таким образом, оценка риска с использованием шкалы SCORE рекомендована у лиц старше 40 лет, которые не имеют других состояний, свидетельствующих о наличии высокого или очень высокого риска, к которым относятся документированные ССЗ, СД, хроническая болезнь почек (ХБП) или очень выражено повышенный уровень хотя бы одного из факторов риска (класс I, уровень С) [11, 25].
Согласно Рекомендациям ESC (2016) выделяют 4 уровня сердечно-сосудистого риска: низкий, умеренный, высокий и очень высокий (табл. 1).
Таблица 1. Категории риска (Joint ESC Guidelines, 2016)
|
Очень
высокий
|
Пациенты, имеющие любое из ниже перечисленных состояний:
Документированные ССЗ или однозначные данные визуализационных методов исследования.
Документированные клинически ССЗ: перенесенный ИМ, ОКС, коронарная реваскуляризация, другая артериальная реваскуляризация, инсульт или ТИА, аневризма аорты, болезни периферических артерий.
Однозначно документированные, по данным визуализационных методов исследования ССЗ: гемодинамически значимые бляшки, по данным КАГ или каротидного УЗИ.
NB! В данную категорию НЕ ВХОДЯТ некоторые инструментальные признаки атеросклероза в состоянии формирования (например, утолщение КИМ, по данным УЗИ БЦА).
СД с поражением органов-мишеней (протеинурия) или при наличии хотя бы одного «большого» фактора риска (курение, выраженная дислипидемия или АГ).
Выраженная ХБП (скорость гломерулярной фильтрации (GFR) <30 мл/мин/1,73м2).
SCORE ≥10%.
|
|
Высокий
|
Пациенты, имеющие:
– очень выраженное повышение хотя бы один фактор риска, особенно ОХ >8 ммоль/л (>310 мг/дл) (например, наследственная гиперхолестеринемия) или АД ≥180/110 мм рт. ст.;
– остальные пациенты с СД (кроме молодых с СД 1-го типа), не имеющие «больших» факторов риска;
– умеренная ХБП (GFR 30–59 мл/мин/1,73м2);
– SCORE ≥5% и <10%.
|
|
Умеренный
|
SCORE ≥1 и <5% на протяжении 10 лет. Большинство пациентов средних лет принадлежат к этой категории.
|
|
Низкий
|
SCORE <1%.
|
Примечание: ИМ – инфаркт миокарда; ОКС – острый коронарный синдром; ТИА – транзиторная ишемическая атака; КАГ – коронароангиография; УЗИ – ультразвуковое исследование.
Однако при использовании шкалы SCORE лица старше 60 лет автоматически попадают в группу очень высокого риска, что может привести к необоснованному назначению медикаментозного лечения, что диктует необходимость оценки у таких пациентов не только общего сердечно-сосудистого риска, но и выраженность отдельных факторов риска и выбора индивидуального подхода в каждом конкретном случае.
При оценке индивидуального риска у каждого пациента необходимо помнить, что у некоторых категорий (например, у лиц с низким социальным статусом, находящихся в социальной изоляции, имеющих неблагоприятный наследственный анамнез ССЗ) может потребоваться ре-классификация риска, вычисленного с помощью шкалы SCORE. Для этого могут быть использованы инструментальные методы исследования: компьютерная томография (КТ) с оценкой коронарного кальциевого индекса (ККИ), оценка плече-лодыжечного индекса и скорости пульсовой волны (СПВ).
Сроки начала и интенсивность мероприятий сердечно-сосудистой профилактики определяются с учетом вычисленногос помощью SCORE риска. В Европе у пациентов низкого риска использование медикаментозной терапии в качестве первичной профилактики считается нецелесообразным, в этом случае рекомендуется следование здоровому стилю жизни. В то же время у пациентов высокого и очень высокого риска наряду с интенсивным изменением стиля жизни показано раннее назначение медикаментозного лечения при лечении АГ и дислипидемии.
Наиболее дискутабельными всегда являлись вопросы лечения дислипидемии: кого лечить и какова цель? Ответы на эти вопросы базируются на данных рандомизированных клинических исследований (РКИ), большинство из которых посвящено изучению статинов. Основные целевые значения модифицируемых факторов риска приведены в табл. 2.
Таблица 2. Целевые значения основных модифицируемых факторов риска (Joint ESC Guidelines 2016)
|
Фактор риска
|
Рекомендация
|
|
Курение
|
Отказ от использования табака в любом виде
|
|
Диета
|
Уменьшение потребления насыщенных жиров, увеличение потребления цельных злаков, овощей, фруктов и рыбы
|
|
Физическая активность
|
Не менее 150 мин/неделю умеренных (3–5,9 МЕТ) аэробных физических нагрузок (30 минут 5 дней в неделю) или 75 минут в день (15 минут 5 дней в неделю) интенсивных (≥6 МЕТ) физических нагрузок или их комбинация
|
|
Масса тела
|
ИМТ 20–25 кг/м2. ОТ <94 см (мужчины) и <80 см (женщины)
|
|
АД
|
<140/90 мм рт. ст.
|
|
СД
|
HbA1C <7% (<53 ммоль/моль)
|
Примечание: ИМТ – индекс массы тела; ОТ – окружность талии; HbA1C – гликированный гемоглобин.
На выявлении и лечении дислипидемии, как ведущего модифицируемого фактора риска, считаем целесообразным остановиться подробнее. Роль повышенного содержания ОХ в развитии атеросклероза была установлена в начале ХХ века русским ученым Н.Н. Аничковым: в 1913 году он предложил теорию возникновения атеросклероза, в основе которой лежал процесс инфильтрации холестерина в стенку сосуда. В 1986 году M. Brown и J. Goldstein описали клеточные рецепторы к липопротеидам низкой плотности (ЛПНП), имеющие чрезвычайно тонкую регуляцию и у человека оптимально работающие при уровне <0,65 ммоль/л. Именно данный факт является ключевым в понимании необходимости достижения достаточно низких целевых значений ЛПНП. Причем, начиная с 1998 и 2003 годов, имеется стойкая тенденция к снижению целевого уровня ЛПНП при лечении дислипидемий. В настоящих Рекомендациях (2016) подчеркивается необходимость подходить к выбору целевого уровня ЛПНП дифференцированно в зависимости от сердечно-сосудистого риска и наличия ассоциированных клинических состояний (табл. 3).
Таблица 3. Целевые уровни при лечении дислипидемии (ESC, 2016)
|
Рекомендация
|
Класс
|
Уровень
|
|
Очень высокий риск: целевой уровень ЛПНП <1,8 ммоль/л
или снижение, как минимум, на 50%, если исходное значение
от 1,8 до 3,5 ммоль/л
|
I
|
В
|
|
Высокий риск: целевой уровень ЛПНП <2,6 ммоль/л
или снижение, как минимум, на 50%, если исходное значение
от 2,6 до 5,2 ммоль/л
|
I
|
В
|
|
Умеренный риск: целевой уровень ЛПНП <3,0 ммоль/л
|
IIa
|
С
|
Результаты многочисленных эпидемио-логических исследований однозначно свидетельствуют о том, что снижение уровня ЛПНП на каждые 1 ммоль/л ассоциируется со снижением смертности от ССЗ и нефатального ИМ на 20–25% [9].
Атерогенная значимость других показателей, характеризующих липидный обмен, и необходимость их медикаментозной коррекции являются предметом дискуссии. В плазме крови липиды, такие как ОХ и триглицериды (ТГ), циркулируют в виде липопртотеидов в ассоциации с различными протеинами (аполипопротеиды). Наиболее атерогенной составляющей ОХ являются ЛПНП. Роль липопротеидов, богатых ТГ, в настоящее время находится в фокусе проводимых исследований. Установлено, что хиломикроны и липопротеиды очень низкой плотности не являются атерогенными, но их высокая концентрация может способствовать развитию острого панкреатита. Остаточные липопротеиды, которые определяются, как разница между ОХ и суммой ЛПНП и липопротеидов высокой плотности (ЛПВП), по данным последних исследований, также могут быть атерогенны. В частности, одним из наиболее хорошо изученных атерогенных липопротеидов не высокой плотности (ЛПнеВП) является аполипротеин В (апоВ) [30]. Благодаря накопленным в настоящий момент данным апоВ придается большое значение, в частности, определение уровня апоВ вместо ЛПНП рекомендовано у лиц с выраженной гипертриглицеридемией (>3,4 ммоль/л), а также уровень апоВ может использоваться в качестве вторичной цели при лечении атерогенных дислипидемий [11].
Гипертриглицеридемия >1,7 ммоль/л также является независимым фактором риска ССЗ, причем риск выше у лиц, имеющих умеренную, а не тяжелую гипертриглицеридемию (>10 ммоль/л). Последняя является независимым фактором риска развития острого панкреатита. Однако данных многоцентровых исследований о целесообразности коррекции изолированной гипертриглицеридемии и целевом уровне ТГ в настоящий момент недостаточно.
В отношении ЛПВП установлено, что их низкий уровень ассоциируется с более высоким сердечно-сосудистым риском. Комбинация низкого содержания ЛПВП и гипертриглицеридемии наиболее часто встречается у лиц, имеющих СД 2-го типа, абдоминальное ожирение и инсулинорезистентность. В общей популяции маркером риска ССЗ рекомендовано считать уровень ЛПВП <1,2 ммоль/л у женщин и <1,0 ммоль/л – у мужчин. Однако в отношении необходимости медикаментозной коррекции содержания ЛПВП убедительных доказательств пока нет. Считается, что физическая активность и воздействие на другие факторы риска (например, курение) являются основными при коррекции уровня ЛПВП.
Однако, несмотря на проведение оптимальной медикаментозной терапии, у части пациентов, включенных в РКИ, не удается достичь целевых уровней холестерина ЛПНП и самое главное – предотвратить развитие сердечно-сосудистых осложнений. В этой связи впервые в Рекомендациях ESC (2016) впервые упомянуто о наличии вторичных целей при лечении дислипидемий:
– у лиц очень высокого риска целевой уровень ЛПнеВП <2,6 ммоль/л;
– в группе высокого риска – <3,3 ммоль/л;
– при умеренном риске – <3,8 ммоль/л.
Данные значения ЛПнеВП рекомендованы в качестве вторичной цели лечения, например, у лиц с выраженной гипертриглицеридемией. У этой категории пациентов в качестве цели можно рассматривать также достижение целевого уровня апоВ: в группе очень высокого риска – <80 мг/дл, в группе высокого риска – <100 мг/дл [25].
Ориентироваться на значение ЛПНП при лечении дислпидемии – основная стратегия, принятая в Европе. Точка зрения Американской коллегии кардиологов/Американской ассоциации сердца (ACC/AHA) по лечению нарушений липидного обмена (ACC/AHA Guideline on the Treatment of Blood Cholesterol to Reduce Atherosclerotic Cardiovascular Risk in Adults) кардинально отличается от Европейской. Первичной целью согласно Рекомендациям АСС/АНА является не уровень ЛПНП, а целевая доза статинов, интенсивность терапии статинами в свою очередь зависит от наличия и степени выраженности ССЗ и сопутствующих заболеваний [28].
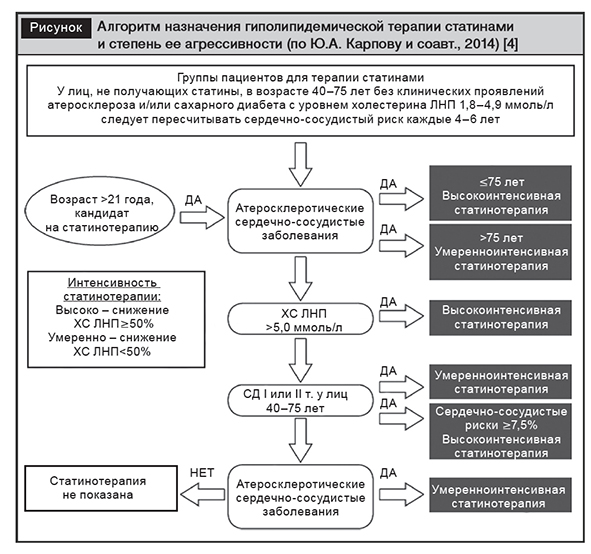
В Рекомендациях АСС/АНА выделено 4 категории пациентов, которым обязательно показано назначение статинов вследствие максимальной пользы и снижения сердечно-сосудистого риска:
1. Лица с сердечно-сосудистыми заболеваниями атеросклеротического генеза (ишемическая болезнь сердца, ишемический инсульт, заболевания периферических артерий).
2. Лица, имеющие первичное повышение уровня ЛПНП ≥190 мг/дл (≥5 ммоль/л).
3. Пациенты с СД в возрасте 40–75 лет, имеющие уровень ЛПНП 70–189 мг/дл (1,8–4,9 ммоль/л).
4. Лица без клинических проявлений атеросклероза и/или без СД, имеющие уровень ЛПНП 70–189 мг/дл (1,8–4,9 ммоль/л) в возрасте 40–75 лет и имеющие сердечно-сосудистый риск ≥7,5% в течение ближайших 10 лет.
Следует отметить, что перечисленные категории пациентов охватывают как вторичную, так и первичную сердечно-сосудистую профилактику, что отличает Рекомендации АСС/АНА от Рекомендаций ESC (2016).
Еще одним кардинальным отличием Рекомендаций АСС/АНА от Рекомендаций ESC (2016) является цель лечения дислипидемии – достижение целевой дозы статинов (тем выше, чем более выражены имеющиеся ССЗ), а не целевого уровня ЛПНП (тем ниже, чем более выражены имеющиеся ССЗ и сопутствующие заболевания). В зависимости от степени выраженности дислипидемии и наличия сопутствующих заболеваний АСС/АНА (2013) предложено 3 варианта интенсивности проводимой статинотерапии [28]:
1) высокоинтенсивная;
2) умеренноинтенсивная;
3) низкоинтенсивная.
Алгоритм назначения терапии статинами, рекомендованный АСС/АНА в 2013 году, представлен на рисунке.
В табл. 4 представлены статины и их дозы, используемые для статинотерапии различной интенсивности.
Таким образом, эксперты АСС/АНА в лечении пациентов высокого риска отдают предпочтение статинам с наиболее выраженным гиполипидемическим действием – розувастатину и аторвастатину. Розувастатин является синтетическим лекарственным средством и обладает наиболее выраженным воздействием как на уровень ЛПНП, так и на другие показатели липидного обмена в сравнении с иными лекарственными средствами своего класса.
Таблица 4. Интенсивность терапии статинами (АСС/АНА, 2013) [28]
|
Высокоинтенсивная
терапия
|
Умеренноинтенсивная терапия
|
Низкоинтенсивная
терапия
|
|
Снижение ХС ЛПНП ≥50%
|
Снижение ЛПНП от 30 до 50%
|
Снижение ЛПНП <30%
|
|
Аторвастатин 40–80 мг
|
Аторвастатин 10–20 мг
|
Симвастатин 10 мг
|
|
Розувастатин 20–40 мг
|
Розувастатин 5–10 мг
|
Правастатин 10–20 мг
|
|
|
Симвастатин 20–40 мг
|
Ловастатин 20 мг
|
|
|
Правастатин 40–80 мг
|
Флувастатин 20–40 мг
|
|
|
Ловастатин 40 мг
|
Питавастатин 1 мг
|
|
|
Флувастатин XL 80 мг
|
|
По данным исследования STELLAR, прием розувастатина в дозе 10 мг способствовал снижению уровня ЛПНП на 46%, а в дозировке 20 мг – на 52% от исходного уровня, что в полной мере отвечает требованиям Рекомендаций АСС/АНА (2013) к высокоинтенсивной статинотерапии [12].
В рандомизированном открытом 12-недельном исследовании DISCOVERY проведен сравнительный анализ эффективности розувастатина в дозе 10 мг и аторвастатина в дозе 10 мг на уровень ЛПНП, ОХ и ЛПВП, а также на возможность достижения целевого уровня ЛПНП (в начале исследования – согласно Рекомендациям 1998 года <3,0 ммоль/л, во второй части исследования – согласно Рекомендациям 2003 года <2,5 ммоль/л). В сравнении с аторвастатином розувастатин способствовал достоверно более выраженному снижению уровня ЛПНП и ОХ (р<0,05), а также более существенному увеличению содержания ЛПВП (p<0,05). Целевого (согласно Рекомендациям 1998 года) уровня ЛПНП достигли 83,4% пациентов в группе розувастатина и лишь 68,3% – аторвастатина (р<0,001) [29].
Сравнительная эффективность различных статинов по их влиянию на показатели липидного спектра крови проанализирована по данным метаанализа VOYAGER (indiVidual patient data-meta-analysis оf statin therapy in at risk Groups: Effects of Rosuvastatin, atorvastatin, and simvastatin) [13]. В метаанализ вошли данные 37 РКИ, включавшие 32 258 пациентов. В сравнении с аторвастатином и симвастатином розувастатин продемонстрировал себя, как наиболее эффективный не только по влиянию на уровень ЛПНП, но и на ЛПВП. Кроме того, в группе розувастатина выявлено наибольшее число пациентов, которые достигли целевого уровня ЛПНП <1,8 ммоль/л в группе очень высокого риска и <2,5 ммоль/л – высокого риска [13].
Кроме того, S.J. Nichholsи соавт. (2010) при проведении многофакторного анализа данных, полученных в исследовании VOYAGER, установили, что статины оказывали дозозависимое влияние не только на уровень ЛПНП, но и на содержание ТГ, ЛПнеВП и атерогенных апоВ. Двойное увеличение дозы статинов приводило к снижению суммарного содержания всех атерогенных ЛПнеВП на 4–7%. Увеличение дозы статинов являлось сильным предиктором достижения целевого уровня ЛПНП у пациентов высокого риска. Лучше целевого уровня ЛПНП достигали лица женского пола, пациенты с СД и имевшие диагностированные атеросклеротические изменения. В то же время нормализация содержания ТГ чаще наблюдалась у лиц мужского пола и у пациентов, не имевших СД. Авторы пришли к выводу, что более частое достижение целевых уровней атерогенных липопротеидов с помощью повышения дозы статинов является обоснованием для высокодозовой статинотерапии с целью повышения эффективности сердечно-сосудистой профилактики [23].
Учитывая полученные данные об эффективности высокодозоввой статино-терапии, в Европейских Рекомендациях по лечению стабильной болезни коронарных артерий (2013) для улучшения прогноза предпочтительными названы статины с наиболее выраженным липидснижающим действием – розувастатин и аторвастатин [24].
Сравнительная эффективность различных статинов анализировалась в рамках масштабной программы GALAXY. Программа GALAXY представляет собой совокупность клинических исследований, посвященных изучению эффективности и переносимости розувастатина в сравнении с другими лекарственными средствами из этой группы [27].
В основе программы GALAXY лежит гипотеза, что статины наиболее эффективны для уменьшения атерогенности липидного спектра крови, благотворно влияют на маркеры воспаления, что в совокупности способствует замедлению прогрессирования атеросклероза и уменьшению частоты развития сердечно-сосудистых осложнений [27].
Выполненные исследования показывают, что розувастатин является более эффективным, чем все остальные статины для снижения уровня ЛПНП, улучшения липидного профиля, позволяет пациентам достичь целевых значений при лечении дислипидемии (в том числе пересмотренных, более жестких целевых значений) даже у пациентов высокого риска.
Исследования, проведенные в рамках программы GALAXY, также продемонстрировали, что розувастатин может способствовать замедлению и даже регрессу атеросклеротического процесса, что в конечном итоге способствует снижению заболеваемости и смертности от ССЗ, то есть может использоваться для полноценной сердечно-сосудистой профилактики [27].
Однако программа GALAXY выполнялась с использованием оригинального препарата. В этой связи весьма актуальным является вопрос о том, обладают ли воспроизведенные (генерические) лекарственные средства выявленными в программе GALAXY эффектами.
Одним из воспроизведенных препаратов розувастатина является Мертенил (ОАО «Гедеон Рихтер», Венгрия). Мертенил имеет свою доказательную базу, свидетельствующую не только о его доказанном гиполипидемическом действии, но и о терапевтической эквивалентности.
О сопоставимой гиполипидемической эквивалентности Мертенила оригинальному лекарственному средству «Крестор» свидетельствуют результаты исследования, проведенного в Беларуси А.М. Пристром и соавт. (2012). Прием Мертенила и Крестора в дозе 10 мг в течение 12 недель обусловливал снижение содержания ЛПНП у 46,7 и 42,6% пациентов соответственно (р>0,05). Целевого уровня ЛПНП достигли 82% принимавших Мертенил и 71% – Крестор (р>0,05). Признаков непереносимости, как и потребовавших отмены лечения побочных эффектов, не зарегистрировано в обеих группах [5].
В Российском исследовании СТРЕЛА (Влияние розувастатина на показатели микроциркуляции и функцию эндотелия сосудов у пациентов с АГ высокого риска и дислипидемией в сравнении с аторвастатином) оценивалось влияние Мертенила в сравнении с аторвастином на показатели микроциркуляции и сосудистая жесткость у пациентов с АГ высокого риска (SCORE ≥5%). Из 82 включенных в исследование 39 получали аторвастатин в суточной дозе 10–20 мг, 43 – Мертенил в дозе 5–10 мг. Пациентам проводили оценку функции эндотелия сосудов, а также анализ жесткости сосудистой стенки. Установлено, что на фоне приема статинов отмечается улучшение эндотелиальной функции у пациентов с АГ, дислипидемией и высоким риском. Статины способствовали снижению показателей жесткости сосудистой стенки и центрального пульсового АД. Более выраженные позитивные изменения как липидного спектра крови, так и функционального состояния сосудистой стенки наблюдались в группе Мертенила [1].
В Венгерское исследование TIGER, посвященное изучению эффективности воспроизведенного розувастатина (ОАО «Гедеон Рихтер», Венгрия), включены 2564 пациента: 1102 мужчины, (средний возраст – 56,4 года), 1462 женщины (средний возраст – 57,8 года). Включенные в исследование имели метаболический синдром (МС) или СД 2-го типа. Исходно 68,8% пациентов принимали 10 мг розувастатина, к 3-му месяцу их стало 59,9%, 6-му – 56,5%. При включении в исследование розувастатин в дозе 20 мг принимали 29,2% больных, к 3-му месяцу – 36,1%, 6-му – 38,9%. Высокодозовый режим (40 мг в сутки) исходно был выбран у 1,9% пациентов, к 3-му месяцу – у 3,8%, 6-му – у 4,4% включенных в исследование. Увеличение дозы розувастатина осуществлялось лечащими врачами с целью достижения целевого уровня ОХ и ЛПНП. Через 3 и 6 месяцев наблюдалось достоверное снижение ОХ, ЛПНП и ТГ в сравнении с исходным (р<0,001). Содержание ЛПВП, напротив, достоверно повышалось уже через 3 месяца, а результат сохранялся и через 6 месяцев (р<0,001). Причем к концу 6-го месяца у 52,2% пациентов был достигнут целевой уровень ОХ (≤4,5 ммоль/л), у 54,3% целевой уровень ЛПНП – <2,5 ммоль/л. Дополнительно у 53,3% лиц отмечалась нормализация содержания ТГ <1,7 ммоль/л. Обращает на себя внимание также, что через 6 месяцев произошло снижение содержания высокочувствительного С-реактивного белка (СРБ), который является общепринятым маркером системного воспаления и неблагоприятного прогноза при ССЗ, от 3,76±1,95 до 2,2±1,09 мг/л (р<0,001) [14].
Важным является доказанное положительное влияние Мертенила на функциональное состояние системы кровообращения у пациентов с острым коронарным синдромом (ОКС) [2]. Выраженное гиполипидемическое действие Мертенила заключалось в снижении уровня ЛПНП на 59% в сравнении с исходным через 30 дней после начала лечения. Нелипидные эффекты Мертенила были представлены антиаритмическим действием, а также благотворным влиянием на процессы ремоделирования миокарда [2].
Возможность использования высокоинтенсивного режима приема Мертенила (в дозе 40 мг) была установлена в исследовании «40?40». В исследование включались пациенты очень высокого риска, которые не могли достичь целевого уровня ЛПНП на фоне приема аторвастатина (18 пациентов), симвастатина (10 пациентов), розувастатина в меньшей дозе (12 пациентов). При переводе пациентов на высокодозовый режим приема Мертенила было достигнуто дополнительное снижение уровня ЛПНП на 22,4%, что способствовало существенному увеличению числа лиц, достигших целевого уровня при лечении дислипидемии [3].
Болезнь коронарных артерий трансплантированного сердца (БАТС) является специфическим осложнением, способствующим существенному снижению эффективности оперативного вмешательства вследствие развития «немых» инфарктов миокарда, жизнеугрожающих аритмий, внезапной смерти, что в совокупности снижает выживаемость после трансплантации сердца (ТС) и ухудшает отдаленные медицинские и социально-экономические результаты проведенного вмешательства. В этой связи поиск способов, оказывающих влияние на развитие и прогрессирование БАТС, является одним из актуальнейших вопросов современной трансплантологии. Патофизиологическим обоснованием эффективности статинов в развитии БАТС являются как их прямое антиатерогенное действие, так и плейотропные (нелипидные) эффекты (противовоспалительный, иммуномодулирующий, антитромботический, антиаритмический и др.). Однако некоторые статины оказывают влияние на цитохромР450(CYP450 ЗА4)-зависимые ферментные системы, вследствие чего может изменяться концентрация иммуносупрессивных препаратов (в первую очередь циклоспорина), что до какой-то степени ограничивало использование статинов после ТС.
В исследовании О.П. Шевченко и соавт. (2013) изучены нелипидные эффекты Мертенила у пациентов после ТС, оцениваемые по динамике уровней СРБ и биомаркеров риска развития васкулопатии трансплантата. Мертенил в суточной дозе 10 мг/сутки получали 15 реципиентов, начиная с 3–4-й недели после ТС. Было показано, что у реципиентов в посттрансплантационном периоде помимо гиполипидемического действия Мертенил обладал противовоспалительным эффектом, диагностируемым по снижение уровня СРБ. Его прием также способствовал снижению уровня биомаркеров риска васкулопатии сердечного трансплантата (РАРР-А и sCD4ОL) [6].
Еще одним распространенным модифицируемым фактором риска ССЗ является АГ, причем в подавляющем большинстве случаев имеет место сочетание дислипидемии и АГ. Известно, что только около 1/3 пациентов с АГ могут достичь целевого уровня АД при монотерапии, в большинстве случаев требуется назначение комбинированной терапии. В то же время увеличение числа принимаемых лекарственных средств снижает приверженность к лечению [13, 17]. Пациенты с АГ, вынужденные принимать несколько препаратов, зачастую отказываются от статинов, так как они не влияют на уровень АД и качество жизни. В этой связи весьма перспективным направлением сердечно-сосудистой профилактики является разработка способов комплексного воздействия на оба фактора риска, в том числе с использованием фиксированных комбинаций лекарственных средств, обладающих как антигипертензивным, так и гиполипидемическим действием.
Весьма интересными представляются результаты 6-месячного проспективного наблюдательного неинтервенционного Вегерского исследования ROSALIA, посвященного оценке эффективности фиксированной комбинации лизиноприл/амлодипин (Экватор, ОАО «Гедеон Рихтер», Венгрия) в качестве комплексной антигипертензивной терапии и свободной комбинации розувастатина в качестве гиполипидемической терапии (Мертенил, ОАО «Гедеон Рихтер», Венгрия) [15]. В исследование включены пациенты с АГ I и II степени и гиперхолестеринемией, относящиеся к категории высокого и очень высокого сердечно-сосудистого риска. В исследование вошли 2452 пациента в возрасте 63,2±11,4 года, комбинированная терапия Экватором (лизиноприл/амлодипин) начиналась с доз 10/5, 20/5 или 20/10 мг/сутки, Мертенил назначался в дозе 10–20 мг с последующей титрацией, вплоть до достижения целевого уровня АД (<140/90 мм рт. ст. у лиц без СД и <140/85 мм рт. ст. – с СД) и ЛПНП (<3,0 ммоль/л у пациентов без ССЗ, <2,5 ммоль/л – у лиц высокого риска и <1,8 ммоль/л – в группе очень высокого риска). Установлено, что через 6 месяцев приема Экватора 91% пациентов достигли целевого уровня АД. Мертенил способствовал достижению целевого уровня ЛПНП <3,0 ммоль/л в 67% случаев, <2,5 ммоль/л – в 49% и <1,8 ммоль/л – в 40% случаев. Снижение АД и ЛПНП было одинаково выраженным как у лиц с СД 2-го типа, так и у лиц с ненарушенным углеводным обменом. Весьма важным является также то, что Экватор и Мертенил обладали одинаковой эффективностью как у ранее леченных пациентов, так и у впервые начавших лечение. Дополнительным положительным эффектом являлось воздействие на другие факторы риска – уровень СРБ и мочевой кислоты, глюкоза в крови и микроальбуминурия, что в совокупности с достижением целевых значений при лечении АГ и дислипидемии дает право говорить о положительном влиянии на прогноз и поражение органов-мишеней.
Таким образом, комплексная сердечно-сосудистая профилактика, включающая мероприятия по изменению образа жизни (отказ от курения, диета, борьба с лишним весом, рациональная физическая активность) и оптимальную медикаментозную терапию (АГ, дислипидемия, СД) является мощным оружием в борьбе с ССЗ. Широкая популяризация сердечно-сосудистой профилактики, информирование населения о пользе некоторых ее мероприятий в доступной популярной форме может способствовать закреплению достигнутых успехов в борьбе с данным видом «болезней цивилизации».
Л И Т Е Р А Т У Р А
1. Драпкина О.М., Корнеева О.Н., Палаткина Л.О., Балахонова Н.П., Ивашкин В.Т. // Леч. врач. – 2013. – №3. – С.1–4.
2. Задионченко В.С., Шехян Г.Г., Шахрай Н.Б. // Consilium Medicum. – 2011. – №5. – С.85–89.
3. Зубарева М.Ю., Рожкова Т.А., Амелюшкина В.А., Сусеков А.В., Кухарчук В.В. // Фарматека. – 2013. – №7. – С.63–68.
4. Карпов Ю.А., Сергиенко И.В., Ежов М.В. // Атеросклероз и дислипидемии. – 2014. – №1. – С.59–61.
5. Пристром А.М., Самоходкина С.В., Крейтер М.Л., Гуменюк А.Г. // Мед. новости. – 2013. – №3. – С.51–56.
6. Шевченко О., Халилулин Т., Шевченко А. и др. // Врач. – 2013. – №5. – С.76–79.
7. Banegas J.R., Lopez-Garcia E., Dallongeville J., et al. // Eur. Heart J. – 2011. – Vol.32. – P.2143–2152.
8. Collins M., Mason H., O’Flaherty M., et al. // Value Health. – 2014. – N17. – P.517–524.
9. Conroy R.M., Pyorala K., Fitzgerald A.P., et al. // Eur. Heart J. – 2003. – N24. – P.987–1003.
10. De Smedt D., Kotseva K., De Bacquer D., et al. // Eur. Heart J. – 2012. – Vol.33. – P.2865–2872.
11. Di Angelantonio E., Sarwar N., Perry P., et al. // JAMA. – 2009. – Vol.302. – P.199–200.
12. Jones P.H., Hunninghake D.B., Ferdinand K.C., et al. // Clin Ther. – 2004. – Vol.26, N9. – P.1388–1399.
13.Karlson B.W., Barter P.J., Palmer M.K.,Lundman P., Nicholls S.J. // Nutr. Metab. Cardiovasc. Dis. – 2012. – Vol.22, N9. – P.697–703.
14. Kekes E., Csaszar А. // Cardiol. Hungarica. – 2012. – Vol.42, N2. – P.61–67.
15. Kуnyi A., Sarszegi Z., Hild G., Balazs G. // J. Comp. Eff. Res. – 2016.
16. Liu K., Daviglus M.L., Loria C.M., et al. // Circulation. – 2012. – Vol.125. – P.996–1004.
17. Mancia G., De Backer G., Dominiczak A., et al. // Eur. Heart J. – 2007. – Vol.28, N12. – P.1462–1536.
18. Mancia G., Fagard R., Narkiewicz K., et al. // Eur. Heart J. – 2013. – Vol.34, N28. – P.2159–2219.
19. Mc Connachie A., Walker A., Robertson M., et al. // Eur. Heart J. – 2014. – Vol.35. – P.290–298.
20. Mistry H., Morris S., Dyer M., et al. / BMJ Open. – 2012; 2:e001029.
21. Montalescot G., Sechtem U., Achenbach S., et al. // Eur. Heart J. – 2013. – Vol.34 (38). – P.2949–3003.
22. NICE Public Health Guidance 25. Prevention of Cardiovascular Disease. http://www.nice.org.uk/guidance/PH25.National Institutes of Health NH, Lung, and Blood Institute. Morbidity & Mortality: 2012 Chart Book on Cardiovascular, Lung, and Blood Diseases. Bethesda, MD: National Heart, Lung, and Blood Institute; 2012.
23. Nicholls S.J., Brandrup-Wognsen G., Palmer M., Barter P.J. // Am. J. Cardiol. – 2010. – Vol.105, N1. – P.69–76.
24. Pereira M., Azevedo A., Lunet N., et al. // Circ. Cardiovasc. Qual. Outcomes. – 2013. – N6. – P.634–642.
25. Perk J., Guy De Backer, Gohlke H., et al. // Eur. Heart J. – 2012. – Vol.33. – P.1635–1701.
26. Roth G.A., Forouzanfar M.H., Moran A.E., et al. // N. Engl. J. Med. – 2015. – Vol.372. – P.1333–1341.
27. Schuster H. // Expert Rev. Cardiovasc. Ther. – 2007. – Vol.5, N2. – P.177–193.
28. Stone N.J., Robinson J., Lichtenstein A.H. // JAMA. – 2013. Nov 7.pii: S 0735-1097 (13)06028-2.
29. Strandberg T.E., Feely J., Sigurdsson E.L. // Clin. Ther. – 2004. – Vol.26, N11. – P.1821–1833.
30. Thompson A., Danesh J. // J. Intern. Med. – 2006. – Vol. 259. – P.481–492.
Медицинские новости. – 2017. – №2. – С. 39-45.
Внимание! Статья адресована врачам-специалистам. Перепечатка данной статьи или её фрагментов в Интернете без гиперссылки на первоисточник рассматривается как нарушение авторских прав.