Внимание! Статья адресована врачам-специалистам
Zaharenko A.1, Kravchenko H.2
1Belarusian Medical Academy of Post-Graduate Education, Minsk
2State Еnterprise «Aсadempharm», Minsk, Belarus
Therapeutic potential of ademetionine (“HeptalNAN”, “Aсadempharm”)
in the treatment of liver disease with intrahepatic cholestasis
Резюме. Данные медицинской статистики указывают на «омоложение» популяции с заболеваниями печени, в том числе на многократное увеличение за последнее десятилетие частоты случаев цирроза печени в возрастной группе 35–55 лет. Адеметионин оказывает выраженный клинический эффект при лечении заболеваний печени с внутрипеченочным холестазом. Белорусское импортозамещающее лекарственное средство «ГепталНАН» (производства «Академфарм») является современным высокотехнологичным генериком адеметионина.
Ключевые слова: хронические заболевания печени, внутрипеченочный холестаз, адеметионин, «ГепталНАН».
Медицинские новости. – 2016. – №11. – С. 28–32.
Summary. Health statistics indicate a “rejuvenation” of the population with liver disease, including multiple increases over the last decade, the incidence of liver cirrhosis in the age group 35–55 years. Ademetionine has a pronounced clinical effect in the treatment of liver disease with intrahepatic cholestasis. Belarusian import-substituting drug “HeptalNAN” (produced by «Aсadempharm») is a modern high-tech generic form of ademetionine.
Keywords: chronic liver disease, intrahepatic cholestasis, ademetionine, “HeptalNAN”.
Meditsinskie novosti. – 2016. – N11. – Р. 28–32.
Данные медицинской статистики указывают на неблагоприятные тенденции, связанные с патологией печени: «омоложение» заболеваний данной локализации, в том числе увеличение в 5 раз за последние 10 лет частоты случаев цирроза печени в возрастной группе 35–55 лет. Такие пациенты умирают молодыми: если средний возраст умерших в результате инфаркта или инсульта составляет 84 года, то умерших вследствие заболеваний печени?–?59 лет [9]. Большинство заболеваний печени сопровождается гибелью гепатоцитов, что обусловлено повреждением клеточных мембран, нарушением оттока желчи из них, влиянием свободных радикалов. Важную роль в обеспечении нормальной жизнедеятельности гепатоцитов играет адеметионин, способствующий регенерации гепатоцитов, уменьшению фиброзирования, транспорту жирных кислот и оттоку желчи из гепатоцитов [9].
Применение адеметионина (в частности, лекарственного средства «ГепталНАН» производства Государственного предприятия «Академфарм», Республика Беларусь) регламентировано Клиническим протоколом «Диагностика и лечение пациентов с заболеваниями органов пищеварения» (утвержден Постановлением Министерства здравоохранения Республики Беларусь от 21 июля 2016 г. №90).
Фармакологическое действие адеметионина
Адеметионин (S-аденозил-L-метионин, SAMe, S-адеметионин) – природное вещество, синтезирующееся в печени. Для адеметионина характерна «многовекторность» действия (плейотропные эффекты). Адеметионин – физиологический субстрат многих биологических реакций, эндогенно синтезируемый из метионина и аденозина. По мнению некоторых авторов, адеметио-нин уступает в разнообразии реакций только аденозинтрифосфату (АТФ): играет ключевую роль в трансметилировании, транссульфировании, синтезе полиаминов [10, 14].
Реакции аденозинзависимого трансметилирования. Адеметионин участвует в синтезе фосфолипидов (ФЛ) – основных строительных компонентов клеточной мембраны, которые вместе с холестерином обеспечивают ее текучесть (чем больше ФЛ, тем выше текучесть). Помимо этого, аденозинзависимое метилирование ФЛ усиливает поляризацию, вызывая непрерывный переход с внутреннего слоя мембраны на внешний, что повышает ее текучесть [10]. Нарушение метилирования ФЛ ведет к уменьшению активности Na+/K+-АТФ-азного насоса, изменению электрохимического потенциала мембраны и нарушению транспорта желчных кислот [10].
Реакции транссульфурирования – второй тип метаболических реакций, в которых принимает непосредственное участие адеметионин [10]. Нарушение транссульфированияприводит к дефициту глутатиона – важнейшего клеточного антиоксиданта [7]. Недостаток глутатиона характерен практически для всех хронических заболеваний печени, снижение его содержания ведет к уменьшению устойчивости гепатоцитов к повреждающему действию свободных радикалов [7], а также к снижению защиты гепатоцитов от эндогенных и экзогенных токсических веществ [10].
Другой метаболит адеметионина – таурин – тоже задействован в детоксицирующей функции печени. Таурин вовлечен в процесс конъюгации желчных кислот [10]. Поскольку конъюгация желчных кислот с таурином увеличивает их растворимость, низкий уровень таурина приводит к накоплению токсических желчных кислот в гепатоците [7]. На обмен таурина отрицательное влияние оказывает не только нерациональное питание, но и интоксикация, особенно алкогольная. В условиях злоупотребления алкоголем резко снижена способность организма усваивать таурин, поэтому больным с алкогольной кардиомиопатией, по мнению некоторых зарубежных авторов, показан прием адеметионина [7]. Таурин играет важную роль в обмене калия и удерживает его внутри клетки, препятствуя нарушению сердечного ритма, уменьшает отеки, в том числе сердечные. Он участвует в кальциевом и магниевом обмене. С этой точки зрения, по мнению зарубежных авторов, применение адеметионина может быть полезно у лиц с алкогольной интоксикацией, атеросклерозом, сердечно-сосудистой недостаточностью, гипертонической болезнью [7].
Имеются данные о том, что глутатион, таурин обладают защитным действием в отношении пруритогенов, то есть биологических субстанций, ответственных за появление кожного зуда [7].
Аминопропилирование – биохимическая реакция, при которой аминопропильная группа переносится с адеметионина на такие полиамины, как путресцин, спермидин и спермин. Эти полиамины играют важную роль в структуре рибосом, а путресцин кроме того стимулирует пролиферацию гепатоцитов после частичной гепатоэктомии; полагают, что стимуляция пролиферации гепатоцитов осуществляется вследствие того, что путресцин выступает в роли комитогена эпидермального фактора роста [7].
Экспериментально показаны: а) способность адеметионина при его добавлении к монослою нормальных фибробластов эпидермиса человека значительно уменьшать образование коллагена, не влияя на пролиферацию и жизнеспособность клеток; б) потенциальная антифиброзная активностьадеметионина [7]. Поскольку холестаз сам по себе может индуцировать фиброз печени, оба эффекта адеметионина (антихолестатический и антифибротический) могут проявлять синергизм в улучшении состояния печени [7].
Доказаны также холеретическое (благодаря улучшению внутриклеточного транспорта компонентов желчи) и холекинетическое (благодаря нормализации моторики желчевыводящих путей) свойства адеметионина [7]. Кроме того, адеметионин характеризуется наличием выраженного мембраностабилизирующего, антиоксидантного, антидепрессивного эффекта[1].
Вышеописанные свойства адеметионина позволяют отнести его к средствам, воздействующим на основные звенья патогенеза внутрипеченочного холестаза.
Холестаз – тяжелый, плохо поддающийся лечению синдром, характеризующийся уменьшением тока желчи и ее поступления в двенадцатиперстную кишку. Известно, что гепатоцеллюлярный и каналикулярный холестаз может быть обусловлен вирусными, алкогольными, лекарственными, токсическими поражениями печени, застойной сердечной недостаточностью, метаболическими нарушениями (доброкачественный возвратный внутрипеченочный холестаз, холестаз беременных, муковисцидоз, ?1-антитрипсиновая недостаточность и др.). Эти процессы приводят к снижению активности S-аденозилметилсинтетазы и, соответственно, к нарушению продукции адеметионина [7].
Снижение синтеза адеметионина связывают с нижеперечисленными негативными последствиями:
1) нарушение биохимических процессов в гепатоците [6];
2) снижение содержания фосфолипидов в гепатоцеллюлярных мембранах, уменьшение активности Na+-K+-АТФазы и других белков-переносчиков. Это, в свою очередь, ведет к нарушению текучести мембран, а также к процессам захвата и выведения компонентов желчи [6];
3) уменьшаются клеточные запасы тиолов и сульфатов (глутатиона, таурина и др.), которые являются главными детоксикационными субстанциями, а также обладают выраженным антиоксидантным эффектом. Их дефицит в конечном итоге обусловливает цитолиз гепатоцитов при холестазах любого генеза [6].
Проблема заместительной терапии в гастроэнтерологической практике включает в себя не только лечение экзокринной недостаточности поджелудочной железы (с использованием ферментных препаратов). В последние годы акцентируется актуальность заместительной терапии и в лечении заболеваний печени [9]. Применение лекарственных средств (ЛС)на основе адеметионина (в том числе «ГепталНАН») можно считать по сути заместительной терапией дефицита адеметионина [9].
Дефицит адеметионина не может быть компенсирован просто путем дополнительного приема метионина с пищей [14]: в экспериментальном исследовании J.D. Finkelstein, J.J. Martin (1986) показано, что даже семикратное повышение содержания метионина в рационе не оказывает существенного влияния на содержание внутрипеченочного адеметионина [14]. Увеличение количества метионина в рационе в ряде случаев может даже стать причиной интоксикации. Так, в ряде исследований у пациентов с заболеваниями печени выявляли повышенную концентрацию циркулирующего в крови метионина и обусловленные ею токсические эффекты, в том числе в виде снижения содержания печеночного АТФ [14]. В случае патологии печени, сопряженной с ферментативной недостаточностью, целесообразно обеспечить организм готовым продуктом дефектной реакции, то есть адеметионином, который играет ключевую роль в нормальном функционировании клетки [14]. Таким образом, адеметионин, поступающий в виде ЛС, выступает в роли эссенциального нутриента [14].
Клиническая эффективность адеметионина
M.P. Virukalpattigopalratnam, T. Singh, A.C. Ravishankar (2013) было проведено обсервационное исследование (250 пациентов на 23 клинических базах в Индии), направленное на оценку эффективности и переносимости адеметионина у пациентов с внутрипеченочным холестазом (ВПХ) на фоне хронической неалкогольной болезни печени. Оценку медико-экономических показателей, биохимических процессов в печени, динамики признаков и симптомов ВПХ (усталость, желтуха и зуд) проводили в два посещения, то есть в начале исследования и после 6 недель применения адеметионина [23]. В заключительный анализ были включены 244 пациента (средний возраст – 43,75±11,14 года, 75,5% (184/244) пациентов – мужского пола, 30,7% (75/244) – страдали циррозом печени). Сопутствующую терапию получали 44,4% (108/243) пациентов [23]. Терапия адеметионином способствовала статистически значимому снижению (Р<0,0001) числа дней временной нетрудоспособности у пациентов и существенному снижению количества визитов к врачу (Р<0,0001), уменьшению уровня биохимических маркеров, а также признаков и симптомов ВПХ. Адеметионин характеризовался хорошей эффективностью и переносимостью у большинства пациентов [23]. В другом обсервационном исследовании показана хорошая эффективность и безопасность адеметионина у больных ВПХ (250 лиц, 21 клиническая база) на фоне хронической алкогольной болезни печени [17].
Мета-анализ/систематический обзор AHRQ (адеметионин) – доказательный отчет, подготовленный Агентством по оценке исследований в области здравоохранения и изучению качества медицинского обслуживания (Agency for Healthcare Research and Quality/AHRQ) Департамента здраво-охранения и социальных служб США: 99 публикаций, 102 рандомизированных контролируемых клинических испытания (РКИ) адеметионина, из которых 41 – при различной патологии печени (9 – при холестазе у беременных, 12 – при холестазе вследствие другой патологии печени, 7 – при циррозе печени, 8 – при гепатите, 4 – при других хронических болезнях печени, 1 – при трансплантации печени) [14]. В результате мета-анализа установлено, что по сравнению с плацебо применение адеметионина при холестазе у беременных, а также у лиц с ВПХ, обусловленным хроническими заболеваниями печени, ассоциировано со значительным уменьшением выраженности кожного зуда и со значительным снижением повышенного уровня билирубина в сыворотке крови [14].
Мета-анализ/систематический обзор (2015). Известно, что применение адеметионина способствует восстановлению запасов печеночного глутатиона и предотвращает нарушения функции печени. Проанализированы базы данных PubMed, CochraneDatabase и EMBASE за последние 20 лет и отобраны релевантные РКИ адеметионина при хронических заболеваниях печени [18]. 12 РКИ, в которые были включены 705 пациентов, были использованы в систематическом обзоре и мета-анализе [18].
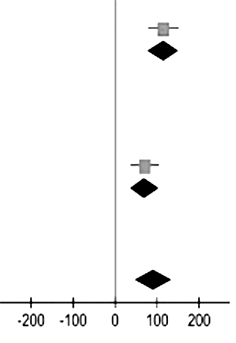
Адеметионин снижал уровень общего билирубина (ОБ) и уровни аспартатамино-трансферазы (АСТ), но не улучшал показатели аланинаминотрансферазы (АЛТ) у пациентов с хроническими заболеваниями печени (ХБП) [18]. Авторами проанализированы данные 8 независимых сравнений уровня ОБ (359 пациентов). В двух сравнениях между адеметионином и группой плацебо были статистически значимые различия (табл. 1, 2) [18]. Снижение уровня АСТ на фоне терапии адеметионином выявлено при мета-анализе с использованием 4 независимых сравнений (177 пациентов). Различия были статистически значимыми (P=0,0003) (табл. 3) [18].
Тблица 1. Результаты мета-анализа по показателю «общий билирубин» (данные исследования P.L. Nicastri) [18]
|
Исследование / подгруппы
|
Адеметионин
|
Контроль
|
Средние
различия,
95% ДИ
|
Средние различия, 95% ДИ
|
|
Среднее значение
|
Стандартное отклонение
|
Среднее значение
|
Стандартное отклонение
|
|
P.L. Nicastri (1998)
Адеметионин
vs плацебо
|
132,6
|
53,04
|
17,68
|
8,84
|
114,92
(77,66;
152,18)
|
|
|
P.L. Nicastri (1998)
Адеметионин + УДХК
vsУДХК
|
176,8
|
35,36
|
106,08
|
35,36
|
70,72 (36,07;
105,37)
|
|
Тест для обобщенной оценки эффекта
|
Z=4,18 (P<0,0001)
|
92,27
(48,97;
135,57)
|
В пользу контроля
|
В пользу адеметионина
|
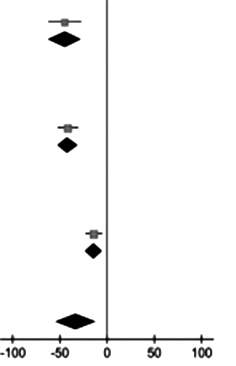
Таблица 2. Результаты мета-анализа по показателю «общий билирубин» (данные исследований QinBo и ZhuShishu) [18]
|
Исследование /
подгруппы
|
Адеметионин
|
Контроль
|
Средние различия, 95% ДИ
|
Средние различия, 95% ДИ
|
|
Среднее значение
|
Стандартное отклонение
|
Среднее значение
|
Стандартное отклонение
|
|
Qin Bo
(холестатический гепатит, 2000)
Адеметионин vs плацебо
|
37,49
|
22,73
|
82,23
|
26,11
|
-44,74
(-62,26; - 27,22)
|
|
|
Qin Bo (вирусный
гепатит с холестазом, 2000)
Адеметионин vs плацебо
|
34,57
|
16,29
|
76,08
|
21,14
|
-41,51
(-52,42; -30,60)
|
|
Zhu Shishu (лекарственно
индуцированное поражение
печени, 2010)
Адеметионин vs плацебо
|
21
|
11
|
35
|
19
|
-14
(-22,78; -5,22)
|
|
Гетерогенность данных
Тест для обобщенной оценки эффекта
Тест для различий в подгруппах
|
P<0,0001
Z=3,03, P=0,002
?2 = 19,13, P<0,0001
|
-32,70 (53,85; -11,55)
|
В пользу адеметионина
|
В пользу
контроля
|
Таблица 3. Результаты мета-анализа по показателю «АСТ» (данные исследований QinBo и ZhuShishu) [18]
|
Исследование / подгруппы
|
Адеметионин
|
Контроль
|
Средние различия, 95% ДИ
|
Средние различия, 95% ДИ
|
|
Среднее значение
|
Стандартное отклонение
|
Среднее значение
|
Стандартное отклонение
|
|
Zhu Shishu
(лекарственно
индуцированное
поражение печени, 2010)
Адеметионин vs плацебо
|
36
|
12
|
52
|
20
|
-16,00
(-25,33; -6,67)
|
|
|
Qin Bo (вирусный
гепатит с холестазом, 2000)
Адеметионин vs плацебо
|
38,88
|
32
|
56,25
|
56,01
|
-17,37
(-43,73; 8,99)
|
|
Тест для обобщенной оценки эффекта
|
Z=3,60 (Р=0,0003)
|
-16,15
(-24,95; -7,36)
|
В пользу
адеметионина
|
В пользу
контроля
|
Адеметионин не повышал число побочных явлений в сравнении с плацебо (169 пациентов) [18]: статистически значимых различий между адеметионином и плацебо не было (относительный риск (ОР) 95% ДИ 0,94 (0,59; 1,52), P=0,81) [18]. Только в 1 исследовании, включавшем 123 пациента, приведены показатели смертности и трансплантации печени, результаты были использованы для оценки долгосрочного прогноза лечения адеметионином. Отмечена отчетливая тенденция в пользу адеметионина в сравнении с группой плацебо (95% ДИ 0,55 (0,27; 1,09), Р=0,09) [18].
Таблица 4. Результаты мета-анализа по показателю «кожный зуд» (данные исследований P.L. Nicastri) [18]
|
Исследование / подгруппа
|
Адеметионин
|
Контроль
|
Средние различия, 95% ДИ
|
Средние различия, 95% ДИ
|
|
Среднее значение
|
Стандартное отклонение
|
Среднее значение
|
Стандартное отклонение
|
|
P.L. Nicastri (1998)
Адеметионин vs плацебо
|
1,4
|
0,2
|
0,9
|
0,1
|
0,5 (0,35; 0,65)
|
|
|
P.L. Nicastri (1998)
Адеметионин + УДХК
vs УДХК
|
1,8
|
0,5
|
0,8
|
0,3
|
1,00 (0,6; 1,4)
|
|
Гетерогенность данных
Тест для обобщенной оценки эффекта
Тест для различий
в подгруппах
|
?2=0,1, ?2=5,13 (Р=0,02)
Z=2,89, P=0,004
?2=5,13, P=0,02
|
0,71 (0,23; 1,20)
|
В пользу
контроля
|
В пользу
адеметионина
|
Анализ данных в подгруппах: беременные [18]. Проведен мета-анализ 3 исследований с участием беременных женщин (P. L. Nicastri,H. JinyangиT. Binder) [18]. В подгруппе беременных (193 пациентки) оценивали параметры ОБ, АЛТ, АСТ, число побочных явлений, данные о зуде (в баллах). По критерию ОБ у P.L. Nicastri выявлены статистически значимые различия между группой лиц, получавших терапию адеметионином и группой плацебо (MD 95% ДИ 92,27 (48,97, 135,57), P<0,0001). Статистически значимых результатов по АЛТ и АСТ не было достигнуто, число побочных явлений на фоне применения адеметионина статистически значимо не отличалось от группы плацебо. В исследовании P.L. Nicastri показано статистически значимое снижение выраженности зуда (в баллах) при терапии адеметионином в сравнении с плацебо: MD 95% ДИ 0,71 (0,23; 1,20), P=0,004 [18]. Полученные результаты согласуется с недавно опубликованными данными мета-анализа (по критерию «зуд» у беременных) 2013 года [19].
Сравнительный анализ эффективности и безопасности адеметионина, УДХК и стронгер неоминофаген С (SNMC) [18]. Как УДХК, так и SNMC были более эффективны, чем адеметионин при лечении вирусного гепатита, при этом на фоне их применения не возникало повышения риска побочныхявлений [18].
Безопасность адеметионина. Получены убедительные данные об отсутствии статистически значимых различий между адеметионином и плацебо по частоте нежелательных явлений (см. выше) [18]. Это подтверждает выводы относительно безопасности применения адеметионина, приведенные в двух ранее опубликованных Кокрановских анализах: а) у беременных женщин [19], б) у пациентов с алкогольной болезнью печени [21]. Указанные исследования показали отсутствие статистически значимых различий между адеметионином и плацебо по числу несерьезных нежелательных явлений; серьезных нежелательных явлений на фоне адеметионина отмечено не было.
Таким образом, в систематическом обзоре и мета-анализе (2015) [18] подтвержденыэффективность и безопасность адеметионина в лечении хронических заболеваний печени [18]. По мнению авторов, адеметионин может быть использован для базисной терапии с целью улучшения функции печени (в особенности благодаря безопасности этого ЛС) [18].
Антидепрессивное действие адеметионина. По данным последних лет (Е.Б. Грищенко, М.И. Щекина, 2014), от 60 до 85% хронических заболеваний пищеварительной системы сопровождается эмоциональными расстройствами разной степени выраженности. Характерным является выявление депрессивных расстройств у лиц, страдающих хроническими диффузными заболеваниями печени различного генеза и их осложнений [5]. Известно, что антидепрессанты могут оказывать гепатотоксическое действие; так, высоким риском гепатотоксического действияхарактеризуется сертралин [2].
Эффективность в качестве антидепрессанта доказана в многочисленных экспериментальных и клинических исследованиях (например, мета-анализ 47 исследований(2002), показавший статистически значимый эффект адеметионина в сравнении с плацебо, расцениваемый как «частичный ответ на лечение» [20]). У пациентов с заболеваниями печени важно своевременно купировать возникающие аффективные расстройства назначением адеметионина [5]. Известно, что антидепрессивное действие адеметионина (описанное около 20 лет назад [15]) отличается от такового известных антидепрессантных ЛС, таких как ингибиторы обратного захвата норадреналина и серотонина или ингибиторы монооксигеназы [8, 12, 13]. Некоторые авторы полагают, что наиболее адекватно назначение адеметионина пациентам с умеренной депрессивной симптоматикой, у которых традиционные антидепрессанты не дают желаемых результатов или плохо переносятся [8, 11, 16]. Сочетание гепатотропного, антиоксидантного и детоксикационного эффектов, а также уникального антидепрессивного действия адеметионина [3] указывает на целесообразность его применения у пациентов с алкогольным поражением печени, в том числе при наличии депрессии и абстинентного синдрома [4].
Особенностью фармакокинетики адеметионина является его способность проникать в спинномозговую жидкость и через гематоэнцефалический барьер [22]; полагают, что адеметионин может проникать в центральную нервную систему посредством Na-независимых систем переносчика нуклеозидов в капиллярах эндотелия мозга [22]. После применения фармацевтических препаратов адеметионина для парентерального и орального применения происходит увеличение концентрации указанного активного вещества в плазме и спинномозговой жидкости человека [15]. Полученные данные указывают на способность адеметионина активно участвовать в метаболизме клеток нервной ткани.
Производитель (государственное предприятие «Академфарм») выпускает препарат с использованием субстанции адеметионина из высококачественной европейской субстанции S-аденозил-L-метионина 1,4-бутандисульфонат(Omniabios s.r.l., Италия), регистрационное удостоверение №1949/15; б) по стандартам GMP, что обеспечивает высокое качество лекарственного средства «ГепталНАН».
В соответствии с Клиническим протоколом «Диагностика и лечение пациентов с заболеваниями органов пищеварения» (утвержден Постановлением Министерства здравоохранения Республики Беларусь от 21 июля 2016 г. №90) адеметионин применяется в терапии хронического гепатита в дозах 800–1600 мг/сутки длительно, а также назначается пациентам с циррозом печени (при холестазе) в дозах 800–1600 мг/сутки длительно.
Таблетки «ГепталНАН» следует принимать внутрь целиком, не разжевывая и запивая достаточным количеством воды. Таблетки не следует принимать вместе с пищей.
Продолжительность лечения. Длительность терапии зависит от тяжести и течения заболевания и определяется врачом индивидуально.
Выводы:
1. Применение адеметионина регламентировано Клиническим протоколом «Диагностика и лечение пациентов с заболеваниями органов пищеварения» (утвержден Постановлением Министерства здравоохранения Республики Беларусь от 21 июля 2016 г. №90). Адеметионин (включая лекарственное средство «ГепталНАН» производства «Академфарм», Республика Беларусь) входит в Республиканский формуляр лекарственных средств 2016 года (утвержден Постановлением Министерства здравоохранения Республики Беларусь от 01.07.2016 №80).
2. Отечественное импортозамещающее лекарственное средство «ГепталНАН» предназначено для применения у взрослых пациентов с ВПХ при прецирротических и цирротических состояниях, беременности, а также с симптомами депрессии.
3. Белорусский генерик адеметионина «ГепталНАН» выпускается государственным предприятием «Академфарм» по стандартам GMP из высококачественной европейской субстанции (Omniabios s.r.l., Италия).
Л И Т Е Р А Т У Р А
1. Барышникова Н.В., Белоусова Л.Н. // Consilium medicum. Гастроэнтерология. – 2014. – №2. – С.16–18.
2. Выборных Д.Э., Кикта С.В. // Клинич. перспективы гастроэнтерологии, гепатологии. – 2010. – №6. – С.21–28.
3. Вялов С.С. // РМЖ. – 2013. – №31. – С.1621.
4. Голованова Е.В. // Фарматека. – 2010. – №12.– С.82–87.
5. Грищенко Е.Б., Щекина М.И. // Психиатрия и психофармакотерапия им. П.Б. Ганнушкина. – 2014. – №4. – С.52–57.
6. Губергриц Н.Б. // Новости медицины и фармации. Гастроэнтерология. – 2008. – №264. – http://www.mif-ua.com/archive/article/6319.
7. Губергриц Н.Б. и др. // Сучасна гастроентерологія. – 2014. – №4 (78). – С.106–118.
8. Каминская Ю.М. // Мед. новости. – 2016. – №3. – С.40–44.
9. Маковецкая М. // Здоров ‘я УкраÏни. – 2016. – №11–12 (384–385). – С.18–19.
10. Новиков В.Е., Климкина Е.И. // Обз. клин фармакол. лек. тер. – 2005. – Т.4, №1. – С.2–20.
11. Оганов Р.Г., Ольбинская Л.И., Смулевич А.Б. и др. // Кардиология. – 2004. – №1. – C.48–49.
12. Птицина С.Н. // Фарматека. – 2010. – №20 (213). – С.26–34.
13. Смулевич А.Б., Дубницкая Э.Б., Иванов С.В. // Психиатрия и психофармакотерапия им. П.Б. Ганнушкина. – 2002. – №3. – С.99–101.
14. Юрьев К.Л. // Укр. мед. часопис. – 2011. – №3 (83) – С.8–15.
15. Bottiglieri T. // Expert Opin. Investig. Drugs. – 1997. – Vol.6, N4. – P.417–426.
16. Fetrow C.W., Avila J.R. // Ann. Pharmacother. – 2001. – Vol.35, N11. – P.1414–1425.
17. Choudhuri G., Singh T. // Int. J. Res. Health Sci. [Internet]. – 2014. – Vol.2 (3). – P.831–841.
18. Guo T., Chang L., Xiao Y., Liu Q. // PLoS ONE. – 2015. – Vol.10, N3. – e0122124 (doi:10.1371/journal.pone.0122124).
19. Gurung V., Middleton P., Milan S.J., et al. // Cochrane Database Syst. Rev. – 2013. – Vol.6. – D493.
20. Hardy M., Coulter I., Favreau J., et al. S-Adenosyl-L-Methionine for Treatment of Depression, Osteoarthritis, and Liver Disease: Agency for Healthcare Research and Quality. – 2002. – [Электрон. ресурс]. – Режим доступа: [https://archive.ahrq.gov/clinic/tp/sametp.htm]. – Дата доступа: 08.11.2016.
21. Rambaldi A., Gluud C. // Cochrane Database Syst. Rev. – 2006. – Vol.2. – D2235.
22. Reichel A., Chishty M., Begley D.J. // J. Physiology. – 1997. – Vol.505. – P.48–49.
23. Virukalpattigopalratnam M.P., Singh T., Ravishankar A.C. // J. Indian Med. Assoc. – 2013. – Vol.111, N12. – P.856–859.
Медицинские новости. – 2016. – №11. – С. 28-32.
Внимание! Статья адресована врачам-специалистам. Перепечатка данной статьи или её фрагментов в Интернете без гиперссылки на первоисточник рассматривается как нарушение авторских прав.