Solovei S.P.
Republican Scientific Practical Center “Cardiology”, Minsk, Belarus
New perspectives in the treatment of stable angina: focus on ranolazine
Резюме. В статье обсуждаются фармакологические особенности и перспективы клинического использования антиишемического препарата ранолазин. Приводится обзор исследований, позволивших включить ранолазин в Американские и Европейские рекомендации по лечению стабильной стенокардии. Недавно в Республике Беларусь зарегистрировано новое отечественное генерическое лекарственное средство «РАНОЛАЗИН-НАН». «РАНОЛАЗИН-НАН» произведен Государственным предприятием «АКАДЕМФАРМ» в соответствии с требованиями GMP.
Ключевые слова: ранолазин, стенокардия напряжения, ишемическая болезнь сердца, антиангинальная терапия, качество жизни, клинические исследования, острый коронарный сидром, фибрилляция предсердий, сахарный диабет, лекарственное средство Государственного предприя-тия «АКАДЕМФАРМ», «РАНОЛАЗИН-НАН».
Медицинские новости. – 2016. – №7. – С. 29–35.
Summary. The article discusses the pharmacological characteristics and perspectives for clinical use the anti-ischemic drug ranolazine. A review of studies is offered allowing ranolazine inclusion in the US and European guidelines for the treatment of stable angina. In the Republic of Belarus a new domestic generic drug “RANOLAZINE?-NAN” was recently registered. “RANOLAZINE?-NAN” is produced by the State enterprise “AKADEMPHARM” in accordance with the requirements of GMP.
Keywords: ranolazine, angina pectoris, IHD, antianginal therapy, quality of life, clinical trials, acute coronary syndrome, atrial fibrillation, diabetes mellitus, the drug of the State enterprise “ACADEMPHARM”, “RANOLAZINE?-NAN”.
Meditsinskie novosti. – 2016. – N7. – P. 29–35.
В последние годы в экономически развитых странах наблюдается определенное снижение смертности от болезней системы кровообращения, в том числе ишемической болезни сердца (ИБС). Очевидный прогресс в терапии пациентов с ИБС связан как с появлением новых групп лекарственных препаратов, так и с ростом частоты использования процедур коронарной реваскуляризации. Тем не менее изменить ведущий вклад сердечно-сосудистых заболеваний в структуру смертности до настоящего времени не удалось. Более того, подсчитано, что распространенность ИБС к 2030 г. увеличится на 9,3%, а прямые медицинские затраты возрастут на 198% по сравнению с таковыми в 2010 г. (P. Heidenreich и соавт., 2011).
Как начальные проявления ИБС примерно в половине случаев выступает стабильная стенокардия. Почти у 50% пациентов с острым коронарным синдромом в анамнезе имеются приступы ангинозных болей. Современная кардиология обладает широким арсеналом средств, рациональное применение которых позволяет добиваться удовлетворительного контроля стенокардии. Однако, несмотря на все достижения медицины, значимая часть пациентов продолжает испытывать клинические симптомы, что в значительной степени снижает активность и качество повседневной жизни. При наличии огромного числа проводимых чрескожных коронарных вмешательств и операций аортокоронарного шунтирования (АКШ) остается актуальным использование адекватной медикаментозной терапии при стабильной ИБС, направленной на купирование и профилактику основной клинической симптоматики заболевания. Так, по разным оценкам, от 25 до 60% пациентов в течение первого года после проведенного коронарного вмешательства требуется назначение антиангинального лечения (Ю.А. Карпов, 2014). Известно также, что у 25% пациентов после успешной реваскуляризации миокарда, даже при приеме всех рекомендованных препаратов, через 5 лет симптомы ишемии появляются вновь [1].
В силу вышеперечисленных обстоятельств одной из главных задач лечения пациентов, страдающих стабильной стенокардией, по-прежнему остается уменьшение частоты и интенсивности болевых приступов с целью повышения качества жизни (КЖ). Последнее характеризует успешность терапии хронических заболеваний в целом. У пациентов со стабильной стенокардией влияние на КЖ оказывает частота и длительность ангинозных приступов. В таком случае улучшение КЖ может быть достигнуто при условии уменьшения болевых эпизодов и увеличения толерантности к физическим нагрузкам. Кроме того, КЖ данной категории пациентов может четко отражать дальнейший прогноз для жизни. Так, в 2002 г. группой исследователей впервые было показано, что наличие значительного ограничения физической активности по причине стенокардии, в сравнении с минимальным ограничением, в 11,5 раз повышает риск летального исхода, а при большой частоте приступов риск смерти увеличивается в 2,4 раза (Spertus и соавт., 2002). По данным Р.Г. Оганова и соавт. (2007), наличие некупированных ангинозных приступов повышает риск смертности от ИБС в 2,2 раза у мужчин и в 1,7 раз – у женщин. Только полное или почти полное устранение эпизодов ишемии улучшает прогноз заболевания, что также отчетливо продемонстрировали результаты исследования TIBBS: выживаемость пациентов с частотой приступов более шести в неделю оказалась существенно ниже, чем у тех, у кого частота менее двух в неделю (vonAmimTh. и соавт., 1996). Таким образом, очень важно и пациенту, и врачу быть убежденными в необходимости устранения количества эпизодов ишемии до минимума (М.Г. Глезер, 2012).
В рекомендациях Европейского общества кардиологов по лечению стабильной ИБС, представленных в обновленной версии в августе 2013 г. [2], указано, что в качестве препаратов 1-й линии для уменьшения симптомов стенокардии и/или выраженности ишемии миокарда рекомендованы к длительному применению бета-адреноблокаторы и/или антагонисты кальция (класс доказательности IIA, уровень доказательности А). В качестве препаратов 2-й линии, которые могут быть присоединены к препаратам 1-й линии или использоваться как препараты 1-й линии (класс доказательности I, уровень доказательности С) при непереносимости последних, относят пролонгированные нитраты, ранолазин, ивабрадин, никорандил (класс доказательности IIA, уровень доказательности В) и может рассматриваться триметазидин (класс доказательности IIВ, уровень доказательности В).
Заслуживает внимания относительно новый рекомендованный препарат ранолазин. Препарат относится к пиперазиновому ряду, запатентован в 1986 г. и применяется в США с одобрения Управления по надзору за качеством пищевых продуктов и лекарственных средств (Food and Drugs Administration of the United States, FDA) с 2006 г. в качестве средства для лечения стабильной стенокардии. В 2008 г. Европейским агентством по оценке лекарственных средств (ЕМЕА) выдано разрешение на маркетинг данного препарата в странах Евросоюза, и с этого года ранолазин присутствует на европейском рынке. В 2012 г. препарат включен в Американские рекомендации, а в 2013 г. – в Европейские рекомендации по улучшению симптомов у пациентов со стабильной ИБС. В России доступен с 2013 г. С 2014 г. ранолазин зарегистрирован в Украине и с 2015 г. присутствует на внутреннем фармацевтическом рынке (Республика Беларусь).
Механизм действия ранолазина уникален и принципиально нов, что выгодно отличает его от других лекарственных средств при стабильной стенокардии и позволяет говорить о появлении современного класса антиангинальных препаратов. Как известно, в основе клинических проявлений стенокардии лежит преходящая ишемия миокарда. В условиях ишемии происходит перегрузка кардиомиоцитов ионами кальция, что в свою очередь приводит к нарушению расслабления миокарда во время диастолы и нарушению диастолического наполнения коронарных артерий, провоцируя тем самым возникновение приступа стенокардии. Ранолазин является мощным селективным ингибитором позднего натриевого тока (INa). Предотвращая перегрузку кардиомиоцитов ионами натрия, препарат блокирует обратный натриево-кальциевый обмен и, соответственно, накопление в клетке ионов кальция. Это способствует улучшению механической и электрической функции миокарда путем улучшения диастолического расслабления и коронарного кровотока, в том числе на уровне микроциркуляции, субэндокардиальных слоях, причем без влияния на параметры гемодинамики, артериальное давление (АД) и частоту сердечных сокращений (ЧСС), и независимо от них (рис. 1).
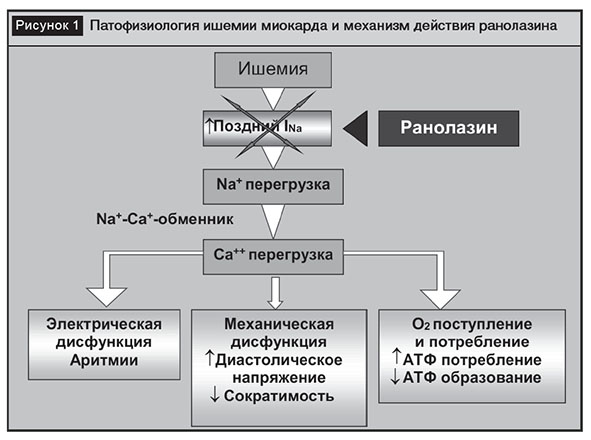
Следует сказать, что, поскольку сразу было очевидным отсутствие влияния ранолазина на гемодинамические показатели, его механизм действия связывали с улучшением метаболизма кардиомиоцита подобно триметазидину [3, 4]. В настоящее время считают, что препарат, ингибируя 3-кетоацетил-КоА-тиолазу и стимулируя пируватдегидрогеназу, модулирует метаболизм ишемизированных миоцитов путем переключения энергетического обмена в сердце с окисления свободных жирных кислот на окисление глюкозы. За счет этого, а также благодаря обрaтимому ингибированию NADH-дегидрогеназы в митохондриях, утилизация кислорода ишемизированным миокардом повышается, образуется большее количество аденозинтрифосфорной кислоты. В условиях ишемии данный эффект может дополнительно способствовать уменьшению симптомов последней [5].
Ранолазин выпускается как для перорального, так и для внутривенного применения, но только таблетированная форма с замедленным высвобождением (slow release, SR) по 500 и 1000 мг используется в клинической практике. Следует отметить, что к этому пришли не сразу, выбор оптимального режима терапии был найден в ходе многочисленных клинических испытаний препарата.
Одними из первых сравнение немедленно высвобождающегося ранолазина с плацебо у пациентов, страдающих стенокардией, провели в 1994 г. в двойном слепом исследовании Ranolazine Study Group [6]. У 318 человек терапия ранолазином в дозах 30, 60 и 120 мг, назначаемого 3 раза/сут. на протяжении 4 недель, не выявила его достоверных преимуществ по частоте болевых приступов, толерантности к нагрузке и показателям холтеровского 48-часового ЭКГ-мониторирования. Объяснялось это недостаточной дозой препарата и использованием лекарственной формы немедленного высвобождения. Аналогичные результаты получили и другие исследователи [7]. Поэтому, когда стало ясно, что в небольших дозах ранолазин не способен оказывать достаточное антиангинальное действие при монотерапии, его стали использовать в комбинированном лечении вместе с бета-адреноблокаторами или антагонистами кальция. В этом случае препарат демонстрировал аддитивный эффект при добавлении к терапии метопрололом (200 мг/сут.), пропранололом (100 мг/сут.) или дилтиаземом (180 мг/сут.), правда, разовая доза все же была увеличена до 240 мг [8].
В последующем появились работы по исследованию больших доз ранолазина. Так, в 2005 г. опубликованы данные перекрестного плацебо-контролируемого исследования RAN080 [9]. Сравнивали влия-ние ранолазина быстрого высвобождения (400 мг 3 раза/сут.) и атенолола (100 мг 1 раз/сут.) после недельной терапии на симптоматику стабильной стенокардии, лимитированной физической нагрузкой. Оба препарата вызывали статистически значимое улучшение переносимости нагрузки по сравнению с плацебо: отмечались увеличение продолжительности нагрузки, снижение вызванной нагрузкой ишемии, частоты и длительности стенокардии. Эффективность ранолазина и атенолола была эквивалентной, однако при приеме ранолазина, в отличие от атенолола, урежение ритма и снижение артериального давления не отмечались.
Таким образом, назначение ранолазина в больших дозах (400 мг 2–3 раза/день) оказывало антиишемический эффект в условиях высокой концентрации препарата в плазме крови (от 1576 нг/мл на пике концентрации до 602 нг/мл перед приемом следующей дозы). Другими словами, для обеспечения антиангинального и антиишемического эффектов на фоне физической активности концентрацию ранолазина в крови следует поддерживать более высокой [10]. Поэтому препарат начали использовать в виде лекарственной формы пролонгированного действия, и в настоящее время ранолазин выпускается в двух дозировках: 500 и 1000 мг – замедленного высвобождения. Рекомендованная начальная доза составляет 500 мг 2 раза в сутки, которая постепенно через 2–4 недели при необходимости и хорошей переносимости может быть увеличена до стандартной 1000 мг 2 раза в сутки. Максимальная суточная доза – 2000 мг.
Высокая эффективность и параметры профиля безопасности ранолазина изучались в крупных многоцентровых клинических исследованиях (MARISA, CARISA, ERICA, MERLIN-TIMI, TERISA, ROLE), в которых приняли участие в общей сложности более 8 тыс. пациентов.
В многоцентровом плацебо-контролируемом перекрестном исследовании MARISA [11], схожем по дизайну с исследованием RAN080, показана эффективность монотерапии ранолазином в профилактике приступов стенокардии. Включались пациенты (n=191) со стенокардией напряжения, получавшие бета-адреноблокаторы, антагонисты кальция и/или органические нитраты. Средний возраст составил 64,3±9,4 года, большинство из них (73,3% мужчин и 52,3% женщин) имели в анамнезе перенесенный инфаркт миокарда (ИМ). Перед началом исследования все антиишемические препараты, кроме нитроглицерина по потребности, были отменены. Далее пациенты получали 500, 1000, 1500 мг ранолазина или плацебо дважды в сутки в течение 1 недели, после чего проводили тестирование на тредмиле. Монотерапия ранолазином во всех дозировках переносилась хорошо и оказалась эффективной: продолжительность физической нагрузки возрастала соответственно на 94, 103 и 116 с (р<0,005 по сравнению с плацебо), т.е. наблюдался дозозависимый эффект. Гемодинамические показатели (АД, ЧСС) на фоне лечения практически не менялись. Прекращение приема ранолазина не приводило к усилению или увеличению частоты приступов стенокардии. Не наблюдалось и развития толерантности к лечению.
Одной из наиболее значимых работ по изучению клинической эффективности ранолазина следует считать многоцентровое двойное слепое исследование CARISA (Combination Assessment of Ranolizine in Stable Angina) [12], в котором приняли участие 823 пациента со стабильной стенокардией тяжелого течения и неудовлетворительными показателями тредмил-теста. Все пациенты на момент включения в исследование получали атенолол (50 мг/сут.), амлодипин (5 мг/сут.) или дилтиазем (180 мг/сут.) в качестве основного антиишемического средства. Дополнительно в течение 12 недель назначался ранолазин в дозах 750 мг 2 раза/сут., 1000 мг 2 раза/сут. или плацебо. Исследование показало достоверное улучшение переносимости физической нагрузки при обоих режимах дозирования, подтвержденное результатами нагрузочной пробы, уменьшением количества болевых приступов при обычной нагрузке и снижением потребления нитроглицерина. Различия в сравнении с группой плацебо достигали статистической значимости уже на 2-й неделе приема. Также прослеживалась зависимость эффекта препарата от дозы, поскольку в группе ранолазина 1000 мг 2 раза/сут. уменьшение частоты приступов стенокардии (на 36,4%) и приема нитроглицерина (на 42%) оказалось более выраженным, хотя и не достигло статистических различий с группой ранолазина 750 мг 2 раза/сут. Не отмечено развития толерантности, синдрома отмены, клинически значимого влияния на АД и ЧСС.
Свою эффективность в составе комбинированной антиангинальной терапии продемонстрировал ранолазин и в исследовании ERICA (Antianginal Efficacy of Ranolazine When Added to Treatment with Amlodipine, 2006),гдеоценивалось взаимодействие ранолазина с антагонистами кальция [13]. Включались пациенты (n=565) со стабильной стенокардией, которые продолжали испытывать ангинозные приступы (≥3 в неделю), несмотря на прием амлодипина в максимальной дозе 10 мг/сут. Участники были рандомизированы в группы приема амлодипина с ранолазином (n=281) и амлодипина с плацебо (n=284). Ранолазин в первую неделю назначался в дозе 500 мг дважды в сутки, затем – 1000 мг дважды в сутки. Сопутствующая терапия включала ацетилсалициловую кислоту, иАПФ, статины, диуретики, противодиабетические средства (в т.ч. инсулин), почти половина пациентов в каждой группе получала пролонгированные нитраты. Общая продолжительность лечения составила 6 недель. На фоне хорошей переносимости ранолазина отмечено достоверное снижение частоты стенокардии и потребления нитроглицерина, причем независимо от возраста пациен-тов и сопутствующего использования пролонгированных нитратов. Более того, чем чаще изначально регистрировались приступы стенокардии, тем более выраженным был эффект препарата!
Ранолазин прошел проверку клинической эффективности не только при стабильной ИБС, но также и при острой форме заболевания. Исследователи, проводившие крупнейшее на сегодняшний день испытание ранолазина MERLIN-TIMI 36,проанализировали эффективность и безопасность препарата в группе пациентов с острым коронарным синдромом (ОКС) без подъема сегмента ST, у которых перед госпитализацией имелась стабильная стенокардия [14]. Исследование имело три цели: определить влияние ранолазина на частоту сердечно-сосудистых событий при ОКС (нестабильной стенокардии/ИМ без подъема сегмента ST с умеренным либо высоким риском); проанализировать эффективность ранолазина в комплексной терапии хронической ИБС; уточнить безопасность препарата. Приняли участие 6560 пациентов из 440 центров 17 стран. На фоне стандартной медикаментозной терапии назначался ранолазин (внутривенно в течение 12–96 ч, затем per os по 1000 мг 2 раза/сут., при клиренсе креатинина <30 мл/мин – по 500 мг 2 раза/сут.) или плацебо. Среднее время наблюдения составило 348 дней.
Частота регистрации основной комбинированной конечной точки (сердечно-сосудистая смерть (CCC), ИМ, рецидивирующая ишемия миокарда) была практически одинаковой в группах ранолазина и плацебо: 21,8% и 23,5%. Тем не менее если риск CCC или ИМ существенно не различался в обеих группах, то риск рецидивирующей ишемии был достоверно ниже на фоне приема ранолазина: 13,9% против 16,1%, ОР 0,87 (р=0,030) (рис. 2).
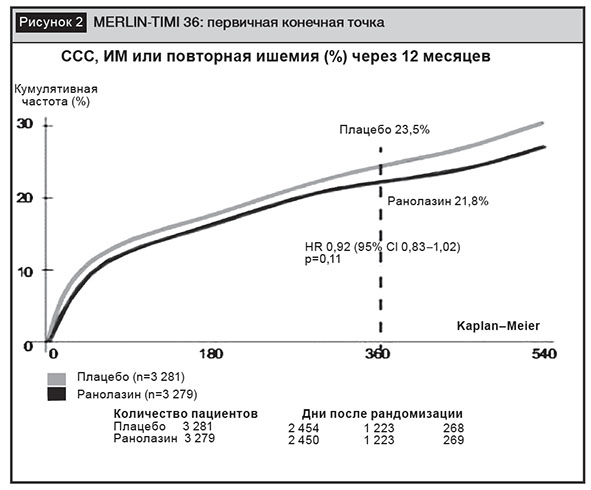
Интересно, что в подгруппе пациен-тов без предшествующей острому коронарному синдрому стенокардии эффективность ранолазина в отношении рецидивов ишемии не отмечена! И еще одно наблюдение заслуживает внимания. Когда провели подгрупповой анализ среди пациентов с повышенным уровнем мозгового натрийуретического пептида, оказалось, что ранолазин все же снижал показатели первичной комбинированной конечной точки в этой когорте. Учитывая особенности кровоснабжения миокарда, осуществляемого из артериол в период диастолы, снижение ранолазином диастолического напряжения путем ингибирования позднего Na-тока и уменьшение экстравазальной компрессии мелких сосудов могут способствовать улучшению миокардиального кровотока. Вероятно, такие механизмы действия у данных пациентов и явились определяющими в осуществлении положительного прогностического влияния препарата.
Анализ дополнительных конечных точек в исследовании MERLIN-TIMI 36 подтвердил антиангинальную эффективность ранолазина. Так, на фоне приема препарата риск ухудшения симптомов стенокардии был на 23% ниже, и на 19% ниже – вероятность назначения еще одного антиангинального средства. Через 8 месяцев терапии достоверно увеличились продолжительность физической нагрузки на тредмиле (514 с против 482 с в контроле; р=0,007), время до возникновения стенокардии (508 с против 477 с в контроле; р=0,002) и время до наступления депрессии сегмента ST на 1 мм (509 с против 479 с в контроле; р=0,003).
Несмотря на то, что в группе ранолазина чаще отмечались головокружение (12,4% против 7,4%), тошнота (9,7% против 6,1%), запоры (8,5% против 3,3%), вследствие чего и отменялся препарат несколько чаще, чем плацебо (8,1% против 4,1%; р<0,001), в целом терапия переносилась хорошо [15]. Однако при оценке профиля безопасности все же вызывало опасение отмеченное в других исследованиях препарата удлинение корригированного интервала QTс (корригированное с учетом ЧСС значение QT) без клинических случаев развития опасных аритмий типа torsades de pointes, причем дозозависимое: в среднем – 6,1 мс на фоне приема 750 мг ранолазина в сутки и 9,2 мс – на фоне приема 1000 мг в исследовании САRISA; 6, 7 и 11 мс на фоне приема 500, 1000 и 1500 мг/сут. соответственно в исследовании MARISA. Такие изменения являются результатом как ингибирования быстро выпрямляющего калиевого тока, что удлиняет желудочковый потенциал действия, так и ингибирования INa, что укорачивает желудочковый потенциал действия. Известно, что удлинение интервала QTc повышает возможность индукции аритмии и неустойчивой желудочковой пароксизмальной тахикардии – пируэтной тахикардии (torsades de pointes), при которой комплекс QRS непрерывно меняется по форме, направлению, амплитуде, длительности, часто сопровождается повторными обмороками и может возникнуть фибрилляция желудочков [16]. Однако ни в одном из представленных исследований этого феномена не наблюдалось. А проведенный популяционный анализ показал, что применение ранолазина как у пациентов со стабильной стенокардией, так и у здоровых добровольцев приводит к удлинению интервала QT относительно исходного уровня в среднем на 2,4–2,6 мс при концентрации ранолазина в плазме 1000 нг/мл (в случае выраженной печеночной недостаточности скорость удлинения QT возрастает) [17].
Тем не менее удлинение интервала QTс явилось предметом детального изучения и в исследовании MERLIN-TIMI 36. В итоге, в группе плацебо увеличение интервала QTc (≥450 мс – у мужчин, ≥470 мс – у женщин) было связано с двукратным повышением риска внезапной сердечной смерти (ВСС). В группе ранолазина связь между аномальной величиной QTc и ВСС была сравнима с таковой в группе плацебо (HR 1,8, р=0,074). Другими словами, существенных различий в отношении опасности ВСС между группами плацебо и ранолазина у пациентов с патологией QTc выявлено не было (HR 0,78, р=0,48).
В то же время не исключен определенный риск при одновременном приеме ранолазина и препаратов, удлиняющих интервал QT. Поэтому при такой комбинации необходимо соблюдать осторожность, контролировать ЭКГ, учитывая возможные фармакологические взаимодействия.
Частота возникновения аритмий, вызванных воздействием на интервал QT, в клинических исследованиях ранолазина оказалась сопоставимой с группой плацебо. Более того, были выявлены антиаритмические свойства препарата. Так, в исследованииMERLIN-TIMI 36пациентам в течение 7 суток после рандомизации проводили мониторирование ЭКГ. В группе ранолазина в сравнении с группой плацебо наблюдалось достоверно меньшее число эпизодов желудочковой тахикардии (166 (5,3%) против 265 (8,3%), p<0,001), включая желудочковую тахикардию типа «пируэт» ≥8 сокращений на 1 эпизод, суправентрикулярной тахикардии (1413 (44,7%) против 1752 (55,0%), p<0,001), впервые возникшей фибрилляции предсердий (ФП) (55 (1,7%) против 75 (2,4%), р=0,08), пауз от 3 с и более (97 (3,1%) против 136 (4,3%), р=0,01). Таким образом, ранолазин не только не показал проаритмического действия (которое могло иметь место в связи со свойством препарата удлинять QTc), но и продемонстрировал способность профилактировать развитие некоторых нарушений ритма при ОКС. Однако данное свойство требует еще дальнейшего изучения.
Данные о роли ионов Na, Са, К и ионообменников в формировании аритмической активности сердца явились предпосылками к изучению антиаритмических свойств ранолазина. Установлено, что в желудочках препарат ингибирует позднюю фазу внутреннего тока INa (поздний INa). Эффект заключается в сокращении потенциала действия и уменьшении задержки активации быстрого ретрификационного тока калия (IKr), удлинении продолжительности потенциала действия. В предсердиях, в дополнение к блокаде позднего INa и IKr, ранолазин замедляет пик потока Na-каналов (пик INa), а также имеет определенное воздействие на другие токи, такие как ICaL, INa–Ca и IKs [18]. Согласно результатам, полученным в отдельных работах, существуют ионные каналы, специфичные только для предсердий, и каналы, имеющиеся в обеих камерах сердца, но ингибирование которых приводит в основном к изменениям электрофизиологических свойств предсердий, к последним и относятся Na-каналы. В работе А. Burashnikov и соавт. была показана селективность действия ранолазина в отношении блокирования Na-каналов именно в предсердиях. Подавление ФП в изолированных миоцитах предсердий происходило при такой концентрации ранолазина, которая вообще не вызывает электрофизиологических изменений в желудочках или инициирует их в незначительной степени [19]. Способность ранолазина подавлять предсердные тахиаритмии и ФП, вероятно, связана с его многоканальными блокирующими свойствами. Препарат вызывает предсердно-селективное, частотно-зависимое снижение параметров в зависимости от функций Na-канала, таких как скорость деполяризации, диастолический порог возбуждения и постреполяризующая рефрактерность [20]. Было отмечено, что в миоцитах предсердий пациентов с персистирующей ФП ингибирующее действие ранолазина на поздние INa сильнее, чем у пациентов с синусовым ритмом [21].
Подтверждением эффективности применения препарата при ФП служат результаты ряда выполненных исследований. В одном из них ранолазин (2000 мг) назначали 18 пациентам с впервые возникшей или пароксизмальной ФП длительностью не более 48 ч: 13 из 18 пациентов восстановили синусовый ритм в течение 6 ч от начала приема, т.е. 72% конверсии оказались сравнимы с другими результатами протоколов «таблетка в кармане» [22]. Был сделан вывод, что ранолазин в дозе 2000 мг может быть эффективен для восстановления синусового ритма у пациентов с пароксизмальной ФП. И эти данные оказались перспективными, несмотря на небольшой объем выборки. Так, в рандомизированном исследовании у 51 пациента изучали безопасность и эффективность комбинации амиодарона и ранолазина по сравнению с амиодароном с точки зрения кардиоверсии недавно развившейся ФП. Частота восстановления ритма в течение 24 ч (первичная конечная точка) составила 88% в группе с сочетанием амиодарона и ранолазина по сравнению с 65% в группе лечения одним амиодароном (p=0,056). Время до восстановления ритма также было короче в группе комбинированной терапии [23].
В конце 2014 г. опубликовали результаты исследования IIb-фазы HARMONY (A StudytoEvaluatetheEffectofRanolazineandDronedaroneWhenGivenAloneandinCombinationinPatientsWith Paroxysmal Atrial Fibrillation), изучавшего безопасность и эффективность ранолазина в комбинации с дронедароном при пароксизмальной форме ФП. В исследование были включены 134 пациента с пароксизмальной формой ФП и имплантированным двухкамерным электрокардиостимулятором. Анализ показал снижение частоты возникновения ФП при совместном приеме препаратов (ранолазин 1500 мг, дронедарон 500 или 300 мг) по сравнению с плацебо на 59%, а при раздельном приеме ранолазина и дронедарона – только на 17% и 9% соответственно [24].
В исследовательских работах с экспериментальными моделями было показано, что ранолазин в паре с амиодароном обладают синергичным эффектом с точки зрения подавления ФП [25, 26]. Данные результаты подтверждают гипотезу об эффективности комбинации блокаторов открытых и инактивированных натриевых каналов, которые могут купировать и предупреждать возникновение пароксизмов ФП [27]. Полученные результаты в будущем могут способствовать дальнейшему совершенствованию медикаментозного лечения ФП.
Возвращаясь к исследованиюMERLIN-TIMI 36, следует еще раз подчеркнуть, что эта работа обнаружила много важных находок. Одной из них явилось то, что у пациентов со стенокардией и сахарным диабетом 2 типа (СД2) терапия ранолазином в течение 4 месяцев привела не только к уменьшению приступов стенокардии (причем с тенденцией большей терапевтической пользы у лиц с СД2, чем в его отсутствие!), но и к достоверному снижению на 32% частоты возникновения новых случаев повышения гликированного гемоглобина (HbA1c) [28]. Впоследствии ретроспективное изучение материалов других исследований ранолазина у пациен-тов со стенокардией навело на мысль о том, что его эффективность в подгруппах с сопутствующим диабетом может быть связана не только с собственно антиангинальным действием, но и со способностью снижать уровень HbA1c. Однако тогда еще эта гипотеза не была изучена проспективно. Позже, в 2013 г., были опубликованы данные проспективного исследования TERISA «Изучение ранолазина при диабете 2 типа у пациентов с хронической стабильной стенокардией» (Type 2 Diabetes Evaluation of Ranolazine in Subjects With Chronic Stable Angina,n=949), которые также продемонстрировали способность препарата уменьшать число приступов стенокардии и потребность в сублингвальном нитроглицерине у пациентов с СД2, уже получавших один или два антиангинальных препарата [29]. Количество эпизодов стенокардии в неделю снижалось с 6,7 до 3,8 (4,3 – в контрольной группе, р=0,008), сублингвального нитроглицерина – с 4,3 до 1,7 раз в неделю (2,1 – в контрольной группе). Это исследование стало первым проспективным международным рандомизированным контролируемым исследованием, направленным специально на изучение антиангинальной медикаментозной терапии (ранолазином или иным образом) пациентов СД2 – терапевтически сложной группы, с высокой степенью риска неблагоприятных событий. Весьма важным явилось обнаружение большей выраженности полезного антиангинального действия ранолазина у пациентов с более высокими уровнями HbA1c по сравнению с более низкими, а также то, что препарат способствует более быстрому снижению плазменных концентраций HbA1c.
Исходя из полученной новой информации, впоследствии было спланировано исследование 3 фазы, нацеленное на изучение безопасности и эффективности ранолазина при его назначении с целью контроля гликемии. Включались пациенты с СД2 и исходным уровнем HbA1c 7–10%. В первой ветви данного исследования (n=465) ранолазин назначался в виде монотерапии. Доза препарата 1000 мг 2 раза/сут. обеспечила через 24 недели снижение HbA1c на 0,56% от исходного, к 12-й неделе число достигших HbA1c <7% возросло примерно на 50%. Также достоверно улучшились и уровни тощаковой гликемии. В этой группе параллельно наблюдалось достоверное уменьшение уровней глюкагона натощак и через 3 часа после еды, что, возможно, может иметь отношение к объяснению механизма сахароснижающего действия ранолазина.
Во второй ветви исследования 215 пациентам, получавшим глимепирид 4 мг, назначали ранолазин 1000 мг 2 раза/сут., а 216 – составили группу глимепирида плюс плацебо. Как и в случае с монотерапией, присоединение ранолазина через 24 недели уменьшило уровни HbA1c на 0,5% по сравнению с плацебо и обеспечило снижение гликемии натощак. А уровень HbA1c <7% был достигнут у почти в 2 раза большего числа пациентов. Наиболее частыми нежелательными явлениями на фоне приема ранолазина являлись тошнота, головная боль, головокружение и запоры. У 4 пациентов, получавших монотерапию, отмечалась гипогликемия. Однако тяжелой гипогликемии, тем не менее, не зарегистрировали, и в целом препарат хорошо переносился.
В третьей ветви исследования пациенты принимали метформин 1000 мг 2 раза/сут. После рандомизации, если они попадали в группу ранолазина, доза метформина уменьшалась до 500 мг 2 раза/сут., а рандомизированные в группу плацебо пациенты продолжали получать 1000 мг. Продиктовано это было наличием лекарственного взаимодействия между метформином и ранолазином: последний уменьшает почечный клиренс метформина. Доза 500 мг выбрана таким образом, чтобы пациенты имели к завершению исследования такие же концентрации метформина в сыворотке, как и у тех, кто получал плацебо с препаратом. По мнению авторов исследования, именно со снижением дозы метформина и был связан тот факт, что в комбинации с метформином ранолазин не оказал влияние на уровень HbA1c.
Резюмируя полученные данные, следует сказать, что механизм гликометаболического действия ранолазина до сих пор точно не установлен. В эксперименте препарат повышает стимулированную глюкозой секрецию инсулина, возможно, за счет воздействия на ионные каналы b-клеток поджелудочной железы. Эффективное антиангиальное действие у пациентов с СД делает ранолазин перспективным антиишемическим препаратом при сочетании стабильной стенокардии и нарушенного метаболизма глюкозы.В последних Европейских рекомендациях по стабильной ИБС особо подчеркивается эффективность ранолазина у пациентов со стенокардией и высоким уровнем HbA1c.
Клинические исследования препарата обнаруживают и другие дополнительные, плейотропные, эффекты терапии. Так, имеются работы, демонстрирующие благоприятное влияние ранолазина на функцию эндотелия сосудов у пациентов со стабильной стенокардией. В работе S.H. Deshmukh и соавт. (2007) применение препарата в дозе 1000 мг 2 раза/сут. в течение 6 недель значительно увеличивало эндотелиальную вазодилатацию при пробе с реактивной гиперемией на плечевой артерии по сравнению с плацебо [30]. При этом одновременно происходило снижение такого маркера воспаления как высокочувствительный С-реактивный белок. Природа данных эффектов также пока не ясна. Возможно, в дальнейшем накопление наших знаний о препарате поможет окончательно раскрыть механизм его разнопланового действия.
Что касается переносимости ранолазина, то с целью уточнения характера и частоты побочных явлений, а также частоты отмены при длительном применении (>2 лет) было выполнено открытое исследование ROLE (Ranolazine Open Label Extension programme), в которое включались 746 пациентов, участвовавших в исследованиях MARISA и CARISA и выразивших желание принять участие в анализе безопасности и переносимости препарата. В первые 6 недель проводилась титрация ранолазина до оптимальной дозы (с 500 до 1000 мг 2 раза/сут.) и разрешалось лечение другими антиангинальными средствами. Переносимость препарата оценивалась через 1 месяц после титрации и затем каждые 3 месяца. Наиболее часто отмечаемыми нежелательными явлениями были головокружение (11,8%) и запор (10,9%). Данные жалобы по отдельности или в комбинации с другими нежелательными явлениями привели к досрочному завершению лечения у 7 (0,9%) и 5 (0,6%) пациентов соответственно. Выявлена статистически значимая корреляция частоты прекращения лечения из-за нежелательных явлений с пожилым возрастом (≥64 лет) пациентов (относительный риск 2,32; p<0,001) [31].
Следует отметить возможное снижение амплитуды и, реже, появление двугорбого зубца Т на ЭКГ на фоне приема ранолазина. Частота развития синкопе составляет менее 1%, при этом синкопы и постуральная гипотония встречались у принимающих высокие дозы препарата (2000 мг/сут.). Однако все эти нежелательные эффекты в большинстве случаев могут быть предотвращены при титрации ранолазина от небольших доз до максимальных с оценкой эффективности и переносимости.
Ранолазин подвергается быстрому и практически полному метаболизму в печени, где метаболизируется системой цитохромов (изоферменты CYP3A4 и CYP2D6). При недостаточной функции печени или приеме ингибиторов цито-хрома плазменная концентрация ранолазина может увеличиваться. Поэтому следует учитывать вероятность развития потенциально значимого лекарственного взаимодействия с препаратами, в биотрансформации которых участвует система цитохрома Р450. Так, кетоконазол может повышать концентрацию ранолазина в крови в 3 раза и более [32]. К средним ингибиторам CYP3A относятся дилтиазем, верапамил, эритромицин и др. При комбинированном применении ранолазин может увеличить концентрацию в крови симвастатина и дигоксина [33, 34].
При почечной недостаточности легкой или средней степени тяжести (клиренс креатинина 30–80 мл/мин), печеночной недостаточности легкой степени, хронической сердечной недостаточности NYHA III–IV ФК, у пожилых пациентов и с низким весом (≤60 кг) рекомендуется тщательный и осторожный подбор дозы. При клиренсе креатинина <30 мл/мин и пациентам с печеночной недостаточностью средней или тяжелой степени препарат противопоказан.
После приема ранолазина внутрь максимальная концентрация в плазме крови достигается через 2–6 ч. Биодоступность составляет 35–50% с высокой степенью индивидуальной вариабельности. Пища не влияет на скорость и полноту всасывания. При приеме препарата дважды в сутки стационарная концентрация в плазме достигается в течение 3 дней. Выводится ранолазин почками, период полувыведения – 7 ч.
Применяется ранолазин преимущественно в комбинации с бета-адреноблокаторами, антагонистами кальция, нитратами. Однако при непереносимости основных антиишемических средств или изначальной склонности к артериальной гипотонии и брадикардии возможна монотерапия ранолазином. Препарат подходит для пациентов, у которых дальнейшее увеличение дозы «классических» антиангинальных препаратов может отрицательно сказаться на гемодинамике, и в первую очередь показан пациентам, у которых невозможно выполнение реваскуляризации, в связи с чем требуется максимально усилить медикаментозную терапию.
Выводы:
1. Доказанная клиническая эффективность, изученный профиль безопасности и хорошая переносимость ранолазина, а также возможность применения у пациентов с сопутствующими заболеваниями позволяет занять достойное место в арсенале препаратов для лечения стабильной стенокардии и стать хорошим дополнением к имеющимся антиишемическим средствам.
2. Ранолазин включен в Американские рекомендации, а также в Европейские рекомендации по улучшению симптомов у пациентов со стабильной ИБС. Появление на фармацевтическом рынке Республики Беларусь отечественного генерика, содержащего ранолазин («РАНОЛАЗИН-НАН»), позволяет обеспечить лечение пациентов в соответствии с международными стандартами.
3. Новое отечественное лекарственное средство «РАНОЛАЗИН-НАН», произведенное Государственным предприятием «АКАДЕМФАРМ», является аналогом оригинального лекарственного средства «РАНЕКСА», производитель Menarini-Von Heyden GmbH, Германия.
Л И Т Е Р А Т У Р А
1. Berger P. // JAMA. – 2004. – Vol.291, N3. – Р.365–367.
2. 2013 ESC guidelines on the management of stable coronary artery disease. The Task Force on the management of stable coronary artery disease of the European Society of Cardiology. http://eurheartj.oxfordjournals.org/ content/early/2013/ 08/28/eurheartj.eht296.
3. Lopaschuk G.D., Kantor P.F., Dyck J.R.B. // Medicographia. – 1999. – Vol.21, N2. – P.109–115.
4. Anderson J.R., Nawarskas J.J. // Cardiol. Rev. – 2005. – N13. – P.202–210.
5. Reffelmann T., Kloner R.A. // Exp. Rev. Cardiovasc. Ther. – 2010. – Vol.8, N3. – P.319–329.
6. Thadani U., Ezekowitz M., Fenney L., Chiang Y.-K. // Circulation – 1994. – Vol.90. – P.726–734.
7. Pepine C.J., Wolff A.A. // Am. J. Cardiol. – 1999. – Vol.84. – P.46–50.
8. Patel P.D., Arora R.R. // Cardiovasc. Health Risk Manag. – 2008. – Vol.4, N4. – P.819–824.
9. Rousseau M.F., Pouleur H., Cocco G., Wolff A.F. // Am. J. Cardiol. – 2005. –Vol.95. – P.311–316.
10. Метелица В.И. Справочник по клинической фармакологии сердечно-сосудистых лекарственных средств. – М., 2005.
11. Chaitman B.R., Skettino S.L., Parker J.O., et al. // J. Am. Coll. Cardiol. – 2004. – Vol.43. – P.1375–1382.
12. Chaitman B.R., Pepine C.J., Parker J.O., et al. // JAMA. – 2004. – Vol.291, N3. – P.309–316.
13. Stone P.H., Gratsiansky N.A., Blokhin A., et al. // J. Am. Coll. Cardiol. – 2006. – Vol.48, N3. – P.566–575.
14. Scirica B.M., Morrow D.A., Hod H., et al. // Circulation – 2007, Vol.116, N15. – P.1647–1652.
15. Wilson S.R., Scirica B.M., Braunwald E., et al. // J. Am. Coll. Cardiol. – 2009. – Vol.53. – P.1510–1516.
16. Michels G., Kochanek M., Hoppe U.C. // Dtsch Med. Wochenschr. – 2010. – Vol.135, N41. – P.2037–2040.
17. ГуревичМ.А., АгабанянД.А., КузьменкоН.А. // Русский мед. журнал. – 2014. – №31. – С.2196.
18. Antzelevitch C., Burashnikov A., Sicouri S. // Heart Rhythm. – 2011. – Vol.8, N8. – Р.1281–1290.
19. Burashnikov A., Di Diego J., Zygmunt A., et al. // Circulation – 2007. – Vol.116, N13. – P.1449–1457.
20. Dorian P., Pinter A., Mangat I., et al. // J. Cardiovasc. Pharmacol. – 2007. – Vol.50, N1. – Р.35–40.
21. Sossalla S., Kallmeyer B., Wagner S., et al. // J. Am. Coll. Cardiol. – 2010. – Vol.55. – Р.2330–2342.
22. Murdock D.K., Kersten M., Kaliebe J., Larrain G. // Indian Pacing Electrophysiol. J. – 2009. – Vol.9, N5. – Р.260–267.
23. Fragakis N., Koskinas К.С., Katritsis D.G., et al. // Am. J. Cardiol. – 2012. – Vol.110. – P.673–677.
24. HARMONY (A Study to Evaluate the Effect of Ranolazine and Dronedarone When Given Alone and in Combination in Patients With Paroxysmal Atrial Fibrillation. http://clinicaltrials. gov/show/NCT01522651 (дата обращения 16.06.2015).
25. Sicouri S., Burashnikov A., Belardinelli L., Antzelevitch C. // Circulation: Arrhythmia Electrophysiol. – 2010. – N3. – P.88–95.
26. Frommeyer G., Uphaus T., Kaese S., Eckardt L., Millberg P. Ranolazine amplifies the antiarrhythmic effect of amiodarone and dronedarone in an experimental whole-heart model of atrial fibrillation. Heart Rhythm Conference. 33rd Annual Scientific Sessions of the Heart Rhythm Society. – 2012. – N9 (Suppl. 5). – S259.
27. Burashnikov A., Sicouri S., Di Diego J.M., Belardinelli L., Antzelevitch C. // JACC. – 2010. – Vol.56. – P.1216–1224.
28. Morrow D.A., Scirica B.M., Chaitman B.R., et al. // Circulation. – 2009. – Vol.119, N15. – P.2032–2039.
29. Kosiborod M., Arnold S.V., Spertus J.A., et al. // J. Am. Coll. Cardiol. – 2013. – Vol.61, N20. – P.2038–2045.
30. Deshmukh S.H., Patel S.R., Pinassi E., et al. // Coron. Artery Dis. – 2009. – Vol.20, N5. – P.343–347.
31. Koren M.J. et al. // J. Am. Coll. Cardiol. – 2007. – Vol.49. – P.1027–1034.
32. Jerling M., Huan B.L., Leung K., et al. // J. Clin. Pharmacol. – 2005. – 45. – P.422–433.
33. Dobesh P.P., Trujillo T.C. // Pharmacotherapy. – 2007. – Vol.27, N12. – P.1659–1676.
34. Jerling M., Huan B.L., Leung K., et al. // J. Clin. Pharmacol. – 2005. – Vol.45. – P.422–433.
Медицинские новости. – 2016. – №7. – С. 29-35.
Внимание! Статья адресована врачам-специалистам. Перепечатка данной статьи или её фрагментов в Интернете без гиперссылки на первоисточник рассматривается как нарушение авторских прав.