Sujayeva V.A.
Republican Scientific and Practical center “Cardiology”, Minsk, Belarus
Various approaches to optimal medicament therapy of stable angina pectoris using ivabradine (coraxan)
Резюме. В статье приведена точка зрения Европейского общества кардиологов на лечение стабильной болезни коронарных артерий, мнение Американской Коллегии Кардиологов/Американской Ассоциации Сердца на ведение пациентов с хронической ишемической болезнью сердца, взгляд Национального института Здоровья и здравоохранения Великобритании на ведение пациентов со стабильной стенокардией. Рассмотрено значение новых лекарственных средств с точки зрения медицины, основанной на доказательствах. Представлен обзор научных исследований, посвященных эффективности нового лекарственного средства с антиишемическим действием – ингибитора If-каналов синусового узла ивабрадина в оптимальной медикаментозной терапии стабильной стенокардии. Рассмотрены различные патофизиологические механизмы формирования ишемии миокарда при стабильной стенокардии и возможности ивабрадина в воздействии на них.
Ключевые слова: стабильная стенокардия, ишемическая болезнь сердца, ингибитор If-каналов, ивабрадин, оптимальная медикаментозная терапия.
Медицинские новости. – 2016. – №5. – С. 17–22.
Summary. The point of view of the European Society of Cardiology on treatment of stable coronary artery disease and point of American College of Cardiology/American Heart Association on the management of patients with stable ischemic heart disease, National Institute for Health Care and Care Excellence on the management of stable angina according to Evidence-based medicine. The review of the scientific researches devoted to efficiency of new medicine with anti-ischemic action – an inhibitor of If of channels of sinus node (ivabradine) in optimal medicament treatment of stable angina pectoris is submitted. Various pathophysiological mechanisms of myocardial ischemia appearance at stable angina pectoris and a possibility of an ivabradine in that’s correction are considered at the article.
Keywords: stable angina pectoris, ischemic heart disease, inhibitor of If of channels, ivabradine, optimal medicament treatment.
Meditsinskie novosti. – 2016. – N5. – P. 17–22.
Увеличение продолжительности жизни, гиподинамия, нерациональное и несбалансированное питание, стрессы и прочие «побочные эффекты цивилизации» привели к росту распространенности ишемической болезни сердца (ИБС), которая в XXI веке приобрела характер эпидемии. Успехи, достигнутые в лечении острого коронарного синдрома (ОКС) и инфаркта миокарда (ИМ), обусловили увеличение числа лиц с хроническими формами ИБС. По данным Американской Коллегии кардиологов/Американской Ассоциации сердца (American College of Cardiology/American Heart Association – AСС/АНА), каждый третий взрослый житель США (т. е. около 81 млн человек) имеют то или иное сердечно-сосудистое заболевание (ССЗ), при этом более 17 млн имеют коронарную болезнь сердца и около 10 млн страдают стенокардией [1]. В 2014 году распространенность хронической ИБС в США составила в среднем 3,2% (от 2,9% до 11,9% в зависимости от возраста), частота новых случаев стенокардии с учетом пола и возраста составляла от 14,1 до 39,3 на 1000 населения в год [2].
В Европе ситуация с болезнями системы кровообращения (БСК) носит схожий характер. По данным Европейского кардио-логического общества (EuropeanSocietyofCardiology – ESC), распространенность стенокардии в 2013 г. составила 5–7% среди женщин 45–64 лет, 10–12% – среди женщин 65–84 года (у мужчин – 4–7% и 12–14% соответственно). Смертность от стабильной ИБС составила 0,6–1,4% в зависимости от возраста и пола, а доля в общей структуре смертности достигла 22% у женщин и 20% у мужчин. В странах Центральной и Восточной Европы и заболеваемость, и смертность от БСК еще выше указанных значений [3].
По данным Национального института Здоровья и здравоохранения Великобритании (NationalInstituteforHealthCareandCareExcellence – NICE), около 8% мужчин и 3% женщин в возрасте 55–64 года имеют стенокардию, в возрасте 65–74 года эта цифра растет и составляет 14% и 8%, соответственно, т. е. около 2 млн британцев страдают стенокардией, которая способствует ухудшению качества жизни, ограничивают профессиональную и повседневную активность [4].
На протяжении последних 5 лет многими кардиологическими сообществами Европы, Великобритании и США пересмотрены рекомендации, регламентирующие тактику ведения пациентов с хронической ИБС, которые учитывают вновь полученные научные данные об эпидемиологии заболевания, об информативности различных методов диагностики, эффективности медикаментозного, хирургического и интервенционного лечения. Так, в 2011 г. NICE опубликовала точку зрения британских кардиологов по ведению стабильной стенокардии – «Stableangina: management» [4]. В 2012 г. вышли Американские рекомендации по диагностике и ведению па-циентов со стабильной ИБС – «2012 ACCF/AHA/ACP/AATS/PCNA/SCAI/STSGuidelinefortheDiagnosisandManagementofPatientsWithStableIschemicHeartDisease» [1]. В 2013 г. увидели свет Европейские рекомендации по лечению пациентов со стабильной болезнью коронарных артерий (БКА) – «2013 ESCGuidelinesonthemanagementofstablecoronaryarterydisease» [3].
Обращают на себя внимание некоторые различия в названиях указанных рекомендаций, отражающие особенности взгляда на патофизиологию формирования ишемии миокарда, национальные демографические различия, отличия в финансировании систем здравоохранения, особенности лекарственного обеспечения и т. д. Кроме того, Британские рекомендации охватывают решение узкой проблемы – только лечение стенокардии, Американские рекомендации освещают более широкий круг вопросов – ведение пациентов со стабильной хронической ИБС, а Европейские рекомендации посвящены ведению стабильной БКА и включают также описание диагностических и лечебных подходов к особым формам стенокардии, протекающим в отсутствии диагностически значимого поражения коронарных артерий (вазоспастическая и микроваскулярная стенокардия).
Несмотря на наличие вышеуказанных различий, общим для всех рекомендаций является определение с позиции медицины, основанной на доказательствах, места различных видов медикаментозного, интервенционного и хирургического лечения при стабильной хронической ИБС для обеспечения максимальной пользы от каждого из указанных видов вмешательств.
Согласно Рекомендациям NICE при лечении пациентов со стабильной стенокардией преследуются следующие цели [4]:
1) купировать приступ (для чего рекомендованы короткодействующие нитраты);
2) проводить вторичную профилактику ИБС: аспирин 75 мг в день и статины – у всех пациентов, ингибиторы ангиотензинпревращающего фермента (иАПФ) показаны у пациентов с сахарным диабетом (СД), коррекция артериального давления (АД, при наличии сопутствующей артериальной гипертензии (АГ));
3) назначить антиангинальное лечение: бета-адреноблокаторы (БАБ) или антагонисты ионов кальция (АК) – препараты первой линии. Выбор одного из них осуществляется в зависимости от сопутствующей патологии, противопоказаний и предпочтений пациента. При непереносимости препаратов первой линии рекомендовано назначить нитраты пролонгированного действия, ивабрадин, никорандил или ранолазин. Вышеуказанные лекарственные средства также рекомендовано добавить к БАБ или АК в составе комплексного лечения стенокардии при недостаточной эффективности БАБ и/или АК.
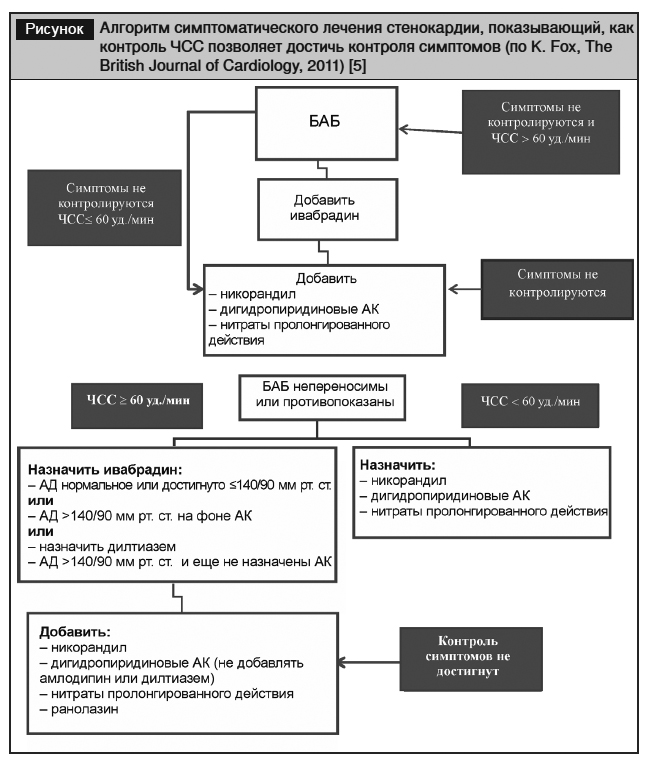
Однако профессор K. Fox отмечает, что такой подход к выбору препаратов не учитывает патофизиологических механизмов формирования ишемии миокарда у каждого конкретного пациента и предлагает свой алгоритм лечения стенокардии, учитывающий принцип персонализации лечения [5] (рисунок).
Медикаментозное лечение стабильной ИБС согласно Американским рекомендациям (2012) предполагает достижение двух основных целей [1].
1. Предотвращение развития ИМ и смерти.
Для этого используются (класс рекомендаций I):
– аспирин 75–162 мг/сут и/или клопидогрель 75 мг/сут;
– БАБ: должны назначаться не менее 3 лет после перенесенного ИМ или ОКС; у всех пациентов с левожелудочковой дисфункцией – фракция выброса левого желудочка (ФВ ЛЖ) ≤40%, ХСН, перенесшим ИМ (кроме имеющих противопоказания); всем пациентам с коронарной болезнью сердца или другими ССЗ;
– иАПФ: должны назначать всем пациентам с хронической ИБС, имеющим АГ, СД, ФВ ≤40%, хроническую болезнь почек (ХБП), за исключением имеющих противопоказания;
– блокаторы рецепторов ангиотензина II (БРА): должны назначать пациентам, имеющим непереносимость иАПФ.
2. Медикаментозное лечение для уменьшения симптомов:
Класс рекомендаций I:
– БАБ: должны назначаться в качестве начальной терапии;
– АК или нитраты пролонгированного действия: должны назначаться для уменьшения выраженности симптомов у пациентов, имеющих противопоказания или непереносимость БАБ вследствие развития побочных эффектов;
– АК или нитраты пролонгированного действия: должны назначаться в комбинации с БАБ при сохраняющихся симптомах у пациентов, уже получающих БАБ.
Класс рекомендаций IIa:
– недигидропиридиновые АК пролонгированного действия (верапамил или дилтиазем) могут назначаться вместо БАБ в качестве начальной терапии для уменьшения симптомов;
– ранолазин может назначаться в качестве начальной терапии вместо БАБ для уменьшения симптомов в том случае, если на фоне приема БАБ развились непереносимые побочные эффекты, а также при неэффективности БАБ и при наличии противопоказаний;
– ранолазин в комбинации БАБ: могут назначаться для уменьшения выраженности симптомов, если монотерапия БАБ неэффективна.
Обращает на себя внимание, что в качестве альтернативы БАБ и АК рассматривается только ранолазин. Это связано с тем, что на момент выхода Рекомендаций АСС/АНА 2012 года никорандил, ивабрадин и триметазидин не были зарегистрированы в США.
Согласно Рекомендациям ESC (2013) целями лечения стабильной БКА являются профилактика развития неблагоприят-ных сердечно-сосудистых событий и улучшение прогноза, а также устранение симптомов стенокардии и/или ишемии миокарда [3].
В зависимости от имеющейся доказательной базы лекарственные средства для лечения стабильной БКА делятся на препараты первой и второй линии. Препараты первой линии способствуют уменьшению риска развития неблагоприятных сердечно-сосудистых событий, т. е. благоприятно воздействую на прогноз. К ним относят нитроглицерин (НГ) короткого действия (для устранения приступов стенокардии), БАБ и АК. Препараты второй линии, как правило, способствуют уменьшению выраженности симптомов, относительно влияния на прогноз данных – недостаточно либо они носят противоречивый характер. К препаратам второй линии для лечения стабильной БКА Европейское общество кардиологов относит нитраты пролонгированного действия, ивабрадин, никорандил, триметазидин, ранолазин [3].
Доказанным влиянием на прогноз обладают аспирин (в случае непереносимости может назначаться клопидогрель), статины (для всех категорий пациентов с установленным диагнозом стабильной ИБС). У некоторых категорий пациентов (с ХСН, АГ, СД) для улучшения прогноза используются иАПФ, в случае их непереносимости – БРА [3].
Для устранения симптомов/ишемии миокарда в виде монотерапии или комбинированного лечения показано назначение препаратов первой линии (с учетом эффективности и переносимости). При недостаточной эффективности моно- или комбинированной терапии препаратами первой линии необходимо добавить препараты второй линии. У отдельных пациентов в зависимости от наличия сопутствующих заболеваний и переносимости препараты второй линии могут быть назначены в качестве препаратов первой линии. У бессимптомных пациентов (с безболевой ишемией миокарда), имеющих большие (>10%) зоны ишемии миокарда по данным визуализационных тестов, следует назначить БАБ. У пациентов с вазоспастической стенокардией в качестве препаратов первой линии используются АК и нитраты, назначение БАБ необходимо избегать [3].
Еще одним объединяющим все упомянутые рекомендации подходом является разделение антиангинальных лекарственных средств на препараты первой и второй линии (с учетом влияния на прогноз).
Однако исторический опыт и, соответственно, доказательная база для упомянутых классов антиангинальных средств существенно отличаются. Например, нитраты используются для лечения стенокардии с середины XIX века: в 1867 г. Brunton описал применение амилнитрита в виде ингаляции при стенокардии. В конце 60-х годов ХХ века появились лекарственные формы нитроглицерина пролонгированного действия.
Бета-адреноблокатор пропранолол был синтезирован в 1964 г. J. Black, который получил за это открытие в 1988 г. Нобелевскую премию. АК (верапамил) были предложены для использования A. Fleckenstein в 1969 г. Триметазидин синтезирован в 80-х годах ХХ века, никорандил используется для лечения стенокардии с 1994 г., ивабрадин был одобрен EuropeanMedicinesAgency в 2005 г., применение ранолазина при стенокардии, рефрактерной к традиционной терапии, разрешено лишь с 2008 г. Поэтому триметазидин, никорандил, ивабрадин и ранолазин зачастую именуются «новыми» антиангинальными лекарственными средствами [6].
Тот факт, что ивабрадин относится к «новым» антиангинальным агентам, обусловливает продолжение крупных многоцентровых исследований в отношении действия на «конечные точки», а также клинических исследований, направленных на установление всех возможных патофизиологических механизмов действия при стабильной стенокардии.
Основной, хорошо описанный антиангинальный эффект ивабрадина при стенокардии – уменьшение потребности миокарда в кислороде за счет снижения частоты сердечных сокращений (ЧСС) как в покое, так и при нагрузке. При этом ивабрадин не оказывает воздействие на АД, сократительную способность миокарда и проводимость [7].
Общеизвестно, что ивабрадин избирательно и специфически ингибирует If-каналы синоатриального соединения. При поддержании мембранного потенциа-ла на уровне -35мВ f-каналы закрыты, связывания ивабрадина с клетками синусового узла не происходит. Способность ингибировать If-каналы совершается при более отрицательном значении трансмембранного потенциала, когда канал находится в открытом состоянии. Такое специфическое свойство ивабрадина связываться с открытыми f-каналами определило концепцию «зависимой терапевтической полезности»:
1) уровень связывания ивабрадина зависит от уровня открытия f-каналов и ЧСС;
2) эффективность ивабрадина возрастает при увеличении ЧСС [8].
Описанные особенности механизма действия ивабрадина обусловливают его большую эффективность у пациентов с ЧСС ≥70 уд./мин как в виде монотерапии, так и в комбинации с БАБ. Весьма важным является также тот факт, что воздействие ивабрадина на ЧСС достигается с помощью механизмов, отличных от действия БАБ и недигидропиридиновых АК, что делает возможным использование ивабрадина у лиц, имеющих непереносимость или недостаточную эффективность указанных лекарственных средств.
Уменьшение ЧСС кроме снижения потребности миокарда в кислороде способствует увеличению субэндокардиального кровотока. Так, увеличение диастолического времени на 1% способствует росту субэндокардиального кровотока на 2,6–6%. В исследовании P. Colin и соавт. (2004) установлено также, что после внутривенного введения ивабрадина в дозе 0,25, 0,5 и 1,0 мг/кг массы тела наблюдалось дозозависимое уменьшение тахикардии при нагрузке на тредмиле, которое не сопровождалось нарушениями как локальной, так и глобальной контрактильной способности миокарда. Выявлена линейная закономерность между ЧСС показателем максимального потребления кислорода во время теста с чреспищеводной стимуляцией предсердий. Кроме того, внутривенное введение ивабрадина вызывало дозозависимое увеличение диастолического времени [9].
Аналогичный эффект препарата выявлен в экспериментальном исследовании X. Monnet и соавт. (2004). У 7 животных был инструментально индуцирован и откалиброван коронарный стеноз для ограничения возрастания коронарного кровотока во время 10-минутного теста с физической нагрузкой. Атенолол и ивабрадин, введенные до выполнения теста, в равной мере более эффективно, чем изотонический раствор, способствовали уменьшению прироста ЧСС при нагрузке. При нагрузке утолщение миокарда стенки ЛЖ после введения изотонического раст-вора уменьшилось от 23±4% до 2±1%, на фоне приема ивабрадина этот эффект был меньше и составил 10±3%. Кроме того, после приема ивабрадина постнагрузочный станнинг миокарда был существенно меньше, чем после введения изотонического раствора. Вышеизложенное в совокупности свидетельствует о том, что ивабрадин способствует уменьшению стресс-индуцированной ишемии миокарда при наличии гемодинамически значимых стенозов коронарных артерий [10].
Значение ЧСС напрямую связано с длительностью фазы диастолы: уменьшение ЧСС ведет к пролонгированию диастолического времени [11] и улучшению перфузии миокарда [12]. В этом состоит одно из важнейших отличий ивабрадина и БАБ, которые также обладают отрицательным хронотропным эффектом: БАБ способствуют пролонгированию фазы систолы.
Кроме того, у ивабрадина имеется свойство поддерживать коронарную вазодилятацию во время физической нагрузки, в то время как БАБ обладают вазоконстрикторным действием на коронарные артерии за счет блокады альфа-адренорецепторов [11].
Уменьшение потребности миокарда в кислороде в совокупности с увеличением миокардиальной перфузии под влиянием ивабрадина способствуют более экономичному функционированию миокарда. Взаимосвязь между уменьшением ЧСС на фоне приема ивабрадина и характером коллатерального коронарного кровотока у пациентов со стабильной БКА выявлена Gloekler и соавт. (2014). Исследование было проспективным, рандомизированным, плацебо-контролируемым, одноцентровым, в которое включено 46 пациентов с хронической стабильной БКА (23 – в группу плацебо, 23 – в группу ивабрадина). Основной анализируемый показатель – индекс коллатерального кровотока (collateralflowindex – CFI), который измерялся через 1 минуту после окклюзии коронарной артерии с помощью баллона. Через 6 месяцев ЧСС в группе плацебо увеличилась на 0,2±7,8 уд./мин, в группе ивабрадина – уменьшилась на 8,1±11 уд./мин (р=0,0089). В группе плацебо CFI уменьшился от 0,140±0,097 до 0,109±0,067 (р=0,12), в группе ивабрадина, напротив, он увеличился от 0,107±0,077 до 0,125±0,90 (р=0,0461). Авторы пришли к выводу, что ивабрадин способствует улучшению коллатерального коронарного кровотока при стабильной БКА уже через 6 месяцев приема препарата.
Наряду с этим препарат способствует росту ударного объема, уменьшению плотности коллагена ЛЖ и повышению плотности капилляров миокарда ЛЖ. В совокупности вышеописанные процессы способствуют оптимизации потребления энергии в миокарде, обратному ремоделированию и предотвращению прогрессирования ХСН [13].
По данным E.I. Skalidis и соавт. (2010), ивабрадин способствовал улучшению резерва коронарного кровотока у пациентов со стабильной БКА. Данный эффект был выявлен по данным измерения скорости коронарного кровотока во время коронароангиографии до и после введения аденозина [14].
Несмотря на то что ивабрадин относится к «новым» антиангинальным средствам, он изучен в ряде исследований по влиянию как на прогноз (табл. 1), так и на симптомы стенокардии/ишемию миокарда (табл. 2).
Таблица 1. Влияние ивабрадина на частоту развития неблагоприятных клинических событий
|
Исследование
|
Дизайн
|
Первичная конечная точка
|
Результат
|
|
BEAUTIFUL (the morBidity-mortality
EvAlUaTion of the I(f) inhibitor ivabradine in patients with coronary disease and left ventricULar dysfunction) [15]
|
Международное многоцентровое рандомизированное двойное слепое плацебо контролируемое.
10 917 пациентов со стабильной БКА и левожелудочковой дисфункцией (ФВ<40%)
|
Общая смертность + госпитализации в связи с острым ИМ + госпитализация в связи с вновь развившейся ХСН/ухудшением течения ХСН
|
Ивабрадин не влиял на частоту развития первичной конечной точки в сравнении с плацебо. В группе ивабрадина выявлено уменьшение частоты госпитализаций в связи с фатальным/нефатальным ИМ (р=0,001) и частоты реваскуляризаций (р=0,016)
|
|
SHIFT (Systolic Heart failure treatment with the I(f) inhibitor ivabradine Trial) [16]
|
Международное многоцентровое рандомизированное двойное слепое плацебо контролируемое. 3 года
|
Госпитализации в связи с ХСН, сердечно-сосудистая смерть
|
Ивабрадин способствовал уменьшению частоты госпитализаций
|
|
SIGNIFY (Study Assessing the Morbidity–Mortality Benefits of the I f Inhibitor Ivabradine in Patients with Coronary Artery Disease) [17]
|
Международное многоцентровое рандомизированное двойное слепое плацебо контролируемое. 19 102 пациента ≥55 лет со стабильной верифицированной леченной БКА, не имевшие ХСН 27,8 месяца
|
Смерть от сердечно-сосудис-
тых причин + ИМ
|
Значимых различий между группами ивабрадина и плацебо по влиянию на композитную конечную точку, а также сердечно-сосудистую смертность, частоту развития ИМ; внезапной сердечной смерти не выявлено. Отмечалось более выраженное уменьшение функционального класса стенокардии в сравнении с группой плацебо (р=0,01)
|
Таблица 2. Влияние ивабрадина на клиническое течение стабильной стенокардии
|
Исследование
|
Дизайн
|
Анализируемый
показатель
|
Результат
|
|
ASSOCIATE (evaluation of the Antianginal efficacy and Safety of the aSsоciation Of the If Current inhibitor ivAbradine with beta-blockEr) [18]
|
Двойное слепое рандомизированное плацебо контролируемое.889 па-циентов рандомизированы на прием ивабрадина 5 или 7,5 мг 2 раза в день + атенолол 50 мг 1 раз в день vs плацебо – 4 месяца
|
Тест с физической нагрузкой: длительность теста (с) время до появления стенокардии (с) время до появления и депрессии сегмента ST ≥1 мм частота развития побочных эффектов
|
Ивабрадин способствовал снижению ЧСС в покое и при нагрузке (р<0,001), увеличивал время выполнения теста, до появления стенокардии и депрессии сегмента ST ≥1 мм (р<0,05).
Частота развития побочных эффектов была сопоставима с плацебо
|
|
ADDITION (practical Daily efficacy anD safety of Procorolan In combination with betablockerS)
|
Многоцентровое открытое. 2330 пациентов со стабильной стенокардией
|
Приступы стенокардии
Потребность в короткодействующих нитратах Качество жизни
|
Частота приступов стенокардии уменьшилась от 1,7 до 0,3, количество таблеток НГ – от 2,3 до 0,4 в неделю
|
|
INITIATIVE (International Treatment of Angina with Ivabradine vs. Atenolol [19]
|
Рандомизированное двойное слепое сравнительное. 939 пациентов со стабильной стенокардией, документированной БКА 4 месяца принимали ивабрадин, начиная с 5 мг 2 раза в день, через 4 недели – 7,5 мг 2 раза в день – 3 месяца или атенолол 50 мг 1 раз в день, через 4 недели – атенолол 100 мг 1 раз в день – 3 месяца
|
Тредмил-тест: длительность теста (с) время до появления стенокардии (с)
Время до появления и депрессии сегмента ST ≥1 мм
|
Ивабрадин 7,5 мг 2 раза в день не хуже атенолола по всем параметрам, за исключением время до появления и депрессии сегмента ST ≥1 мм
|
|
REDUCTION Treatment of stable angina pectoris by ivabradine in every day practice [20]
|
Многоцентровое. 4954 пациента со стабильной стенокардией. 4 месяца
|
ЧСС
Приступы стенокардии
Потребность в короткодействующих нитратах
Частота развития побочных эффектов
|
Достоверное снижение ЧСС от 82,9±15,3 до 70,4±9,2 уд./мин (р<0,0001).
Частота приступов стенокардии уменьшилась с 2,4±3,1 до 0,4±1,5 в неделю (р<0,0001).
Потребность в приеме короткодействующего НГ уменьшилась от 3,3±4,4 до 0,6±1,6 т/неделю (р<0,0001).
Эффективность и безопасность оценивалась врачами, как «отличная/хорошая» у 97% и 98% пациентов, соответственно
|
Весьма важным является тот факт, что при проведении субанализа в исследовании BEAUTIFUL было установлено, что использование ивабрадина способствовало уменьшению числа развития неблагоприятных сердечно-сосудистых событий (сердечно-сосудистая смертность, госпитализации, фатальные и нефатальные ИМ, ХСН), а также снижению потребности в реваскуляризации миокарда у пациентов со стабильной БКА, стенокардией и снижением систолической функции ЛЖ [15].
При проведении субанализа SIGNIFY (StudyassessInGthemorbidity-mortalitybeNefitsoftheIfinhibitorivabradineinpatientswithcoronarYarterydisease), в которое было включено 19 102 пациента со стабильной БКА в возрасте старше 55 лет, установлено, что у лиц со стенокардией класса 2 и выше через 3 месяца приема ивабрадина использование препарата способствовало уменьшению числа случаев развития неблагоприятных сердечно-сосудистых событий в сравнении с плацебо [17].
Антиангинальное и антиишемическое действие ивабрадина в комбинации с БАБ и в виде монотерапии также не вызывает сомнений (см. табл. 2).
При лечении пациентов со стабильной стенокардией в клинической практике зачастую возникает проблема: улучшение прогноза, влияние на конечные точки и выраженность ишемии миокарда, по данным инструментальных методов исследования, не мотивируют пациента к приему препаратов. Сами больные зачастую отдают предпочтение лекарственным средствам, купирующим симптомы (например, периферическим вазодилятаторам), а не рекомендуемым препаратам первой линии, влияющим на прогноз. В этой связи весьма важными являются результаты исследования ADDITION, в котором с помощью опросника EuroQol 5 Dimension (использованы обе шкалы тревоги и депрессии – AnxietyandDepressionScore и визуально-аналоговая шкала) установлено влияние ивабрадина на качество жизни. Уменьшение числа приступов стенокардии и потребности в дополнительном приеме короткодействующего НГ способствовали значительному улучшению психоэмоционального статуса включенных в исследование пациентов [19].
Заключение
Таким образом, ивабрадин (кораксан) является достаточно хорошо изученным антиангинальным лекарственным средством, которое обладает удовлетворительным профилем безопасности, многокомпонентным действием на клинические и инструментальные проявления ишемии миокарда при стабильной стенокардии, особенно у пациентов со снижением контрактильной функции миокарда (ФВ<40%) и тахикардией, несмотря на прием бета-адреноблокаторов (ЧСС>70уд./мин).
Ивабрадин способствует уменьшению частоты развития неблагоприятных сердечно-сосудистых событий (госпитализации в связи с ХСН, частоту развития и потребность в госпитализации в связи с фатальным и нефатальным ИМ).
Препарат обладает сопоставимой с БАБ клинической эффективностью и может использоваться как в виде монотерапии, так и в комбинации с БАБ для лечения стабильной стенокардии. Выбор в пользу монотерапии ивабрадином возможен у пациентов, имеющих противопоказания и/или признаки непереносимости БАБ (например, при наличии вазоспастической стенокардии, хронической обструктивной болезни легких, артериальной гипотонии, заболеваний периферических артерий, запоров).
Выбор в пользу комбинированной терапии (ивабрадин и БАБ) возможен при недостаточной эффективности моно-терапии БАБ (особенно при невозможности достижения ЧСС≤70 уд/мин).
Учитывая наличие оригинальных, отличных от БАБ механизмов уменьшения ЧСС, возможно расширение показаний для использования препарата.
Л И Т Е Р А Т У Р А
1. Fihn S.D., Gardin J.M., Abrams J., et al. // Circulation. – 2012. – Vol.126, N25. – P.3097–3137.
2. Heart Disease and Stroke Statistics – 2014 Update: A Report From the American Heart Association.
3. Montalescot G., Sechtem U., Achenbach S., et al. // Eur. Heart. J. – 2013. – Vol.34, N38. – P.2949–3003.
4. National Institute for Health and Clinical Excellence. NICE clinical guideline 126. Management of stable angina. London: National Institute for Health and Clinical Excellence, 2011. www.nice.org.uk/guidance/CG126 (http://www. nice.org.uk/guidance/CG126).
5. Fox K. / Br. J. Cardiol. – 2011. – Vol.18 (Suppl. 3). – S.1–12.
6. Ferreira R.M. // Vol.12, N15. – 11 Feb 2014.
7. Fox K., Ford I., Steg P.G., Tendera M., Ferrari R. // Lancet. – 2008. – Vol.372 (9641). – P.807–816.
8. Руководство по кардиологии: учебное пособие в 3т. / под ред. Сторожакова Г.И., Горбаченкова А.А. – 2009. – Т.3. – 512 с.
9. Colin P., Ghaleh B., Monnet X., et al. / J. Pharm. Exp. Therap. – Vol.1308, N1. – P.236–240.
10. Monnet X., Colin P., Ghaleh B., et al. // Eur. Heart. J. – 2004. – Vol.25, N7. – P.579–586.
11. Heusch G. // J. Pharmacol. – 2008. – Vol.153, N8. – P.1589–1601.
12. Colin P., Ghaleh B., Monnet X., et al. // Am. J. Physiol. Heart. Circ. Physiol. – 2003. – Vol.284, N2. – H676–H682.
13. Mulder P., Barbier S., Chagraoui A., et al. // Circulation. – 2004. – Vol.109, N13. – P.1674–1679.
14. Skalidis E.I., Hamilos M.I., Chlouverakis G., et al. // Atherosclerosis. – 2011. – Vol.215, N1. – P.160–165.
15. Fox K., Ford I., Steg P.G., et al. // Eur. Heart. J. – 2009. – Vol.30, N19. – P.2337–2345.
16. Swedberg K., Komajda M., Bohm M., et al. / J. Am. Coll. Cardiol. – 2012. – Vol.59, N22. – P.1938–1945.
17. Fox K., Ford I., Steg P.G., et al. // Am. Heart. J. – 2013. – Vol.166, N4. – P.654–661.
18. Tardif J.C., Ponikowski P., Kahan T. // Int. J. Cardiol. – 2013. – Vol.168, N2. – P.789–794.
19. Tardif J.C., Ford I., Tendera M., et al. / Eur. Heart J. – 2005. – N26. – P.2529–2536.
20. Köster R., Kaehler J., Meinertz T. // Am. Heart J. – 2009. – Vol.158, N4. – e51–57.
Медицинские новости. – 2016. – №5. – С. 17-22.
Внимание! Статья адресована врачам-специалистам. Перепечатка данной статьи или её фрагментов в Интернете без гиперссылки на первоисточник рассматривается как нарушение авторских прав.