TrisvetovaE.L.1, PatorskayaO.A.1, PolyanskayaA.V.1, KaminskiyK.M.2, ShkrebnevaE.I.2, PonomarenkoI.N.3
1Belarusian State Medical University, Minsk, Belarus
29th City Clinical Hospital, Minsk, Belarus
3Minsk Consulting and Diagnostic Center, Minsk, Belarus
Post-marketing observation of the efficacy and safety of Mildronate
in patients with mitral valve prolapse
Резюме. Постмаркетинговое наблюдение позволяет подтвердить пользу Милдроната и вывить те проблемы, которые могут возникнуть у практического врача в результате применения лекарственного средства у пациентов с конкретной патологией. В наблюдении участвовали 89 пациентов (82 мужчины и 7 женщин) в возрасте 18–32 лет с пролапсом митрального клапана (ПМК) и системным вовлечением соединительной ткани.
В результате при лечении Милдронатом у пациентов с ПМК отмечалось улучшение субъективного состояния, метаболического и энергетического состояния миокарда, функции эндотелия. Доказательством хорошей переносимости и безопасности препарата, отсутствия побочных реакций явилась длительная приверженность к лечению.
Ключевые слова: Милдронат, посмаркетинговое наблюдение, пролапс митрального клапана, хроническая сердечная недостаточность, переносимость препарата.
Медицинские новости. – 2016. – №2. – С. 34–38.
Summary. The post-marketing observation allows to confirm the benefits of Mildronate and to identify problems that a practical doctor may be faced as a result of the exposure to the drug in patients with specific pathology. The observation involved 89 patients (82 men and 7 women) at the age of 18–32 years with mitral valve prolapse (MVP), and systemic involvement of connective tissue.
As a result, improvement of subjective state, metabolic and energy state of myocardium, endothelial function was observed in patients with mitral valve prolapse who had been taking Mildronate. A long-term compliance demonstrated a good tolerance to the drug and good safety, the absence of side effects.
Keywords: Mildronate, post-marketing observation, mitral valve prolapse, chronic heart failure, tolerance to the drug.
Meditsinskie novosti. – 2016. – N2. – P. 34–38.
Постмаркетинговое наблюдение приобретает все большую популярность в связи с тем, что позволяет подтвердить пользу определенного лекарственного препарата и выявить те проблемы, которые могут возникнуть у практического врача в результате применения лекарственного средства у пациентов с конкретной патологией.
Цель несравнительного открытого постмаркетингового наблюдения с последовательным включением пациентов – оценка эффективности и безопасности Милдроната при краткосрочном и долгосрочном применении при пролапсе митрального клапана (ПМК).
Изучению Милдроната, созданного в Латвийском институте органического синтеза, посвящено несколько сотен экспериментальных и клинических исследований различного уровня. В этих исследованиях у пациентов с ишемической болезнью сердца (ИБС) и хронической сердечной недостаточностью (ХСН) доказана кардиопротективная эффективность препарата в условиях острой и рецидивирующей транзиторной ишемии миокарда, в улучшении систолической и диастолической функции ишемизированного миокарда, эндотелиальной функции и липидного профиля. Применение препарата сопровождается повышением толерантности к физической нагрузке и улучшением качества жизни пациентов [1–5].
В течение 10 лет накоплен практический опыт применения Mилдроната при наследственных нарушениях соединительной ткани (ННСТ), синоним ННСТ – дисплазия соединительной ткани (ДСТ).
В исследованиях ведущих российских специалистов (Э.В. Земцовского и соавт., Т.И. Кадуриной и соавт., Г.И. Нечаевой и соавт.) по изучению влияния Милдроната на состояние здоровья, качество жизни, гемодинамические характеристики сердца, переносимость физической нагрузки, электрокардиографические признаки нарушения метаболизма у лиц с ННСТ отмечена эффективность препарата в составе комбинированной терапии [6–8].
Применение Милдроната в течение 4 месяцев у лиц молодого возраста с ДСТ способствовало улучшению качества жизни пациентов, снижению частоты жалоб на утомляемость, усталость, мышечную слабость, уменьшению доли пациентов с ЭКГ-признаками нарушения реполяризации, улучшению гемодинамических показателей при эхокардиографическом (ЭхоКГ) исследовании [7].
Методика патогенетического и симптоматического лечения пациентов с ННСТ, включающая Милдронат, предложенная Т.И. Кадуриной и соавт., не только улучшала клинико-биохимические показатели, но и замедляла темпы прогрессирования заболеваний [6].
При ПМК с системным вовлечением соединительной ткани отмечено улучшение функционального состояния сердечно-сосудистой системы и качества жизни у молодых людей, получавших Милдронат [8].
Милдронат относится к представителям новой группы препаратов – парциальным ингибиторам жирных кислот (partial fatty and oxidation inhibitors – pFOX-ингибитор), уменьшающих интенсивность ?-окисления свободных жирных кислот, ограничивающих транспорт через мембраны митохондрий длинноцепочечных жирных кислот, препятствующих накоплению недоокисленных жирных кислот в митохондриях [9].
По своему химическому строению Милдронат – структурный аналог непосредственного предшественника карнитина – гамма-бутиробетаина. Специфическая активность Милдроната обусловлена его способностью ингибировать карнитинзависимое окисление жирных кислот, снижая содержание карнитина и его метаболически активной фракции (ацилкарнитина) в миокарде [10]. В результате снижения уровня карнитина в цитозоле снижается скорость транспорта жирных кислот в митохондрии, восстанавливается транспорт произведенного АТФ в цитозоль и повышается активность окисления глюкозы. Анаэробный гликолиз глюкозы в цитозоле осуществляется с образованием двух молекул АТФ и двух молекул пировиноградной кислоты. В случае недостатка кислорода в клетке пировиноградная кислота превращается в лактат, а в присутствии кислорода – в пируват, который поступает в митохондрии до полного окисления в виде воды и углекислого газа [11].
Процесс образования АТФ является кислородосберегающим по сравнению с бета-окислением жирных кислот, что обеспечивает необходимое количество АТФ для энергетических затрат сердца. Влияние Милдроната не сопровождается возрастанием в митохондриях концентрации недоокисленных, промежуточных продуктов метаболизма свободных жирных кислот, предшествующих их бета-окислению, которые, в свою очередь, могут служить источником образования токсических липопероксидов в результате активации свободно-радикальных процессов при ишемии и реперфузии миокарда [12]. Высокии? уровень свободных радикалов оказывает негативное воздействие, активируя процессы гиперкоагуляции, ингибируя синтез оксида азота, уменьшая чувствительность оксида азота и барорецепторов сосудистои? стенки.
Милдронат, помимо активации митохондриального аэробного окисления глюкозы, подавления синтеза карнитина, приводит к накоплению гамма-бутиробетаина, способного стимулировать ацетилхолиновые рецепторы. В результате повышается синтез оксида азота, что объясняет вазопротективный и антиоксидантный эффект препарата [13]. Известно, что под влиянием Милдроната в эритроцитах усиливается синтез 2,3-бисфосфоглицерата, молекулы которого связываются с бета-цепями гемоглобина и снижают его сродство к кислороду, таким образом улучшая в тканях процесс освобождения кислорода из гемоглобина и повышение его уровня в тканях. Предшественник карнитина гамма-бутиробетаин оказывает вазодилатирующее деи?ствие и улучшает микроциркуляцию в тканях [14].
Пролапс митрального клапана относится к распространенным проявлениям наследственных нарушений соединительной ткани (ННСТ). Пролабирование створки (-ок) митрального клапана встречается как признак системного вовлечения при многих моногенных (синдром Марфана, Элерса – Данло и др.) и многофакторных нарушениях соединительной ткани или как самостоятельный синдром – первичный ПМК [15]. В популяции по результатам ЭхоКГ-исследования первичный ПМК встречается с частотой 2–3%, при аутопсии – 8% [16, 17]. Основные клинические признаки ПМК – вегетативная дисфункция, ортостатическая недостаточность, артериальная гипотензия, аритмии сердца, нарушения реполяризации желудочков на ЭКГ [18].
У лиц с ПМК системное вовлечение соединительной ткани проявляется гемодинамическими особенностями вследствие изменений внеклеточного матрикса миокарда и стенок сосудов, нарушений микроциркуляции миокарда и вегетативной дисфункции, обусловливающими повышенное потребление кислорода тканями [8, 14]. Вместе с тем при ННСТ отмечается генетически детерминированное снижение способности клеток извлекать из крови кислород. Тканевая гипоксия и вторичная митохондриальная недостаточность, по мнению исследователей, характерна при ННСТ для клеток головного мозга и миокарда [6]. Чаще при физической нагрузке, чем в покое, у молодых людей с ПМК отмечают снижение кислородного обеспечения миокарда, появление ишемических изменений, что при выполнении велоэргометрии регистрируется на ЭКГ в виде инверсии зубца Т в грудных отведениях [7, 8]. Метаболические расстройства усугубляются в результате дисфункции вегетативной нервной системы, преобладающего влияния симпатического и недостаточного обеспечения деятельности сердца парасимпатическим отделом. На фоне повышенного потребления кислорода и энергозатрат создаются условия для энергетического истощения клеток миокарда с последующим развитием фиброза и сердечной недостаточности.
Известно, что при ННСТ, помимо структурных изменений сосудистой стенки, определяют расстройство вазоактивной функции эндотелия, усугубляющей прогрессирование развития фиброза и нарушения деятельности сердца [19, 20]. Исследования, выполненные с участием пациентов с ХСН, получающих ингибиторы АПФ и ?-адреноблокаторы, показали, что после лечения Милдронатом наблюдается улучшение или нормализация эндотелий-зависимого ответа плечевой артерии [21].
Таким образом, у пациентов с ПМК патогенетически обоснованным является применение Милдроната – цитопротектора и антиоксиданта, обладающего способностью улучшать функциональное состояние сердечно-сосудистой системы, эндотелия и периферической скелетной мускулатуры, уменьшать вегетативный дисбаланс за счет улучшения энергетического внутриклеточного обмена.
Материалы и методы
В наблюдении участвовали 89 пациентов (82 мужчины и 7 женщин) в возрасте 18–32 лет (20,7±3,8 года) с ПМК и системным вовлечением соединительной ткани. Критерии включения: возраст 18–35 лет; наличие признаков многофакторных ННСТ с ПМК; информированное согласие на исследование.
К критериям исключения отнесли наличие острых или обострения хронических заболеваний внутренних органов, врожденные и приобретенные пороки сердца, воспалительные заболевания сердца в настоящее время или по анамнестическим данным, заболевания щитовидной железы и клинически манифестирующие заболевания других эндокринных желез, психические заболевания и болезни центральной нервной системы, онкологические заболевания, неполучение согласия на исследование.
В наблюдении участвовали пациенты, направленные районными военкоматами на обследование в кардиологическое отделение 9-й городской клинической больницы, Минский консультационно-диагностический центр или обратившиеся самостоятельно.
Комплексное обследование включало результаты анамнеза, наследственной отягощенности по ННСТ и сердечно-сосудистым заболеваниям, антропометрии, физического развития, фенотипа, физикального обследования.
Анализировали результаты инструментальных методов: рентгенографии органов грудной клетки, электрокардио-графии (ЭКГ) в 12 стандартных отведениях, суточного мониторирования ЭКГ, эхокардиографии (ЭхоКГ), нагрузочных проб (тредмила, велоэргометрии), ультразвукового исследования (УЗИ) органов брюшной полости, почек, щитовидной железы. Выполняли рутинные лабораторные методы исследования, определяли уровень гормонов щитовидной железы. Вазоактивную функцию эндотелия оценивали по модифицированной методике D.S. Celermaier и соавт., нормальной считали функцию эндотелия при увеличении диаметра плечевой артерии на 9–13%, другие показатели рассматривали как патологические: <9% считали сниженной, >13% – повышенной функцией эндотелия.
Субъективную оценку переносимости препарата оценивали по визуальной аналоговой шкале (ВАШ) от 0 до 10 баллов.
Продолжительность исследования составила 2 месяца (апрель – ноябрь 2015 г.), кратность исследования исходно, через 2 месяца. Участники наблюдения получали Милдронат 500 мг 2 раза в сутки в течение 8 недель и поливитамины.
У 12 пациентов (мужчин – 5, женщин – 7) наблюдение продолжалось в течение 36 месяцев (с января 2013 г. по декабрь 2015 г.) с интервалами между амбулаторными визитами 6 месяцев. Лечение Милдронатом по 500 мг 2 раза в сутки в течение 8 недель пациенты получали 2 раза в год (через каждые 6 месяцев) в течение 36 месяцев.
Наблюдение выполнили в соответствии со стандартами надлежащей клинической практики (Good Clinical Practive) и принципами Хельсинской декларации. Дизайн наблюдения представлен на рис. 1.
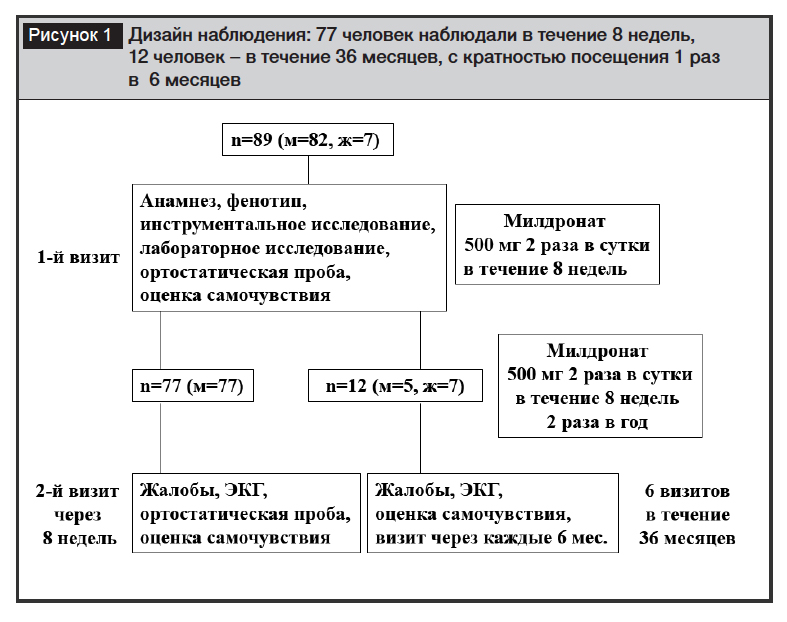
Статистический анализ выполнен в программе анализа данных AtteStat (13.1). Нормальность распределения признаков оценивали по критерию Shapiro – Wilk, достоверность различий – по Student при нормальном распределении и по Mann – Whitney при распределении, отличном от нормального. Уровень значимости p=0,05.
Результаты и обсуждение
Субъективные ощущения исследуемых пациентов включали жалобы на боль в левой половине грудной клетки (71,9%), сердцебиение (17,9%), головную боль физического напряжения (38,2%), потливость ладоней и стоп (71,9%), парестезии в кистях и стопах (23,6%), слабость, утомляемость (68,5%). На плохую переносимость умеренных физических нагрузок жаловались 90% пациентов. Средняя оценка самочувствия по ВАШ составила 4,6 баллов.
Наследственный анамнез с указаниями на ПМК, сердечно-сосудистые заболевания и события имели 38,2% пациентов. На момент включения в исследование курящих пациентов было 3,4% (3 мужчин), среднее число выкуриваемых сигарет – 10,4±2,7, продолжительность курения – 3,5±1,8 лет.
При физикальном исследовании частота сердечных сокращений составила 76,5 ударов в минуту (Ме 76,3; Q25:75 64–82), артериальное давление (АД) – 108±5,2/82±5,1 мм рт. ст.
При оценке фенотипа в среднем выявили 11 признаков дисморфогенеза, в том числе изменения кожи – у 89,9%, ушных раковин – у 71,9%, глаз – у 48,3%, носа – у 56,2%, ротовой полости – у 71,9%, грудной клетки – у 86,5%, С- или S-образный сколиоз грудного отдела позвоночника – у 84,3%, поперечное плоскостопие – у 86,5%, гипермобильность суставов – у 23,6% (в среднем 3,8 балла), расширение подкожных вен нижних конечностей – у 7,9%. Висцеральные признаки ННСТ включали изогнутый желчный пузырь (5,6%), нефроптоз правой почки 1-й степени без нарушений уродинамики (5,6%).
При ЭхоКГ-исследовании, помимо ПМК I степени (100%) с минимальной регургитацией (48,3%) и без миксоматоза, выявили аномально расположенные хорды у 71,9%, пролабирование створок трикуспидального клапана – у 38,2%, другие гемодинамически незначимые аномалии – у 17,9%. Единичные аномалии встречали у 26%, множественные (2–4) – у 74%.
Антропометрические показатели: рост – 182,4 см (95% ДИ 181,0–183,7 см), средняя масса тела – 72,4 кг (95% ДИ 71,3–75,2 кг), средний индекс массы тела – 19,3 кг/м2 (95% ДИ 19,2–23,1 кг/м2).
При ЭхоКГ-исследовании морфометрические и гемодинамические показатели пациентов не превышали нормальные значения (таблица).
Ультразвуковые морфометрические и гемодинамические показатели пациентов на первом визите
|
Показатели
|
ННСТ (n=77)
|
|
Аорта, мм
|
Ме 28 (95% ДИ 27–29)
|
|
Диаметр аорты на уровне клапана, мм
|
Ме 28 (95% ДИ 27–29)
|
|
Дуга аорты, мм
|
Ме 25,9 (95% ДИ 25–26)
|
|
Нисходящая аорта, мм
|
Ме 20 (95% ДИ 19–20)
|
|
Левое предсердие, мм
|
Ме 32 (95% ДИ 31–33)
|
|
Толщина межжелудочковой перегородки в диастолу, мм
|
Ме 10 (95% ДИ 9–10)
|
|
Толщина межжелудочковой перегородки в систолу, мм
|
Ме 14 (95% ДИ 13–14)
|
|
Толщина задней стенки левого желудочка в диастолу, мм
|
Ме 9 (95% ДИ 8–9)
|
|
Толщина задней стенки левого желудочка в систолу, мм
|
Ме 15 (95% ДИ 15–15)
|
|
Конечный диастолический объем, мл
|
115±2,02 (95% ДИ 111,5–119,6)
|
|
Конечный систолический объем, мл
|
Ме 37 (95% ДИ 34–38)
|
|
Ударный объем, мл
|
77,3±1,52 (95% ДИ 75,3–81,3)
|
|
Фракция выброса, %
|
Ме 67 (95% ДИ 66–69)
|
|
Правый желудочек, мм
|
Ме 22 (95% ДИ 21–22,6)
|
|
Индекс массы тела, кг/м2
|
87,6±2,38 (95% ДИ 83,3–92,9)
|
|
Давление в легочной артерии, мм рт. ст.
|
Ме 13 (95% ДИ 12,9–14)
|
По ЭКГ-данным у большинства пациентов регистрировали синусовый ритм (71,9%), у остальных – дыхательную аритмию (5,6%), миграцию водителя ритма по предсердиям (ВР) (13,5%) синусовую брадикардию (9%). Нарушения ритма и проводимости на ЭКГ в 12 стандартных отведениях включали наджелудочковую (10,1%) и желудочковую экстрасистолию (3,4%), атриовентрикулярную блокаду I степени (2,24%), полную и неполную блокаду правой ножки пучка Гиса (1,1%), синдром CLC (4,5%), синдром ранней реполяризации желудочков (СРРЖ) (25,8%).
Нарушения метаболизма миокарда проявлялись в виде изменения конечной части желудочкового комплекса – косонисходящее смещение сегмента ST (не более 1,5 мм) и зубца Т (инверсия или снижение вольтажа), которые регистрировали в 20,2% случаев.
При суточном мониторировании ЭКГ аритмии сердца выявляли часто по сравнению с ЭКГ в 12 стандартных отведениях: синусовая тахикардия и брадикардия, наджелудочковая и желудочковая экстрасистолия, синоатриальная блокада и атрио-вентрикулярная блокада (в 2 случаях 2-й степени) на фоне брадикардии, эпизоды миграции ритма по предсердиям, нарушения реполяризации желудочков. Метаболические нарушения выявили чаще, чем при исследовании ЭКГ в 12 стандартных отведениях – в 31,5% случаев.
Результаты велоэргометрической пробы указывали на хорошую физическую работоспособность и в 71,9% случаев высокую толерантность к физической нагрузке. Физиологическую реакцию АД во время физической нагрузки зарегистрировали у 78,7%, гипертензивную реакци – у 12,4%, дистоническую реакцию – у 8,9% пациентов.
По результатам пробы с реактивной гиперемией нарушение функционального состояния эндотелия выявлено в 71,9% случаев, в виде недостаточной – в 53,4% или избыточной – в 16,9% вазодилатации.
После 8-недельного лечения. Милдронатом на 2 визите отметили улучшение состояния практически все пациенты (n=77). Не зарегистрировано отказов от приема Милдроната и неявки на визит.
Динамика жалоб и основных клинических проявлений представлена на рис. 2. Результаты наблюдения указывали на уменьшение доли пациентов, испытывающих кардиалгии, сердцебиение, парестезии в стопах и кистях рук, головную боль, потливость ладоней и стоп, слабость.
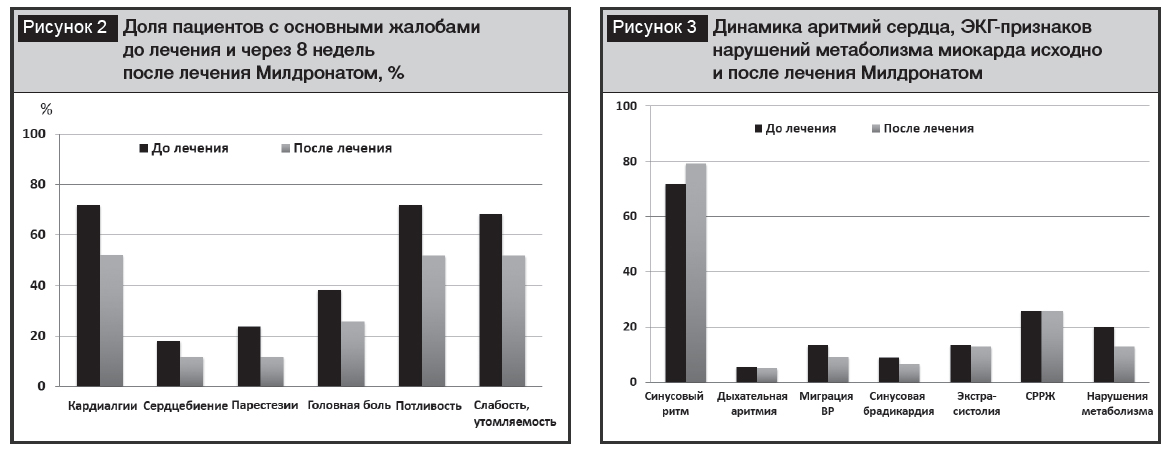
Согласно оценке самочувствия по ВАШ из 77 пациентов 17 отметили самочувствие как хорошее (9 баллов), остальные – как хорошее или значительное улучшение (6–8 баллов). Средний балл составил 7,2, превысив исходный в 1,5 раза.
Положительное влияние лечения Милдронатом на метаболизм миокарда отметили при анализе ЭКГ. Изменения сегмента ST и зубца Т регистрировали реже (13%) по сравнению с исходной ЭКГ. Аритмии сердца после лечения Милдронатом наблюдали реже на ЭКГ в 12 стандартных отведениях (рис. 3).
Таким образом, при краткосрочном наблюдении и лечении Милдронатом пациентов с ПМК отмечается улучшение субъективного состояния по снижению доли жалоб, предъявляемых до лечения, и результатам ВАШ. Улучшение метаболического и энергетического состояния миокарда, функции эндотелия сосудов подтверждали не только субъективные признаки, но результаты ЭКГ, свидетельствующие о снижении частоты аритмий сердца, уменьшении доли пациентов с изменениями конечной части желудочкового комплекса на ЭКГ.
Нежелательных реакций на фоне приема Милдроната не отмечено за 8 недель лечения.
Долгосрочное наблюдение 12 пациентов, получавших регулярно 2 раза в год по 8 недель Милдронат, показало значительное улучшение самочувствия. Через 36 месяцев оценка по ВАШ указывалась пациентами не ниже 8 баллов. Эпизоды кардиалгий, сердцебиения, головной боли, мышечной слабости, утомляемости возникали реже по сравнению с исходными проявлениями. Пациенты отметили повышение работоспособности, переносимости физических и интеллектуальных нагрузок, улучшение настроения. Доказательством хорошей переносимости и безопасности препарата, отсутствия побочных реакций явилась длительная приверженность к лечению.
Результаты инструментальных исследований, выполненных в разные сроки (через 12, 24, 28, 36 месяцев) на фоне лечения Милдронатом, показали по сравнению с исходными показателями повышение физической работоспособности и уменьшение гипертензивной, отсутствие дистонической реакции АД на физическую нагрузку при ВЭМ, нормализацию ритма на ЭКГ в 12 стандартных отведениях (отсутствие экстрасистолии, синусовой бради- и тахикардии, миграции водителя ритма по предсердиям). Число пациентов с изменениями конечной части желудочкового комплекса снизилось с 5 до 2.
Заключение
Субъективные и объективные данные, позволяющие оценивать результаты применения препарата у лиц с ПМК и системным вовлечением соединительной ткани, указывают на эффективность Милдроната при краткосрочном в течение 2 месяцев и долгосрочном в течение 36 месяцев лечении. За счет коррекции метаболических расстройств, нормализации микроциркуляции и функции эндотелия улучшаются электрофизиологические свойства миокарда, снижается частота регистрируемых аритмий сердца и эпизодов нарушения реполяризации желудочков. В связи с уменьшением клеточного энергодефицита повышается адаптация к физической нагрузке. Нормализующее влияние Милдроната на дисбаланс вегетативной нервной системы, периферическую мускулатуру во многом обусловливают повышение физической работоспособности и оценки состояния здоровья.
В связи со значительной распространенностью ННСТ среди людей молодого возраста, системностью расстройств, прогрессирующим течением и развитием ассоциированных заболеваний особую важность приобретает патогенетическое лечение Милдронатом, обладающим универсальностью действия.
Л И Т Е Р А Т У Р А
1. Liepinsh, E. Mildronate treatment alters ?-butyrobetaine and l-carnitine concentrations in healthy volunteers / E. Liepinsh, I. Konrade, E. Skapare [et al.] // J. Pharm. Pharmacol. – 2011. – Vol. 63 (9). – P.1195–1201.
2. Дзерве, В.Я. Динамика толерантности к физической нагрузке у пациентов с ишемической болезнью сердца и периферической болезнью артерий на фоне длительной терапии Mилдронатом / В.Я. Дзерве, Ю.М. Поздняков // Рос. кард. журнал. – 2011. – №1. – С.49–55.
3. Драпкина, О.М. Новые способы оптимизации противоишемической терапии / О.М. Драпкина, Е.И. Козлова // Рос. кард. журнал. – 2010. – №1. – С.82–84.
4. Гейченко, В.П. Эндотелиальная дисфункция при сердечной недостаточности с сохраненной систолической функцией и ее коррекция препаратом метаболического ряда Mилдронатом / В.П. Гейченко, А.В. Курята, О.В. Мужчиль // Рос. кард. журнал. – 2005. – №4. – С.68–71.
5. Sjakste, N. Mildronate: an antiischemic drug with multiple indications / N. Sjakste, I. Kalvinsh // Pharmacology- on line. – 2006. – Vol.1. – P.1–18.
6. Кадурина, Т.И. Дисплазия соединительной ткани. Руководство для врачей / Т.И. Кадурина, В.Н. Горбунова. – М.: ЭЛБИ,2009. – 714 с.
7. Дубилей, Г.С. Клиническая эффективность Милдроната у лиц с дисплазией соединительной ткани: опыт терапии в условиях специализированного центра г. Омска / Г.С. Дубилей, Г.И. Нечаева, И.В. Друк [и др.] // Рос. кард. журнал. – 2011. – №3. – С.55–57.
8. Земцовский, Э.В. Диспластические синдромы и фенотипы. Диспластическое сердце / Э.В. Земцовский. – СПб.: Ольга, 2007. – 80 с.
9. Дзерве, В.Я. Милдронат в кардиологии / В.Я. Дзерве, И.Я. Калвиньш. – Рига: Grindex, 2013. – 74 с.
10. Dambrova, M. Mildronate: cardioprotective action through carnitine-lowering effect / M. Dambrova, E. Liepinsh, I. Kalvinsh // Trends Cardiovasc. Med. – 2002. – Vol.12. – P.275–279.
11. Михин, В.П.Милдронатвкардиологическои?практике – итоги, новыенаправления, перспективы / В.П. Михин, Ю.М. Поздняков, Ф.Е. Хлеболаров [идр.] // Кардиоваскулярнаятер. ипроф. – 2012. – №11 (1). – С.95–102.
12. Vitols, A. Mildronate improves carotid baroreceptor reflex function in patients with chronic heart failure / A. Vitols, D. Voita, V. Dzerve // Seminars in Cardiovascular Medicine. – 2007. – Vol.13. – P.6.
13. Воронков, Л.Г. Влияние Mилдронатанаэндотелии?-зависимуювазодилатациюубольныххроническои?сердечнои?недостаточностью: двои?ноеслепоеперекрестноеисследование / Л.Г. Воронков, И.А. Шкурат, Е.А. Луцак // Рац. фармакотер. вкард. – 2008. – №2. – С.38–40.
14. Белоусов, Ю.Б.Клиническаяфармакологияифармакотерапия: рук. дляврачеи?. 2-еизд. / Ю.Б. Белоусов, В.С. Моисеев, В.К. Лепахин. – М.: УниверсумПаблишинг, 2000. – 539 с.
15. Freed, L.A. Prevalence and clinical outcome of mitral-valve prolapse / L.A. Freed, D. Levy, R.A. Levine, M.G. Larson, J.C. Evans, D.L. Fuller, B. Lehman, E.J. Benjamin // N. Engl. J. Med. – 1999. – Vol.341. – P.1–72.
16. Vahanian, A. Guidelines on the management of valvular heart disease (version 2012) / A. Vahanian, O. Alfieri, F. Andreotti [et al.] // Eur. Heart. J. – 2012. – Vol.33. – P.2451–2496.
17. Трисветова, Е.Л. Анатомиямалыханомалийсердца / Е.Л. Трисветова, О.А. Юдина. – Минск: Белпринт, 2006. – 104 с.
18. Delling, F.N. Epidemiology and pathophysiology of mitral valve prolapse: new insights into disease progression, genetics, and molecular basis / F.N. Delling, R.S. Vasan // Circulation. – 2014. – Vol.129. – P.2158–2170.
19. Трисветова, Е.Л.Особенностисосудодвигательнойфункцииэндотелияумужчинмолодоговозраста / Е.Л. Трисветова, Н.М. Вараницкая, Р.Ф. Ермолкевич // Дисфункцияэндотелия: экспериментальныеиклиническиеисследования. Труды V международнойнаучно-практ. конф., 22–23 мая 2008 г. – Витебск: ВГМУ, 2008. – С.217–220.
20. Трисветова, Е.Л.Особенностиэндотелиальнойфункциипорезультатампробысреактивнойгиперемиейумужчинпризывноговозрастаснаследственныминарушениямисоединительнойткани / Е.Л. Трисветова, О.А. Паторская, Н.В. Томчик; отв. ред. В.В. Зинчук // Вопросыэкспериментальнои?иклиническои?физиологии: сборникнаучныхтрудов, посвященныи? 100-летиюсоднярожденияАринчинаНиколаяИвановича. – Гродно: ГрГМУ, 2014. – С.301–304.
21. Михин, В.П.ПерспективыпримененияМилдронатаубольныхссердечно-сосудистои?патологиеи? / В.П. Михин, Ф.Е. Хлебодаров // Рос. кард. журнал. – 2010. – №84 (4). – С.158–168.
Медицинскиеновости. – 2016. – №2. – С. 34-38.
Внимание! Статья адресована врачам-специалистам. Перепечатка данной статьи или её фрагментов в Интернете без гиперссылки на первоисточник рассматривается как нарушение авторских прав.