Kozhanova I.N.1, Romanova I.S.1, Gavrilenko L.N.1, Sachek M.M.2
1Belarusian State Medical University, Minsk
2Republican Center of Medical Technology, Information Technology, Management and Economics Health Care, Minsk
Pharmacoeconomic analysis of the ciclesonide use
in health care system of Republic of Belarus
Резюме. На основании систематического исследования с включением национальных эпидемиологических и статистических данных, перечня лечебных процедур и вмешательств, соответствующих Клиническому протоколу диагностики и лечения бронхиальной астмы, проведен фармакоэкономический анализ «затраты/эффективность» применения циклесонида (Альвеско®) в условиях системы здравоохранения Респуб-лики Беларусь. С учетом различных сценариев течения заболевания проведен анализ чувствительности, детерминированный по стоимости циклесонида и степени тяжести обострений бронхиальной астмы. С позиции фармакоэкономики, научно обосновано место циклесонида (Альвеско®) в терапии бронхиальной астмы в условиях системы здравоохранения Республики Беларусь.
Ключевые слова: фармакоэкономика, циклесонид, бронхиальная астма, анализ «затраты/эффективность».
Медицинские новости. – 2015. – №10. – С. 76–80.
Summary. Pharmacoeconomic cost-effectiveness analysis of the ciclesonide use in health care system of Republic of Belarus has been performed according to the national epidemiological and statistical data, national asthma guidelines and results of clinical. Sensitivity analysis determined by the cost of ciclesonide and severity of exacerbations of asthma has been made. The place of ciclesonide (Alvesko®) in the treatment of asthma in the health care system of Republic of Belarus has been established.
Keywords: pharmacoeconomics, ciclesonide, asthma, cost-effectiveness analysis.
Meditsinskie novosti. – 2015. – N10. – P. 76–80.
Последние десятилетия ХХ века принесли значительные успехи в лечении бронхиальной астмы (БА). Национальные стандарты лечения БА базируются на международном руководстве (GINA – Глобальная стратегия по лечению и профилактике БА), объединяющем рекомендации ведущих мировых организаций (The National Heart, Lung and Blood Institute, The National Institutes for Health и др.), специалистов ВОЗ. Руководство GINA предусматривает ступенчатый подход к терапии с разделением лекарств на средства базисной терапии и скорой помощи, а также с выделением ключевых групп препаратов, использование которых по отдельности или в виде комбинаций с последовательным усилением терапии позволяет контролировать заболевание [21]. Цель ступенчатого подхода состоит в достижении контроля астмы с применением наименьшего количества препаратов. Согласно руководству GINA, основой терапии БА являются ингаляционные глюкокортикостероиды (ИГКС). Современные ИГКС должны отличаться высокой противовоспалительной эффективностью и системной безопасностью.
В Республике Беларусь с 2011 г. зарегистрирован препарат нового поколения для лечения БА ? циклесонид (Альвеско®) [1, 4, 12]. Уникальными особенностями циклесонида являются высокий уровень депонирования в легких и распределения в мелких дыхательных путях, что определяет его эффективное лечебное воздействие [4, 18, 28, 32]. Появление возможности использования при лечении БА нового ИГКС требует не только клинического, но и экономического определения его позиции на национальном фармацевтическом рынке и в клинической практике.
Целью настоящего исследования является фармакоэкономическая оценка целесообразности применения циклесонида у пациентов с БА в условиях системы здравоохранения Республики Беларусь. Работа выполнена в соответствии с инструкцией по применению «Порядок проведения клинико-экономических исследований», утвержденной Министерством здравоохранения Республики Беларусь 03.10.2008 г., регистрационный номер 075-0708.
Перечень ИГКС, рекомендуемых международными клиническими руководствами для лечения БА, включает беклометазона дипропионат, будесонид, флутиказона пропионат, флунизолид, триамсинолона ацетонид, мометазона фуроат и циклесонид, выпускаемые в виде дозированных аэрозольных ингаляторов, сухой пудры с соответствующими ингаляторами для их использования (турбухалер, циклохалер и др.), а также в виде растворов или суспензий для применения с помощью небулайзеров [6, 7, 21]. Указанные ИГКС различаются по фармакологической активности и биодоступности. В международных, российских и белорусских клинических рекомендациях, основанных на результатах оценки эффективности различных вариантов лечения в условиях контролируемых клинических испытаний, применяемые в клинической практике ИГКС рассматриваются как терапевтически эквивалентные [21, 30].
Особенностью циклесонида является его фармакокинетический профиль, позволяющий применять препарат один раз в сутки при любой степени тяжести БА [1, 4, 18]. Этот факт может способствовать повышению приверженности пациентов с БА к лечению и увеличению эффективности терапии [11, 13, 17, 35, 42]. Для оценки клинической эффективности циклесонида в условиях реальной клинической практики с учетом влияния кратности применения ИГКС на приверженность пациентов с БА к лечению был проведен систематический библиографический поиск по базам данных MEDLINE (с 1966 г. до апреля 2013 г.), Cochrane Database of Systematic Reviews, Cochrane Central Register of Controlled Trials и Database of Abstracts of Reviews of Effects (апрель 2013 г.). Использовали следующие ключевые слова: inhaled corticosteroids, adherence, compliance, сiclesonide, fluticasone, budesonide, triamcinolone, flunisolide, beclomethasone, controlled clinical trial. Дополнительно проведен поиск в библио-графиях медицинских журналов Thorax, The American Journal of Managed Care, British Medical Journal, The New England Journal of Medicine, Фарматека, РМЖ, Consilium-medicum, Pharmacoeconomics Journal of Managed Care Pharmacy, The Journal of American Medical Association, а также материалах конгрессов ISPOR по ссылкам, полученным при анализе публикаций, отобранных при первоначальном поиске. Также осуществлен поиск по общим и специализированным электронным источникам: US Food and Drug Administration, NICE, The European Medicines Agency.
В исследовании оценивали только прямые медицинские затраты, учитывали стоимость лекарственных средств, диагностических процедур (лабораторных и инструментальных), госпитализации, вызова бригады скорой медицинской помощи. Перечень анализируемых лечебных процедур и вмешательств, включающих лечение обострения и терапию БА в межприступный период, соответствовал национальным Клиническим протоколам диагностики и лечения БА [6, 7]. Поиск информации о стоимости медицинских услуг у взрослых и детей (консультации специалистов, клинические лабораторные и диагностические исследования) проводили систематическим образом в общедоступных интернет-источниках Республики Беларусь по запросу: прейскурант, лабораторные исследования, диагностические процедуры, стоимость госпитализации в детский и взрослый стационары по состоянию на апрель – август 2013 г. Поскольку стоимость медицинских услуг для взрослых и детей старше 5 лет сопоставима, а протоколы лечения заболевания для этих групп населения сходны, проведен общий фармакоэкономический анализ для этих возрастных категорий с учетом применения для базисной терапии средних доз ИГКС [6, 7]. Анализ стоимости лекарственных средств осуществляли путем систематического поиска в электронных ресурсах и базе данных «Фармасервис» по состоянию на апрель – август 2013 г. и 2015 г.
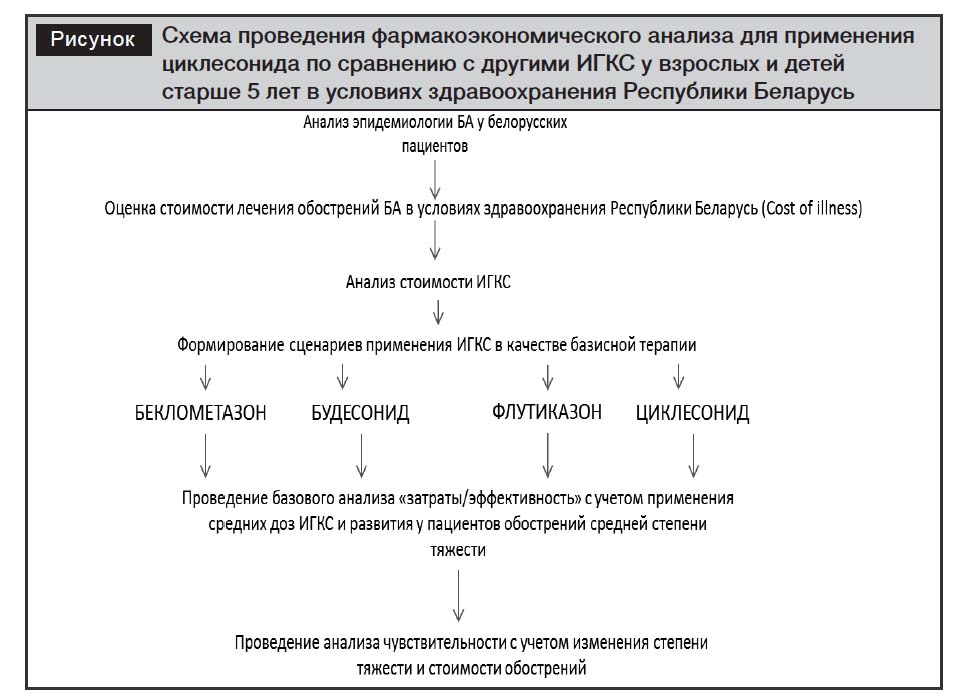
В качестве критерия эффективности лекарственных средств принимали вероятность развития обострения БА различной степени тяжести. Применяли метод фармакоэкономического анализа «затраты/эффективность» с оценкой инкрементального коэффициента приращения затрат (ICER), а также анализ «стоимость болезни» [5, 8]. Все расчеты проведены на модели течения БА, построенной с использованием национальных эпидемиологических данных. Базовый фармакоэкономический анализ проведен для сценария, при котором пациент получает базисную терапию средними дозами ИГКС, а все перенесенные обострения – средней степени тяжести. Сформирован ряд стоимостных сценариев применения разных ИГКС (беклометазона, будесонида, флутиказона, циклесонида) в условиях здравоохранения Республики Беларусь (рисунок).
Все финансовые расчеты проведены по состоянию на апрель – август 2013 г. при следующих курсах валют: 1 доллар США равен 8 890 бел. рублей, 1 Евро – 11 820 бел. рублей, 1 российский рубль – 269 бел. рублей. Выбранный горизонт исследования составил 1 год. Дисконтирование не осуществляли.
Проведен многосторонний детерминированный анализ чувствительности с исследованием влияния на итоговые фармакоэкономические оценки величины затрат на терапию нежелательных событий, развивающихся у пациентов с БА (обострения, госпитализации, обращения за неотложной помощью). При проведении анализа чувствительности были сформированы блоки анализа и сценариев развития событий в соответствии с результатами анализа литературных источников и эпидемиологической базой данных белорусских пациентов с БА.
Блок 1: допущение о том, что при увеличении приверженности на 10% (с 69% при двукратном назначении препарата до 79% – при однократном) число всех обострений уменьшится на 9,76% [9].
Блок 2: допущение о том, что при увеличении приверженности на 10% (с 69% при двукратном назначении препарата до 79% – при однократном) число обострений, закончившихся госпитализацией (как наиболее объективный критерий наличия события), уменьшится на 9,76% [9].
Блок 3: допущение о том, что при увеличении приверженности на 10% (с 69% при двукратном назначении препарата до 79% – при однократном) число обострений, закончившихся госпитализацией (как наиболее объективный критерий наличия события), уменьшится в 1,44 раза [42].
Сценарии анализа чувствительности:
А – все перенесенные обострения легкой степени тяжести;
В – все перенесенные обострения средней степени тяжести;
С – все перенесенные обострения тяжелой степени тяжести;
D – в качестве стоимости обострения принято значение средней возможной стоимости (легкого, среднего, тяжелого обострения) без учета вероятности наступления события;
E – в качестве стоимости обострения принято значение средней возможной стоимости (легкого, среднего, тяжелого обострения) с учетом вероятности наступления события;
F – в качестве стоимости госпитализации принято минимальное значение;
G – в качестве стоимости госпитализации принято максимальное значение;
H – в качестве стоимости госпитализации принято среднее значение.
С целью актуализации полученных данных проведен дополнительный анализ чувствительности с учетом изменившихся уровней стоимости на медицинские услуги и лекарственные средства по состоянию на май – июнь 2015 г.
Результаты и обсуждение
В основе данного фармакоэкономического анализа лежит парадигма об увеличении эффективности лечения БА при повышении приверженности к применению лекарственных средств в условиях реальной клинической практики. Для подтверждения и количественного измерения этой зависимости в результате проведенного систематического анализа литературы обнаружены публикации, изучающие и анализирующие взаимосвязь приверженности (adherence, compliance) и эффективности фармакотерапии БА [11, 13, 17, 35, 42].
По данным фармакоэкономического исследования А.В. Рудаковой и соавт., средняя приверженность к терапии ИГКС, применяемым один раз в сутки, составила 79% и снижалась до 69% в случае необходимости двукратного использования, хотя различия не достигли уровня статистической значимости [6]. Анализ одно- и двукратного режима применения мометазона фуроата показал, что приверженность к лечению при увеличении частоты использования препарата снижалась на 3,8–4,6% [35]. Сравнение приверженности пациентов к лечению при применении мометазона фуроата, назначаемого 1 раз в сутки, и беклометазона, назначаемого 2 раза в сутки, показало, что в первом случае показатель был выше на 9,3% [20]. Таким образом, при назначении ИГКС однократно приверженность к лечению выше на 9,3–10% по сравнению с показателем при применении лекарственных средств 2 раза в сутки. В качестве базового показателя приверженности к лечению в анализе принимали увеличение приверженности на 10%.
В исследовании L.K. Williams и соавт. было показано, что увеличение на 25% времени без поддерживающей терапии ИГКС влечет за собой повышение частоты обусловленных обострениями БА госпитализаций в 2,01 раза (95% ДИ 1,06–3,79) [42]. Позже было установлено, что отношение шансов вероятности обострения при тяжелой БА составляет 0,61 (0,41–0,9) для приверженных к терапии (принимающих более 75% назначенных доз) пациентов, а 24,4% обострений БА связаны с ненадлежащей приверженностью к терапии ИГКС [41].
Эти данные были использованы при создании модели течения БА у пациентов с разной степенью приверженности к фармакотерапии, связанной с кратностью назначения препарата. При условии линейного характера зависимости эффективности от приверженности к лечению было сделано допущение, что если при изменении приверженности на 25% происходит уменьшение общего числа обострений на 24,4%, то при изменении на 10% – на 9,76% (базовое значение). Для числа госпитализаций рассмотрены два варианта. При снижении числа обострений на 9,76% (при увеличении приверженности к лечению на 10%) вероятность развития обострения составит 0,272 [9]. Если при изменении приверженности на 25% происходит увеличение риска госпитализаций в 2,01 (1,06–3,79) раза, то при изменении на 10% – в 1,44 (1,024–2,116) раза. Таким образом, вероятность развития обострения составит 0,21 [42]. Если при изменении приверженности на 25% происходит увеличение риска обращений за неотложной помощью в 1,25 раза, то при изменении на 10% – в 1,1 [42].
Эпидемиологические данные о течении БА получены из электронной базы данных, созданной на основе опроса белорусских пациентов и медицинских работников (врачей) в 2010 г. в рамках выполнения НИР «Разработать научно-обоснованные рекомендации по совершенствованию системы медицинской помощи пациентам с бронхиальной астмой на основе информационных технологий», и представлены в табл. 1. В ходе исследования были опрошены более 600 врачей разных специальностей и проведена выкопировка медицинской документации более 470 пациентов с БА с фиксацией лекарственных средств и всех событий, происходящих с пациентом. Поскольку БА относится к заболеваниям, подлежащим льготному отпуску лекарственных средств, медицинская документация этой категории пациентов содержит исчерпывающую информацию о назначении и эффективности терапии (случаи обращения за неотложной медицинской помощью, госпитализации, коррекция лечения и т. д.).
Таблица 1. Базовые эпидемиологические данные о течении БА в Республике Беларусь (по результатам анализа электронной базы данных, составленной на основе опроса пациентов в 2010 г.) и модель расчета числа событий для 1000 пациентов
|
Показатель
|
Эпидемиологические данные
о течении БА
|
Модель для 1000 пациентов
|
|
Обострения БА
|
|
Доля пациентов с обострениями* (разной степени тяжести)
в течение 1 года
|
0,6
|
600
|
|
Доля пациентов без обострений
|
0,4
|
400
|
|
Медиана количества перенесенных обострений* (разной степени тяжести)
|
4,5
|
2700
|
|
Госпитализации по поводу БА
|
|
Доля пациентов, госпитализированных по поводу БА
в течение 1 года
|
0,302
|
302
|
|
Доля пациентов без госпитализации по поводу БА
|
0,698
|
698
|
|
Среднее число госпитализаций в течение года
|
2
|
603
|
|
Вызовы неотложной помощи
|
|
Доля пациентов, вызывавших бригаду скорой медицинской помощи
|
0,14
|
142
|
|
Доля пациентов, не обращавшихся за неотложной помощью
|
0,86
|
858
|
|
Медиана количества вызовов бригады скорой медицинской помощи
|
4,5
|
640
|
П р и м е ч а н и е : * под термином «обострение» понимается любая ситуация, требующая применения дополнительных лекарственных средств или внепланового обращения в организации здравоохранения за медицинской помощью.
Для проведения анализа «затраты/эффективность» была рассчитана средняя стоимость лечения ИГКС, зарегистрированными в Республике Беларусь на момент проведения исследования (табл. 2), а также минимальные, максимальные и средние значения затрат на лечение обострений БА разной степени тяжести с учетом возможности госпитализации (табл. 3).
Таблица 2. Стоимость терапии различными ИГКС
|
Препарат
|
Упаковка
|
Средняя розничная цена, бел.руб
|
Кратность применения в сутки
|
Стоимость, руб./сутки
|
Стоимость 1 года терапии, бел. руб.
|
|
Беклазон Эко Легкое Дыхание®
|
250 мкг
200 доз
|
105 200
|
2
|
1052
|
383 980
|
|
Будесонид интели®
|
200 мкг
200 доз
|
148 550
|
2
|
1485,5
|
542 208
|
|
Фликсотид®
|
125 мкг
60 доз
|
150 000
|
2
|
5000
|
1 825 000
|
|
Альвеско®
|
160 мкг
60 доз
|
301 125
|
1
|
5018,75
|
1 831 844
|
Таблица 3. Расчетная стоимость терапии обострений БА
|
Показатель
|
Стоимость терапии обострения БА, бел. руб.
|
|
мини-мальная
|
максимальная
|
средняя
|
|
Обострение легкой степени тяжести
|
508
|
227 875
|
83 412
|
|
Обострение средней степени тяжести
|
1 514 300
|
6 024 900
|
3 778 411
|
|
Обострение тяжелой степени тяжести
|
1 514 300
|
8 124 900
|
4 486 536
|
|
Обострение без учета вероятности наступления исхода
|
1 009 703
|
4 792 558
|
2 782 786
|
|
Обострение с учетом вероятности наступления исхода (тяжелого обострения – 0,223; обострения средней степени тяжести – 0,237, обострения легкой степени тяжести – 0,539)*
|
232 571
|
1 122 383
|
647 826
|
|
Госпитализация
|
1 514 300
|
8 124 900
|
4 132 474
|
П р и м е ч а н и е : * – значения получены в ходе анкетирования белорусских пациентов с БА.
Таблица 4. Базовый фармакоэкономический анализ «затраты/эффективность» применения ИГКС при лечении БА
|
Показатель
|
ИГКС
|
|
бекло-
метазон
|
будесонид
|
флутиказон
|
циклесонид
|
|
Затраты на ИГКС, бел. руб.
|
383 980
|
542 208
|
1 825 000
|
1 831 844
|
|
Стоимость терапии обострения, бел. руб.
|
3 778 411
|
3 778 411
|
3 778 411
|
3 778 411
|
|
Вероятность возникновения обострения
|
0,6000
|
0,6000
|
0,6000
|
0,5414
|
|
Затраты на терапию обострений, бел. руб.
|
2 267 047
|
2 267 047
|
2 267 047
|
2 045 783
|
|
Общие затраты на лечение БА
в течение 1 года, бел. руб.
|
2 651 027
|
2 809 254
|
4 092 047
|
3 877 627
|
|
Приращение затрат, бел. руб.
|
стоимость лечения циклесонидом – беклометазоном
|
стоимость лечения циклесонидом – будесонидом
|
стоимость лечения циклесонидом – флутиказоном
|
–
|
|
1 226 600
|
1 068 372
|
–214 420
|
П р и м е ч а н и е : представлен базовый сценарий, при котором пациент получает базисную терапию средними дозами ИГКС, все перенесенные обострения средней степени тяжести
Результаты базового фармакоэкономического анализа представлены в табл. 4. Применение циклесонида являлось доминирующей технологией по отношению к стратегии использования флутиказона, но не беклометазона и будесонида.
Проведенный анализ чувствительности подтвердил выявленное по итогам базового фармакоэкономического анализа доминирование технологии применения циклесонида над технологией использования флутиказона, за исключением сценария, при котором все обострения, развившиеся у пациента в течение года, – легкой степени тяжести. В этом случае дополнительные затраты при применении циклесонида по сравнению со стоимостью назначения флутиказона составят 1 959 бел. рублей в год, то есть данные стратегии являются практически сходными с позиций клинико-экономической эффективности. Во всех остальных случаях дополнительные и более значительные затраты потребуются для лечения с применением флутиказона (от 31 093 до 742 219 бел. рублей).
Актуализированный в 2015 г. анализ стоимостных показателей продемонстрировал тот факт, что цена оригинальных лекарственных препаратов, зависящая от курсов валют, изменилась значительнее, чем стоимость медицинских услуг, обусловленных в большей степени конкурентной средой и уровнем оплаты труда специалистов. Тем не менее полученные данные о возможной фармакоэкономической приемлемости применения циклесонида у пациентов с неудовлетворительным контролем БА и частыми обострениями тяжелой степени сохраняются. В этом случае снижение затрат на терапию одного пациента в течение года может составлять от 3 до 168 долларов США.
Исследование имеет методологические ограничения. Фармакоэкономический анализ проведен с учетом средней розничной стоимости лекарственных средств, применяемых в средних терапевтических дозах. Использованные в исследовании данные о взаимосвязи эффективности терапии БА и приверженности к применению ИГКС немногочисленны, что требует проведения дополнительных исследований, в том числе в Беларуси. Продемонстрирована чувствительность результатов к прямым затратам на приобретение ИГКС зарубежного производства. Вопросы фармакоэкономической оценки генерической замены различных ИГКС при лечении БА не являлись предметом рассмотрения в данном исследовании (циклесонид не имеет генерических аналогов на фармацевтическом рынке).
Проведенное исследование показало фармакоэкономические преимущества применения циклесонида по сравнению с использованием флутиказона у пациентов с обострениями БА средней и тяжелой степени тяжести, а также клинико-экономическую предпочтительность стратегии назначения циклесонида пациентам с неудовлетворительным контролем БА и частыми обострениями тяжелой степени. Полученные данные в сочетании с фармакокинетическими и фармакодинамическими особенностями циклесонида (мелкодисперсная лекарственная форма и высокая степень проникновения препарата в мелкие бронхи; низкая частота побочных эффектов, характерных для ИГКС) позволяют обосновать применение данного лекарственного препарата в качестве одного из альтернативных ИГКС в условиях системы здравоохранения Республики Беларусь.
Л И Т Е Р А Т У Р А
1. Айсанов З.Р., Калманова Е.Н., Стулова О.Ю. Циклесонид (Альвеско®) в лечении больных бронхиальной астмой // РМЖ. – 2012. – №6. – С.341–344.
2. Давидовская Е.И. Бронхиальная астма сегодня – проблемы и решения // Электронный ресурс: http://www.belmapo.by/page/5/355 (доступ 24.07.2013)
3. Дуболенко А.И. Региональные особенности заболеваемости взрослого населения Республики Беларусь // Белорусский медицинский журнал. – 2004. – №1. – С.43–45.
4. Инструкция по медицинскому применению препарата Альвеско. Согласовано Министерством здравоохранения Республики Беларусь. Приказ Министерства здравоохранения Республики Беларусь №1017 от 20.10.2011 г.
5. Клинико-экономический анализ (оценка, выбор медицинских технологий и управление качеством медицинской помощи) / П.А. Воробьев, М.В. Авксентьева, А.С. Юрьев, М.В. Сура. – М.: Издательство «Ньюдиамед», 2004. – 404 с.
6. Клинический протокол диагностики и лечения астмы. Приложение 3 к Приказу Министерства здравоохранения Республики Беларусь №768 от 05.07.2012 г.
7. Клинические протоколы диагностики и лечения аллергических заболеваний у детей. Приказ Министерства здравоохранения Республики Беларусь №829 от 08.08.2014 г.
8. Кожанова И.Н., Романова И.С., Хапалюк А.В., Степанова М.Д. Основы фармакоэпидемиологического и фармакоэкономического анализа использования лекарственных средств при хронических заболеваниях. – Мн.: БелМАПО, 2006. – 39 с.
9. Рудакова А.В. Фармакоэкономические аспекты поддерживающей терапии бронхиальной астмы ингаляционными кортикостероидами // Качественная клиническая практика. – 2013. – №1. – С.47–49.
10. Цой А.Н. Ингаляционные глюкокортикоиды: эффективность и безопасность // РМЖ. – 2001. – №9. – С.182–185.
11. Цой А.Н. Сравнительная фармакокинетика ингаляционных глюкокортикоидов // Аллергология. – 1999. – №3. – С.25–33.
12. Цой А.Н., Аржакова Л.С., Архипов В.В. Фармакодинамика и клиническая эффективность ингаляционных глюкокортикостероидов у больных с обострением бронхиальной астмы // Пульмонология. – 2002. – №3. – С.88.
13. Bailey W.C., Richards J.M. Jr., Brooks C.M. et al. A randomized trial to improve self management practices of adults with asthma // Arch. Intern. Med. – 1990. – Vol.150 (8). – P.1664–1668.
14. Braman S. The Global Burden of Asthma // Chest. – 2006. – N130. – 4S–12S.
15. Brown P.H., Greening A.P., Crompton G.K. Large volume spacer devices and the influence of high dose beclomethasone dipropionate on hypothalamo-pituitary-adrenal axis function // Thorax. – 1993. – Vol.48 (3). – P.233–238.
16. Buist S. Development of evidence for inhaled therapeutic interventions in asthma // Eur. Respir. Rev. – 1998. – Vol.8 (58). – P.322–323.
17. Claxton A.J., Cramer J., Pierce C. A systematic review of the associations between dose regimens and medication compliance // Clin. Ther. – 2001. – Vol.23 (8). – P.1296–1310.
18. Cohen J., Douma W.R., N.H.T. ten Hacken et al. Ciclesonide improves measures of small airway involvement in asthma // Eur. Respir. J. – 2008. – Vol.31. – Р.1213–1220.
19. Crompton G. A brief history of inhaled asthma therapy over the last fifty years // Primary Care Respiratory Journal. – 2006. – Vol.15. – Р.326–331.
20. Friedman H.S., Urdaneta E., McLaughlin J.M., Navaratnam P. Mometasone furoate versus beclomethasone dipropionate: effectiveness in patients with mild asthma // Am. J. Manag. Care. – 2010. – Vol.16 (7). – e151–156.
21. From the Global Strategy for Asthma Management and Prevention, Global Initiative for Asthma (GINA) 2015 // Available from: http://www.ginasthma.org.
22. Guevara J.P., Wolf F.M., Grum C.M., Clark N.M. Effects of education al interventions for self management of asthma in children and adolescents: systematic review and meta analysis // BMJ. – 2003. – Vol.326 (7402). – P.1308–1309.
23. Jayasiri B., Perera C. Successful withdrawal of inhaled corticosteroids in childhood asthma // Respirology. – 2005. – Vol.10. – P.385–388.
24. Jeffery P.K., Godfrey R.W., Adelroth E. et al. Effects of treatment on airway inflammation and thickening of basement membrane reticular collagen in asthma. A quantitative light and electron microscopic study // Am. Rev. Respir. Dis. – 1992. – Vol.145 (4 Pt 1). – P.890–899.
25. Juniper E.F., Kline P.A., Vanzieleghem M.A. et al. Effect of long-term treatment with an inhaled corticosteroid (budesonide) on airway hyper responsiveness and clinical asthma in nonsteroid-dependent asthmatics // Am. Rev. Respir. Dis. – 1990. – Vol.142 (4). – P.832–836.
26. Kohler C.L., Davies S.L., Bailey W.C. How to implement an asthma education program // Clin. Chest. Med. – 1995. – Vol.16 (4). – P.557–565.
27. Lai C., T. De Guia et al. Asthma control in the Asia-Pacific region: the Asthma Insights and Reality in Asia Pacific Study // J. Allergy Clin. Immunol. – 2003. – N111. – P.263–268.
28. Leach C.L. Improved delivery of inhaled steroids to the large and small airways // Respir. Med. – 1998. – Vol.92. Suppl. A. – Р.3–8.
29. Long-term effects of budesonide or nedocromil in children with asthma. The Childhood Asthma Management Program Research Group // N. Engl. J. Med. – 2000. – Vol.343 (15). – P.1054–1063.
30. Manning P., Gibson P.G., Lasserson T.J. Ciclesonide versus other inhaled steroids for chronic asthma in children and adults // Cochrane Database Syst. Rev. – 2008. – Vol.2. – CD007031.
31. Murphy V.E., Gibson P.G., Talbot P.I. et al. Asthma self management skills and the use of asthma education during pregnancy // Eur. Respir. J. – 2005. – Vol.26 (3). – P.435–441.
32. Nave R., Mueller H. From inhaler to lung: clinical implications of the formulations of ciclesonide and other inhaled corticosteroids // International Journal of General Medicine. – 2013. – Vol.6. – P.99–107.
33. Pauwels R.A., Lofdahl C.G., Postma D.S. et al. Effect of inhaled formoterol and budesonide on exacerbations of asthma. Formoterol and Corticosteroids Establishing Therapy (FACET) International Study Group // N. Engl. J. Med. – 1997. – Vol.337 (20). – P.1405–1411.
34. Pedersen S., O/Byrne P. A comparison of the efficacy and safety of inhaled corticosteroides in asthma // Allergy. – 1997. – Vol.52 (Suppl.39). – P.1–34.
35. Price D., Robertson A., Bullen K. et al. Improved adherence with once-daily versus twice-daily dosing of mometasone furoate administered via a dry powder inhaler: a randomized open-label study // BMC Pulm. Med. – 2010. – Vol.10. – P.1.
36. Rabe K., Vermeire P. et al. Clinical management of asthma in 1999: the Asthma Insights and Reality in Europe (AIRE) study // Eur. Respir. J. – 2000. – N16. – P.802–807.
37. Shah S., Peat J.K., Mazurski E.J. et al. Effect of peer led program for asthma education in adolescents: cluster randomised controlled trial // BMJ. – 2001. – Vol.322 (7286). – P.583–585.
38. Suissa S., Ernst P., Benayoun S., Baltzan M., Cai B. Low-dose inhaled corticosteroids and the prevention of death from asthma // N. Engl. J. Med. – 2000. – Vol.343 (5). – P.332–336.
39. Thorsson L., Dahlstrom S., Edsbacker V. et al. Pharmacokinetics and systemic effects of inhaled fluticasone propionate in healthy subjects // Brit. J. Clin. Pharmacol. – 1997. – Vol.43. – P.155–161.
40. Waalkens H.J., Van Essen Zandvliet E.E., Hughes M.D. et al. Cessation of long-term treatment with inhaled corticosteroid (budesonide) in children with asthma results in deterioration. The Dutch CNSLD Study Group // Am. Rev. Respir. Dis. – 1993. – Vol.148 (5). – P.1252–1257.
41. Williams L.K., Peterson E.L., Wells K. et al. Quantifying the proportion of severe asthma exacerbations attributable to inhaled corticosteroid nonadherence // J. Allergy Clin. Immunol. – 2011. – Vol.128 (6). – P.1185–1191.
42. Williams L.K., Pladevall M., Xi H. et al. Relationship between adherence to inhaled corticosteroids and poor outcomes among adults with asthma // J. Allergy Clin. Immunol. – 2004. – Vol.114 (6). – P.1288–1293.
Медицинские новости. – 2015. – №10. – С. 76-80.
Внимание! Статья адресована врачам-специалистам. Перепечатка данной статьи или её фрагментов в Интернете без гиперссылки на первоисточник рассматривается как нарушение авторских прав.