Gontschar I.A.1, Prudyvus I.S.2, Bаnchkouskaya T.J.1
1Republican Scientific and Practical Center of Neurology and Neurosurgery, Minsk, Belarus
2N.N. Alexandrov Republican Scientific and Practical Center of Oncology and Medical Radiology Lesnoy, Minsk District, Belarus
Hemostatic parameters and clinical outcome of acute ischemic stroke
Резюме. Цель исследования – определение взаимосвязи между выраженностью нарушений гемостаза с функциональным исходом и выживаемостью пациентов с острым инфарктом головного мозга. Проведено проспективное исследование когорты из 339 пациентов с инфарктом мозга; средний возраст – 71,7±10,6. Проведен комплексный анализ состояния сосудисто-тромбоцитарного и плазменного гемостаза, позволивший установить клинически значимые ассоциации дизрегуляции гемостаза с риском летального исхода после инфаркта мозга. Определена взаимосвязь параметров оптической агрегометрии тромбоцитов с тяжестью неврологических нарушений, функциональным исходом и выживаемостью пациентов в постинсультном периоде.
Ключевые слова: выживаемость, гемостаз, инфаркт мозга, оптическая агрегометрия тромбоцитов, функциональный исход.
Медицинские новости. – 2015. – №3. – С. 65–70.
Summary. The purpose of investigation – to determine the relationship between the severity of hemostatic disorders and functional outcome of acute ischemic stroke (IS). A prospective cohort study of 339 patients with IS; average age – 71,7±10,6 years was carried out. A comprehensive analysis of the primary and secondary hemostasis allowed to establish clinically significant association of hemostasis dysregulation with risk of death after IS. Relationship parameters of the light transmission platelet aggregometry with the severity of neurological disorders, functional outcome and survival after IS was defined.
Keywords: functional outcome, hemostasis, ischemic stroke, light transmission platelet aggregometry, survival.
Meditsinskie novosti. – 2015. – N3. – P. 65–70.
В развитии и прогрессировании острого инфаркта головного мозга (ИГМ) значительная роль принадлежит дизрегуляции сосудисто-тромбоцитарного и плазменного гемостаза [2, 3]. Система гемостаза человека включает шесть основных компонентов: эндотелий сосудов, тромбоциты, прокоагулянтные протеины крови, естественные антикоагулянты – белки плазмы крови, фибринолитические и антифибринолитические протеины. В процессе гемостаза выделяют три основных этапа. Первичный, или сосудисто-тромбоцитарный гемостаз, в котором принимают участие эндотелий и кровяные пластинки (тромбоциты), продолжается 3–5 минут, результатом этапа является образование тромбоцитарного сгустка. Вторичный гемостаз, или ферментативная коагуляция, – реализуется с помощью плазменных факторов свертывания и тромбоцитарного фактора. Продолжительность второго этапа – 5–10 минут, в течение которых образуются нити фибрина, скрепляющие тромбоцитарный сгусток, и происходит окончательное формирование тромба. Третий, или последний, этап гемостаза – это фибринолиз, приводящий к растворению тромба.
Пациентам с ИГМ, не получающим тромболитическую терапию, с первых суток госпитализации назначают антитромботическую терапию, воздействующую на основные звенья гемостаза. Антиагрегантные лекарственные средства, такие как ацетилсалициловая кислота (АСК) и клопидогрел, снижающие агрегационную активность кровяных пластинок, назначают с целью вторичной профилактики ишемических церебро- и кардиоваскулярных событий. Пациентам с фибрилляцией предсердий (ФП), тромбозом глубоких вен, гипомобильностью показаны антикоагулянты, призванные снизить риск тромбоэмболических осложнений: нефракционированный гепарин, низкомолекулярные гепарины, варфарин или новые оральные антикоагулянты – дабигатран, ривароксабан.
Цель исследования – определение взаимосвязи между выраженностью нарушений гемостаза с функциональным исходом и выживаемостью пациентов, госпитализированных по поводу острого ИГМ.
Материалы и методы
Проведен анализ состояния сосудисто-тромбоцитарного гемостаза 339 пациентов с ИГМ (средний возраст 71,7±10,6 года), госпитализированных в неврологическое отделение №1 Больницы скорой медицинской помощи города Минска. В группу контроля включили 17 добровольцев (средний возраст 70,8±3,8 года), не имеющих клинически значимых острых или хронических цереброваскулярных заболеваний, сердечно-сосудистой, инфекционной, аутоиммунной, онкологической патологии. Возраст пациентов основной и контрольной групп не отличался (р=0,194).
Диагноз ИГМ основывали на клинических данных, подтверждая его во всех случаях нейровизуализационным исследованием – компьютерной и/или магнитно-резонансной томографией головного мозга. Сроки от развития инсульта до взятия крови для определения гемостазиологических параметров в 1-е сутки лечения не превышали 48 ч. Повторный забор крови выполняли на 10-е сутки. Взятие крови проводили в пробирки, содержащие в качестве антикоагулянта 3,8% раствор цитрата натрия при соотношении крови и антикоагулянта 9:1.
Индуцированную оптическую агрегометрию тромбоцитов(ОАТ) регистрировали с помощью оптического агрегометра АР 2110 («Солар», Беларусь) согласно методу Борна [9]. Оценивали образование тромбоцитарных агрегатов в ответ на действие трех индукторов: раствора аденозиндифосфата (АДФ) низкой концентрации – 0,5 мкмоль/л, раствора АДФ средней концентрации – 1,5 мкмоль/л, а также раствора коллагена в конечной концентрации 2 г/л («Технология-Стандарт», Россия) [1, 3]. Процесс образования тромбоцитарных агрегатов визуализировали графически с помощью агрегационных кривых. Анализ результатов ОАТ включал скорость агрегации (амплитуда агрегатограммы через 30 секунд после начала агрегации, %/мин), степень агрегации (максимальная амплитуда агрегатограммы, %) и время достижения максимальной агрегации (мин). Данные ОАТ пациентов с ИГМ анализировали путем сопоставления их с контрольными значениями агрегации кровяных пластинок здоровых лиц [3].
Исследование параметров плазменного гемостаза выполняли с помощью автоматического коагулометра ACL ELITE PRO («Instrumentation Laboratory», США) унифицированным клоттинговым методом. Определяли активированное парциальное тромбопластиновое время (АПТВ), отношение уровня АПТВ пациента к значению АПТВ контрольной плазмы (R АПТВ), протромбиновое время (ПВ), R ПВ, международное нормализованное отношение (МНО), протромбиновый индекс (ПТИ), концентрацию фибриногена [3]. Определение плазменного уровняД-димеров (ДД), а также активности антигена фактора Виллебранда (ФВ) проводили на коагулометре ACL-10000 в соответствии с инструкциями производителя («Instrumentation Laboratory Company», США) [2].
Протокол исследования одобрен этическим комитетом. Взятие образцов крови для исследования выполняли с соблюдением процедуры добровольного информированного согласия на участие в исследовании.
Статистический анализ данных выполняли с использованием программы R-system V. 2.8.0. Статистическую значимость различий между группами оценивали: для двух подгрупп с помощью критерия Манна–Уитни (при распределении данных, отличных от нормальных) или с применением критерия Стьюдента (для данных с нормальным распределением). Для оценки значимости различий качественных данных использовали точный критерий Фишера. Выживаемость пациентов с ИГМ оценивали по методу Каплана–Майера. Сравнение выживаемости в подгруппах выполняли с использованием лог-ранг теста. Оценку влияния изучаемых параметров на исход выполняли с использованием регрессионного анализа пропорциональных рисков Кокса. Различия считали статистически значимыми при значениях оцененного p<0,05.
Результаты и обсуждение
Основные кинические характеристики пациентов с ИГМ представлены в табл. 1.
Таблица 1. Клинические характеристики пациентов с ИГМ (n = 339)
|
Критерий
|
Кол-во пациентов
|
|
Мужской пол
|
145 (42,8%)
|
|
ИГМ в левом каротидном бассейне артерий
|
153 (45,1%)
|
|
Классификация TOAST: макроангиопатия
|
101 (29,8%)
|
|
кардиоэмболия
|
61 (18,0%)
|
|
микроангиопатия
|
54 (15,9%)
|
|
неуточненная / смешанная этиология
|
123 (36,3%)
|
|
Оксфордская классификация: тотальный инсульт в каротидном бассейне
|
87 (25,7%)
|
|
частичный инсульт в каротидном бассейне
|
143 (42,2%)
|
|
лакунарный синдром
|
66 (19,5%)
|
|
ИГМ задней мозговой циркуляции
|
43 (12,7%)
|
|
Прогрессирующий инсульт
|
118 (34,8%)
|
|
Стеноз церебральных артерий?больше или равно 30%
|
73 (32,9%)
|
|
Транзиторная ишемическая атака или инсульт в анамнезе
|
90 (26,5%)
|
|
Постинфарктный кардиосклероз
|
63 (18,6%)
|
|
Фибрилляция предсердий
|
157 (46,3%)
|
|
Застойная сердечная недостаточность
|
116 (34,2%)
|
|
Артериальная гипертензия 3 ст.
|
84 (24,8%)
|
|
Сахарный диабет
|
89 (26,3%)
|
Оценка неврологических нарушений по шкале инсульта Национальных институтов здравоохранения (NIHSS) при поступлении соответствовала 7 {5; 13} баллам, по окончании лечения – 5 {3; 12}. Функциональный дефицит при выписке достигал 3 {2; 4} баллов по Модифицированной шкале Рэнкина (МШР). В качестве антитромботической терапии пациенты с острым ИГМ получали АСК (153 чел.; 45,1%), клопидогрел (37 чел.; 10,9%), АСК в сочетании с прямыми антикоагулянтами (69 чел.; 20,4%), прямые или непрямые антикоагулянты (80 чел.; 23,6%).
В табл. 2 сопоставлены данные ОАТ в 1-е сутки госпитализации пациентов с ИГМ в сравнении с группой контроля. В дебюте инсульта состояние первичного гемостаза характеризовалось гиперагрегационным ответом тромбоцитов на действие индукторов. Об этом свидетельствует статистически значимое увеличение степени агрегации тромбоцитов у пациентов с ИГМ по сравнению с группой контроля при действии всех использованных индукторов. Скорость и время ОАТ с такими индукторами, как АДФ 1,5 мкмоль/л и коллаген, также имели статистически значимые отличия от параметров здоровых добровольцев.
Таблица 2. Параметры оптической агрегатометрии тромбоцитов в 1-е сутки госпитализации пациентов с ИГМ и пациентов группы контроля
|
Параметр
|
ИГМ, n = 339
|
Контроль, n = 17
|
р
|
|
Индуктор АДФ в концентрации 0,5 мкмоль/л
|
|
Скорость агрегации, % в мин
|
35,3 {28,4; 43,6}
|
31,8 {28,2; 41,5}
|
НЗ
|
|
Степень агрегации, %
|
64,1 {52,7; 74,1}
|
65,4 {50,0; 62,0}
|
0,026
|
|
Время агрегации, мин
|
5,1 {3,7; 6,6}
|
4,9 {3,7; 5,2}
|
НЗ
|
|
Индуктор АДФ в концентрации 1,5 мкмоль/л
|
|
Скорость агрегации, % в мин
|
40,2 {31,7; 48,9}
|
30,1 {28,2; 34,4}
|
0,003
|
|
Степень агрегации, %
|
73,2 {64,8; 82,0}
|
57,8 {55,8; 59,2}
|
< 0,001
|
|
Время агрегации, мин
|
6,5 {5,3; 7,5}
|
4,7 {3,7; 5,1}
|
< 0,001
|
|
Индуктор коллаген
|
|
Скорость агрегации, % в мин
|
34,0 {24,2; 44,4}
|
39,5 {36,3; 45,1}
|
0,047
|
|
Степень агрегации, %
|
72,2 {56,2; 83,2}
|
56,9 {55,4; 70,1}
|
0,021
|
|
Время агрегации, мин
|
8,1 {6,1; 9,3}
|
5,0 {4,4; 7,4}
|
< 0,001
|
П р и м е ч а н и е (здесь и в табл. 3–5) : Данные представлены в виде: медиана {Q1; Q3}. НЗ – различия статистически незначимы.
На 10-е сутки при исследовании ОАТ с индуктором АДФ в концентрации 0,5 мкмоль/л отмечено снижение степени и времени агрегации тромбоцитов. Применение в качестве индуктора агрегации раствора АДФ средней концентрации (1,5 мкмоль/л) продемонстрировало сокращение времени агрегации за время лечения с 6,9 {5,4; 8,1} до 6,2 {5,0; 7,5} мин соответственно; р = 0,001. Аналогичные результаты получены при стимулировании агрегации кровяных пластинок раствором коллагена. Прогрессирующее клиническое течение ИГМ, диагностированное у 118 (34,8%) из 339 пациентов, не сопровождалось достоверными изменениями ОАТ.
Тяжелый неврологический дефицит, превышающий 14 баллов по шкале NIHSS при поступлении в клинику, был ассоциирован с удлинением времени агрегации тромбоцитов при действии АДФ 0,5 мкмоль/л и с коллагеном (р = 0,001 и р = 0,009 соответственно). Тяжесть неврологических симптомов инсульта, сохраняющаяся на момент выписки из стационара, также имела статистически значимые взаимосвязи с показателями ОАТ (табл. 3).
Таблица 3. Параметры оптической агрегатометрии тромбоцитов пациентов с ИГМ и выраженность неврологического дефицита на 10-е сутки
|
Параметр
|
NIHSS 0-14 баллов, 10-е сутки,
n = 275
|
NIHSS больше или равно 15 баллов, 10-е сутки, n = 64
|
р
|
|
Время агрегации с АДФ в концентрации
0,5 мкмоль/л в 1-е сутки, мин
|
4,7 {3,5; 6,5}
|
6,0 {4,6; 7,8}
|
0,002
|
|
Время агрегации с коллагеном в 1-е сутки, мин
|
8,0 {6,0; 9,3}
|
8,6 {6,7; 9,4}
|
0,015
|
|
Скорость агрегации с АДФ в концентрации 0,5 мкмоль/л на 10-е сутки, % в мин
|
34,7 {27,5; 42,2}
|
31,2 {27,1; 36,8}
|
0,038
|
|
Время агрегации с АДФ в концентрации
0,5 мкмоль/л на 10-е сутки, мин
|
4,1 {2,8; 5,5}
|
5,3 {3,3; 6,3}
|
0,030
|
|
Время агрегации с коллагеном
на 10-е сутки, мин
|
7,5 {6,0; 9,2}
|
9,0 {7,4; 9,5}
|
0,001
|
Грубые неврологические симптомы при выписке сопровождались удлинением времени агрегации кровяных пластинок с раствором АДФ низкой концентрации и раствором коллагена на 10-е сутки (р = 0,030 и р = 0,001 соответственно). Аналогичная взаимосвязь отмечена и при сопоставлении выраженности неврологического дефицита с данными ОАТ, выполненной в 1-е сутки.
При рассмотрении результатов лечения функциональный исход инсульта считали удовлетворительным при восстановлении способности пациентов к самостоятельному передвижению и самообслуживанию (0–3 балла МШР) и неудовлетворительным – при сохранении потребности в постороннем уходе, невозможности передвижения и самообслуживания, а также в случае летального исхода (4–6 баллов МШР). Параметры ОАТ и функциональный исход ИГМ отражены в табл. 4.
Неудовлетворительный функциональный исход инсульта сопровождался удлинением времени агрегации тромбоцитов с индукторами АДФ 0,5 мкмоль/л и коллагеном, а также снижением скорости агрегации с раствором АДФ средней концентрации, что указывает на угнетение функциональной активности тромбоцитов, возможно, по причине истощения депо собственных индукторов, содержащихся в гранулах. Кроме того, пациенты с тяжелыми инвалидизирующими нарушениями при выписке уже на момент поступления в стационар демонстрировали статистически значимое удлинение времени агрегации тромбоцитов с растворами коллагена и АДФ 0,5 мкмоль/л по сравнению с пациентами с легким/умеренным функциональным дефицитом.
Данные ОАТ в отношении постинсультной летальности представлены в табл. 5. Летальный исход, развившийся в течение 30 суток, ассоциирован с увеличением скорости, степени и времени ОАТ с АДФ 0,5 мкмоль/л в 1-е сутки заболевания. Удлинение времени агрегации с раствором АДФ низкой концентрации на 10-е сутки при одновременном снижении скорости ОАТ также было ассоциировано с развитием летального исхода в постинсультном периоде, что согласуется с показателями, отраженными в табл. 4.
Таблица 4. Параметры оптической агрегатометрии тромбоцитов пациентов с ИГМ и функциональный исход ИГМ
|
Параметр
|
Удовлетворительный исход ИГМ (МШР 0–3 балла), n = 208
|
Неудовлетворительный исход ИГМ (МШР 4–6 баллов),
n = 131
|
р
|
|
Время агрегации с АДФ в концентрации 0,5 мкмоль/л в 1-е сутки, мин
|
4,5 {3,4; 6,4}
|
5,6 {4,4; 7,2}
|
<0,001
|
|
Время агрегации с коллагеном
в 1-е сутки, мин
|
7,7 {6,0; 9,1}
|
8,4 {6,5; 9,4}
|
0,008
|
|
Время агрегации с АДФ в концентрации 0,5 мкмоль/л на 10-е сутки, мин
|
3,5 {2,5; 5,4}
|
4,5 {3,2; 6,2}
|
0,002
|
|
Скорость агрегации с АДФ в концентрации 1,5 мкмоль/л на 10-е сутки, % в мин
|
39,4 {32,8; 46,0}
|
35,8 {29,4; 41,5}
|
0,030
|
|
Время агрегации с коллагеном
на 10-е сутки, мин
|
7,3 {5,7; 9,2}
|
8,3 {7,1; 9,5}
|
0,003
|
Таблица 5. Параметры оптической агрегатометрии тромбоцитов и летальный исход в течение 30 суток после ИГМ
|
Параметр
|
Выжившие пациенты,
n = 288
|
Умершие пациенты,
n = 51
|
р
|
|
Скорость агрегации с АДФ в концентрации
0,5 мкмоль/л в 1-е сутки, % /мин
|
34,9 {28,2; 42,8}
|
39,9 {31,4; 48,0}
|
0,035
|
|
Степень агрегации с АДФ в концентрации
0,5 мкмоль/л в 1-е сутки, %
|
63,5 {52,1; 73,3}
|
68,5 {57,0; 80,4}
|
0,027
|
|
Время агрегации с АДФ в концентрации
0,5 мкмоль/л в 1-е сутки, мин
|
5,0 {3,5; 6,5}
|
5,6 {4,6; 7,3}
|
0,010
|
|
Скорость агрегации с АДФ в концентрации
0,5 мкмоль/л на 10-е сутки, % в мин
|
34,8 {27,6; 42,0}
|
27,6 {21,6; 36,4}
|
0,019
|
|
Время агрегации с АДФ в концентрации
0,5 мкмоль/л на 10-е сутки, мин
|
4,0 {2,8; 5,6}
|
5,3 {3,7; 7,0}
|
0,025
|
В качестве конечной точки исследования анализировали случаи инсульта с летальным исходом, развившимся в течение 365 суток после ИГМ. Регрессионный анализ пропорциональных рисков Кокса показал, что удлинение времени ОАТ в тесте с АДФ 0,5 мкмоль/л, выполненном на 10-е сутки наблюдения в стационаре, ассоциировано с достоверным снижением выживаемости после инсульта (р = 0,043).
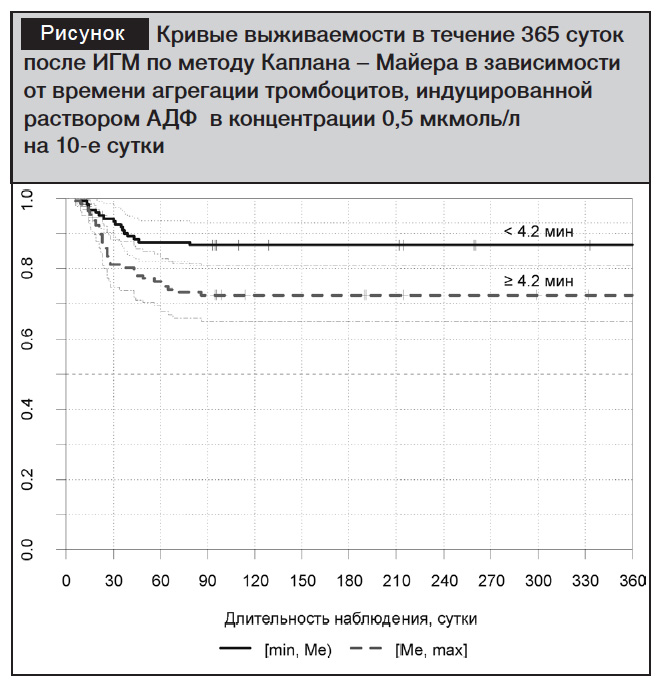
На рисунке представлены кривые выживаемости Каплана – Майера пациентов с ИГМ в зависимости от состояния ОАТ, индуцированной раствором АДФ в концентрации 0,5 мкмоль/л, на 10-е сутки госпитализации. Медиана времени ОАТ составила 4,2 минуты. Данное значение принято в качестве порогового, разделяющего 254 пациентов с инсультом на две подгруппы: с коротким временем агрегации, не превышающим 4,2 минуты, и длинным, равным или превышающим 4,2 минуты. В течение 365 суток наблюдения в первой подгруппе (время ОАТ < 4,2 минуты) скончалось 16 из 125 пациентов (12,8 %), а во второй подгруппе (время ОАТ ? 4,2 минуты) – 35 из 129 (27,1%). Сопоставлена выживаемость пациентов с коротким временем агрегации с выживаемостью лиц с удлиненным временем ОАТ. При этом выживаемость пациентов в первой подгруппе достигала 0,866 {95% Доверительный интервал (ДИ): 0,808–0,930}, а во второй – лишь 0,725 {95% ДИ: 0,651-0,807}. Короткое время агрегации тромбоцитов по данным ОАТ на 10-е сутки, индуцированной раствором АДФ 0,5 мкмоль/л, сопряжено с достоверно более высоким уровнем долгосрочной выживаемости в постинсультном периоде по сравнению с удлиненным временем агрегации: лог-ранг тест p = 0,006.
Проанализированы данные гемостазиограмм на 1-е и 10-е сутки ИГМ. Пациенты с грубыми функциональными нарушениями при выписке по сравнению с пациентами с благоприятным исходом лечения отличались:
– повышением уровня фибриногена в 1-е сутки (3,56 {2,87; 4,16} и 3,27 {2,81; 3,88} г/л соответственно; р = 0,023) и 10-е сутки (3,95 {3,3; 5,02} и 3,3 {2,75; 4,2} г/л соответственно; р = 0,003);
– снижением количества тромбоцитов на 10-е сутки наблюдения (195{141; 237} и 225 {187; 260} ? 109/л соответственно; р = 0,001);
– удлинением ПВ в 1-е сутки (14,9 {13,9; 16,0} и 14,1 {13,4; 14,9} с соответственно; р = < 0,001) и 10-е сутки (15,5{14,2; 16,9} и 13,9 {13,2; 14,4} с соответственно; р < 0,001);
– удлинением МНО в 1-е сутки (1,11 {1,03; 1,19} и 1,07 {1,00; 1,13} соответственно; р = 0,001) и 10-е сутки (1,17 {1,08; 1,3} и 1,04 {0,99; 1,1} соответственно; р < 0,001).
Кроме того, выявлено повышение уровня ДД в 1-е сутки, а также активности антигена ФВ в 1-е и 10-е сутки госпитализации [2]. Аналогичная закономерность отмечена и при анализе параметров плазменного гемостаза у умерших и выживших пациентов с ИГМ. Летальный исход в течение 30 суток наблюдения был сопряжен с увеличением количества лейкоцитов при поступлении, снижением числа тромбоцитов в 1-е и 10-е сутки, сокращением R АПТВ в 1-е сутки при одновременном удлинении ПВ, R ПВ и МНО в 1-е и 10-е сутки, возрастании уровня фибриногена и ФВ в крови в 1-е сутки инсульта.
В острейшем периоде ишемического инсульта тромбоцитарное звено гемостаза находится в состоянии гиперактивации. При этом не только скорость и степень агрегации, но и время ОАТ значимо отличаются от параметров здоровых лиц в тестах с АДФ и коллагеном. Необходимо отметить, что в доступных нам источниках мы не нашли научных работ, анализирующих взаимосвязь скорости, степени и времени ОАТ с выживаемостью после инсульта. Ряд исследователей указывают на недостаточное снижение степени агрегации тромбоцитов под действием АСК или клопидогрела, назначенных с профилактической целью, как фактор риска ишемических коронарных или цереброваскулярных событий [5, 6]. Однако время агрегации кровяных пластинок ранее не являлось предметом научного анализа в свете постинсультной выживаемости. Наше исследование позволило обнаружить клинически значимую взаимосвязь времени, степени и скорости агрегации тромбоцитов, индуцированной растворами АДФ и коллагена, с выраженностью неврологических симптомов ИГМ, функциональным исходом и летальностью, информация о чем в ранее проведенных исследованиях отсутствовала.
В нашем исследовании повышение уровней ПВ, R ПВ, МНО, фибриногена на фоне низкого количества тромбоцитов стало маркером хронически протекающего ДВС-синдрома, сопряженного с повышенным риском смерти. С неудовлетворительным исходом лечения инсульта, приведшим к сохранению выраженной инвалидизации или развитию летального исхода в остром периоде инсульта, ассоциировано также снижение уровня R АПТВ, количества тромбоцитов, ПТИ при одновременном удлинении ПВ, R ПВ, МНО, увеличении концентрации фибриногена, ФВ и ДД. При ФП, застойной сердечной недостаточности, обездвиженности пациентов запускается каскад сложных тромбоэмболических механизмов [1–3, 6], связанных с эндотелиальной дисфункцией, застоем крови в левом предсердии, гиперкоагуляцией, что нашло отражение в показателях, отражающих состояние гемостаза. Ключевым ферментом коагуляционного процесса является тромбин, активность которого определяют по уровню Д-димеров и других маркеров фибринообразования [5].
Истощение функции тромбоцитов в остром периоде ИГМ, проявляющееся снижением агрегабельности кровяных пластинок в ответ на действие индуктора – АДФ средней концентрации, отражает выраженные дисметаболические нарушения у тяжело инвалидизированных пациентов. Определение уровня ОАТ наряду с традиционной коагулограммой на 1-е и 10-е сутки ИГМ позволяет не только обнаружить дизрегуляцию сосудисто-тромбоцитарного гемостаза в остром периоде инсульта, но и использовать полученные результаты для прогнозирования постинсультной выживаемости и степени функционального восстановления пациентов.
В ходе клинической интерпретации данных гемостазиологического исследования необходимо принимать во внимание, что реакции коагуляционного каскада in vivo протекают не в свободной плазме, а «посажены» на поверхности клеточных мембран, в первую очередь, тромбоцитов [7]. Кровяные пластинки активно участвуют в функционировании системы свертывания крови за счет экспонирования прокоагулянтной мембраны и синтеза альфа-гранул, содержащих факторы роста, тромбоцитарный фактор 4 и другие протеины системы тромбообразования, а также Р-селектин [14].
Снижение количества тромбоцитов у пациентов с летальным исходом и тяжелой инвалидизацией сопряжено с процессом повышенного потребления и плазменных факторов свертывания и тромбоцитов в процессах микротромбообразования при подостром и хроническом синдроме диссеминированного внутрисосудистого свертывания крови (ДВС-синдроме). Это проявляется декомпенсацией состояния пациентов с ИГМ с увеличением ПВ, МНО, концентрации фибриногена, ВФ, ДД наряду с удлинением времени агрегации тромбоцитов с АДФ и коллагеном. Нарушение агрегационных свойств тромбоцитов на фоне лечения при неудовлетворительном исходе ИГМ может быть объяснено воздействием на них продуктов деградации фибрина при ДВС-синдроме. Снижение скорости агрегации с одновременным удлинением времени ОАТ на 10-е сутки наблюдения у пациентов с инфарктом мозга необходимо рассматривать с позиций функциональной неполноценности тромбоцитов, поступающих в системный кровоток из лизированных тромбов микрососудистого русла [11].
Для подострого варианта ДВС-синдрома при ИГМ характерно удлинение периода гиперкоагуляции и/или гиперагрегации тромбоцитов, сопряженное с тромбоцитопенией, сокращенным АПТВ, нормальным или удлиненным ПВ, нормальным или повышенным уровнем фибриногена в крови. Геморрагические осложнения при подостром ДВС-синдроме, осложняющем течение ИГМ, встречаются нечасто. Ранее было показано, что повышение уровня фибриногена, как протеина острой фазы воспаления, является основной причиной венозных и артериальных тромбоэмболических осложнений [4].
Хроническая форма ДВС-синдрома оказывает постоянное, но менее интенсивное активирующее воздействие на систему гемостаза, что объясняется малой скоростью генерации тромбина, достаточной для формирования микроциркуляторных нарушений. Известно, что хроническая форма ДВС-синдрома наблюдается при атеросклерозе сосудов мозга, сердца, конечностей, сахарном диабете, артериальной гипертензии и других факторах риска инфаркта мозга, а также при хронической патологии легких, почек и других заболеваниях [4]. Наличие процессов хронического диссеминированного свертывания крови при ишемическом инсульте продемонстрировано в работах З.А. Суслиной с соавт. [6].
Ведущим механизмом дизрегуляции сосудисто-тромбоцитарного гемостаза при ДВС являются нарушения в системе микроциркуляции [14]. Выпадение фибрина в сосудах микроциркуляторного русла сопровождается снижением скорости кровотока, сборкой эритроцитов в монетные столбики, травматизацией и деформированием эритроцитов, нарастанием анизоцитоза и появлением клеточного дебриса [4]. Кровяные пластинки при ДВС – базовый субстрат действия патологического фактора, когда в результате их повышенного потребления в процессах микро- и макротромбообразования развивается тромбоцитопения со снижением количества тромбоцитов менее 150 ? 109/л. [11]. Наряду с тромбоцитопенией развивается тромбоцитопатия вследствие экстренного выхода в кровоток незрелых тромбоцитов и потребления наиболее полноценного пула кровяных пластинок [4].
О нарушении сосудисто-тромбоцитарного гемостаза при ДВС-синдроме в остром периоде ИГМ свидетельствует снижение в крови тромбоцитов при одновременном повышении степени и скорости ОАТ. Вместе с тем необходимо учитывать, что при ДВС-синдроме выраженная тромбоцитопатия сопровождается снижением скорости и степени индуцированной агрегации кровяных пластинок [4]. Помимо сокращения скорости и степени ОАТ к 10-м суткам лечения, у пациентов с неблагоприятным исходом ИГМ зафиксировано увеличение времени агрегации тромбоцитов с растворами АДФ низкой концентрации и коллагена.
Полученные нами данные согласуются с исследованиями других авторов, продемонстрировавшими удлинение, а не укорочение времени свертывания крови вследствие дефицита факторов свертывания на фоне усиления тромбообразования при остром и хроническом ДВС-синдроме [10, 13]. Большинство клоттинговых тестов для исследования плазменного звена гемостаза, направленных в первую очередь на выявление гипокоагуляции, проводятся в лабораториях в условиях максимальной активации свертывания, поэтому изолированное применение коагулограммы не всегда позволяет диагностировать гиперкоагуляцию [8, 12], характерную для подострого и острого ДВС-синдрома у пациентов с ишемическим инсультом. Очевидно, что проведение ОАТ наряду с коагулограммой позволяет дать комплексную оценку состояния сосудисто-тромбоцитарного, плазменного и фибринолитического звена гемостаза в остром периоде инфаркта мозга.
Выполненное исследование показало, что степень дизрегуляции сосудисто-тромбоцитарного и плазменного гемостаза имеет тесную связь с клиническим исходом инсульта. Сохранение дисбаланса основных звеньев гемостаза на фоне лечения свидетельствует о недостаточной эффективности проводимой медикаментозной терапии, не позволившей предотвратить фатальный исход ИГМ. В этом контексте необходимо отметить, что цель реперфузионной и антитромботической терапии в остром периоде ИГМ состоит не в достижении полной нормализации показателей гемостазиограммы, а в переводе системы гемостаза на безопасный уровень, позволяющий, с одной стороны, предотвратить развитие повторного ишемического инсульта, с другой, минимизировать риск геморрагических осложнений. В результате клинико-лабораторного исследования разработана и внедрена в практическое здравоохранение инструкция по применению [3], включающая алгоритм диагностики состояния системы гемостаза, позволяющий выявить признаки наличия и прогрессирования ДВС-синдрома в остром периоде ИГМ, сопряженного с неблагоприятным клиническим исходом лечения.
Таким образом, принципиально новым и важным в нашей работе является комплексный анализ состояния сосудисто-тромбоцитарного и плазменного гемостаза, позволивший установить клинически значимые ассоциации дизрегуляции гемостаза с риском летального исхода после ИГМ. Определена взаимосвязь параметров ОАТ с тяжестью неврологических нарушений, функциональным исходом и выживаемостью пациентов в постинсультном периоде. Разработаны методы диагностики состояния системы гемостаза, позволяющие выявить признаки ДВС-синдрома в остром периоде ИГМ, сопряженного с неблагоприятным клиническим исходом лечения.
Л И Т Е Р А Т У Р А
1. Гончар И. А., Степанова Ю. И., Лихачев С. А. и др. // Неврология и нейрохирургия в Беларуси. – 2011. – №3 (11). – С.76–85.
2. Гончар И.А., Степанова Ю.И., Прудывус И.С. Биохимические предикторы и маркеры острого инфаркта мозга. – Минск: БелМАПО, 2013. – www.slideshare.net.
3. Гончар И.А., Степанова Ю.И., Лихачев С.А. и др. Методы диагностики и лечения нарушений сосудисто-тромбоцитарного и плазменного гемостаза при остром инфаркте мозга: Инструкция по применению №228-1213, утв. 27.12.2013. – Минск, 2014. – www.slideshare.net.
4. Долгов В.В., Свирин П.В. Лабораторная диагностика нарушений гемостаза. – М. –Тверь: Триада, 2005.
5. Комаров А.Л. Факторы, определяющие прогноз и эффективность антитромбоцитарной терапии у больных хронической ишемической болезнью сердца: автореф. дис. …д-ра мед. наук. – М., 2012. – 52 с.
6. Очерки ангионеврологии / под ред З.А. Суслиной. – М: Атмосфера, 2005. – 368 с.
7. Пантелеев М. А., Атаулаханов Ф. И. // Клинич. онкогематология. – 2008. – Т.1(1). – С.50–62.
8. Сошитова Н. П. Выявление нарушений гемостаза при сепсисе с помощью метода пространственного роста сгустка: автореф. дис. …канд. биол. наук. – М., 2012. – 20 с.
9. Born G.V.R. // J. Physiol. – 1962. – Vol.162. – P.67–68.
10. Collins P.W., Macchiavello L.I., Lewis S.J. et al. // Br. J. Haematol. – 2006. – Vol.135. – P.220–227.
11. Damodaran V.B., Leszczak V., Wold K.A. et al. // RSC Adv. – 2013. – Vol.14. – P.46–49.
12. Dempfle C.E. // Thromb. Haemost. – 2004. – Vol.91. – P.213–224.
13. Stief T. W., Ijagha O., Weiste B. et al. // Blood Coagul. Fibrinolysis. – 2007. – Vol.18. – P.179–186.
14. Waiker V. P., Shivalingappa S. // World J. Plast. Surg. – 2015. – Vol.4 (1). – P.50–59.
Медицинские новости. – 2015. – №3. – С. 65-70.
Внимание! Статья адресована врачам-специалистам. Перепечатка данной статьи или её фрагментов в Интернете без гиперссылки на первоисточник рассматривается как нарушение авторских прав.