Prystrom А.М.1, Kazakov S.А.1, Rachok S.М.1, Rutskaya Т.А.1, Chechko R.U.2, Kursevich V.V.2, Lushnikova I.Е.3,
Samohodkina S.V.3, Kolobova Е.V.3, Seregin S.V.3, Tselikova N.G.3, Kostukevich S.V.3, Piskunov S.Е. 3, Shumilov V.N.3
1Belarusian Medical Academy of Post-Graduate Education, Minsk, Belarus
22nd Clinical Hospital Minsk, Belarus
31st Clinical Hospital Minsk, Belarus
Treatment of hypertension: open prospective postmarketing study of Valsacor® and Valsacor® H80 antihypertensive efficacy
Резюме. Представлена информация о рекомендуемых в настоящее время целевых цифрах артериального давления у больных артериальной гипертензией (АГ) с различными степенями сердечно-сосудистого риска, а также у пациентов пожилого возраста согласно «Рекомендациям ESH/ESC по лечению АГ 2013 г.». Дан анализ эффективности и безопасности антагонистов рецепторов ангиотензина (АРА) и трудностей, которые сопровождали эту группу препаратов на пути внедрения в широкую клиническую практику. Приводятся результаты собственных исследований эффективности антигипертензивных препаратов Вальсакор® 80 и 160 мг (KRKA) и фиксированной комбинации Вальсакор® Н80 (KRKA). Терапия препаратами Вальсакор® и Вальсакор® Н80 обеспечивает стабильный и длительный антигипертензивный эффект, позволяя в большинстве случаев (76%) достигать целевых уровней артериального давления. Побочных эффектов и нежелательных явлений в течение 4 недель наблюдения не отмечалось.
Ключевые слова: артериальная гипертензия, валсартан, Вальсакор, антигипертензивная терапия, антигипертензивная эффективность лечения Вальсакором.
Медицинские новости. – 2014. – №12. – С. 33 –37.
Summary. The article provides information on the currently recommended blood pressure goals in hypertensive patients with various categories of total cardiovascular risk, as well as in elderly patients according to the «2013 ESH/ESC Guidelines for the management of arterial hypertension». The analysis of the efficacy and safety of angiotensin receptor antagonists and the difficulties that accompany this group of drugs to the introduction of a broad clinical practice are reviewed. We present the results of our own research of the effectiveness of antihypertensive drugs Valsakor® 80 and 160 mg (KRKA) and fixed combination Valsakor® N80 (KRKA). Therapy with Valsakor® and Valsakor® N80 provides a stable and long-lasting antihypertensive effect, allowing in most cases (76%) to reach target blood pressure levels. Side effects and adverse events in four weeks observations weren’t noted.
Keywords: arterial hypertension, valsartan, Valsacor, antihypertensive therapy, antihypertensive efficacy of treatment with Valsacor.
Meditsinskie novosti. – 2014. – N12. – P. 33 –37.
Артериальная гипертензия (АГ) входит в число самых распространенных заболеваний в мире. Так, частота встречаемости АГ, стандартизированная по полу и возрасту, составляет от 28% в странах Северной Америки до 44% странах Европы [52*]. АГ – важнейший фактор риска, приводящий к развитию таких сердечно-сосудистых заболеваний, как инфаркт миокарда и мозговой инсульт, которые признаются ведущей причиной инвалидности и смертности взрослого населения большинства стран мира [35–37].
Доказательства в пользу назначения антигипертензивных препаратов для снижения риска основных клинических сердечно-сосудистых исходов (фатального и нефатального инсульта, инфаркта миокарда, сердечной недостаточности и других сердечно-сосудистых смертей) у пациентов с АГ были получены в многочисленных рандомизированных клинических исследованиях (РКИ) (в основном плацебо-контролируемых), проведенных в период между 1965 и 1995 годами. Их метаанализ [9] был представлен в рекомендациях ESH/ESC по лечению артериальной гипертензии в 2003 году [2]. Данные, подтверждающие эту точку зрения, свидетельствуют, что регрессия АГ-индуцированных повреждений органов-мишеней, таких как гипертрофия левого желудочка (ГЛЖ) и протеинурия, может сопровождаться снижением фатальных и нефатальных исходов у пациентов с АГ [13, 24].
Основные цели лечения пациентов с АГ – максимальное снижение общего риска, сердечно-сосудистой заболеваемости, сердечно-сосудистых осложнений и смертности [35, 36, 37]. Получение максимальной пользы от лечения антигипертензивными препаратами обычно ассоциируется с достижением пациентом целевого уровня АД.
В опубликованных в 2007 г. «Рекомендациях ESH/ESC по лечению артериальной гипертензии» [35] предлагались два различных целевых уровня артериального давления (АД), а именно <140/90 мм рт. ст. для пациентов с АГ и низким либо умеренным общим сердечно-сосудистым риском и <130/80 мм рт. ст. для пациентов с АГ и высоким либо очень высоким общим сердечно-сосудистым риском (пациенты с сахарным диабетом, сердечно-сосудистыми и цереброваскулярными заболеваниями или заболеваниями почек).
Проведенный в последнее время тщательный анализ имеющихся данных РКИ [55], привел к переоценке отдельных пунктов «Рекомендаций ESH/ESC 2007 г.» [35] и «Дополнений рекомендаций ESH/ESC 2009 г.» [37] в отношении целевых цифр АД у больных сахарным диабетом, сердечно-сосудистыми и цереброваскулярными заболеваниями, заболеваниями почек, а также у пациентов пожилого возраста. «Рекомендации ESH/ESC по лечению артериальной гипертензии 2013 г.» [36] по целевым цифрам АД приведены в таблице.
Таблица. Целевые цифры АД у пациентов с артериальной гипертензией
|
Рекомендации
|
Класс
рекомендации
|
Уровень
доказательности
|
|
Целевой уровень САД <140 мм рт. ст.
а) должен быть рекомендован пациентам
с низким либо умеренным общим сердечно-сосудистым риском;
|
I
|
B
|
|
б) с сахарным диабетом;
|
I
|
A
|
|
с) следует рекомендовать пациентам с ранее перенесенным инсультом или транзиторной
ишемической атакой (ТИА);
|
IIa
|
B
|
|
д) с ишемической болезнью сердца (ИБС);
|
IIa
|
B
|
|
е) с диабетической или не диабетической хронической болезнью почек (ХБП).
|
IIa
|
B
|
|
Пожилым гипертоникам моложе 80 лет с САД ? 160 мм рт. ст. рекомендовано снижение САД
до диапазона между 150 и 140 мм рт. ст.
|
I
|
A
|
|
Пожилым гипертоникам моложе 80 лет может быть рекомендован уровень САД <140 мм рт. ст.
при условии, что в этой уязвимой популяции целевой уровень САД должен быть адаптирован
к индивидуальной переносимости.
|
IIb
|
C
|
|
Пожилым гипертоникам старше 80 лет с исходным САД?? 160 мм рт. ст. рекомендовано
снижение САД до диапазона между 150 и 140 мм рт. ст. при условии, что они находятся
в хорошем физическом и психическом состоянии.
|
I
|
B
|
|
Целевой уровень ДАД <90 мм рт. ст. должен быть рекомендован всем пациентам, за исключением
пациентов с сахарным диабетом, которым рекомендован целевой уровень ДАД <85 мм рт. ст.
Следует отметить, что уровень ДАД от 80 до 85 мм рт. ст. является безопасным
и хорошо переносится.
|
I
|
A
|
П р и м е ч а н и е : САД – систолическое артериальное давление; ДАД – диастолическое артериальное давление.
В «Рекомендациях ESH/ESC по лечению артериальной гипертензии 2013 г.» подтверждается позиция, согласно которой пять классов антигипертензивных препаратов, таких как мочегонные (тиазиды, хлорталидон и индапамид), бета-блокаторы, антагонисты кальция, ингибиторы ангиотензинпревращающего фермента (иАПФ) и антагонисты рецепторов ангиотензина (АРА) могут использоваться и на начальном, и на поддерживающем этапе антигипертензивной терапии либо в качестве монотерапии, либо в некоторых комбинациях [36].
АРА – самый «молодой» из основных классов антигипертензивных препаратов. Включение АРА в арсенал антигипертензивной лекарственной терапии стало важным достижением, поскольку эти препараты способны обеспечить эффективный контроль АД и профилактику сердечно-сосудистых осложнений [11].
Фармакологическая группа сартанов имеет клинические преимущества, которые позволяют широко применять их в терапевтической практике. Ингибирование ангиотензинпревращающего фермента (АПФ) конкурентно и может преодолеваться за счет высокого содержания ангиотензина (АТ) I, который является результатом отрицательной обратной связи ингибирования АТ II на высвобождение ренина. АТ II может продуцироваться независимым АПФ шунтом, с вовлечением химазы. Перечисленные механизмы объясняют недостаточную эффективность и феномен «ускользания антигипертензивного эффекта» иАПФ. Действие АРА II на рецепторы 1 типа высокоспецифично по сравнению с влиянием иАПФ, которые также ингибируют катаболизм кининов, повышая уровень брадикинина, субстанции Р и тахикинина. Накопление этих продуктов (брадикинина, тахикинина) лежит в основе реализации побочных эффектов иАПФ – кашля и ангионевротического отека.
АРА также являются классом препаратов, применяющихся для лечения широкого спектра сердечно-сосудистых заболеваний. Вследствие чрезвычайно широкой распространенности АГ, основного показания для назначения АРА, использование препаратов этой группы достигло высокого уровня. Подсчитано, что около 200 миллионов человек на планете лечатся АРА и что этот класс препаратов охватывает приблизительно 25% назначений антигипертензивных средств. Такая ситуация обусловлена благоприятным отношением к препаратам этой группы как со стороны врачей, так и со стороны пациентов, поскольку АРА лидируют по минимальному количеству побочных эффектов и по переносимости среди сердечно-сосудистых препаратов [10, 15], а также хорошо изучены в клинической и исследовательской практике.
В клинической практике широко используется препарат из группы АРА валсартан. Для валсартана характерен простой фармакокинетический профиль, он является активным препаратом и не требует метаболических превращений.
Антигипертензивная эффективность валсартана. При гипертензии для Валсартана характерна дозозависимая эффективность в снижении как САД, так и ДАД при однократном приеме суточной дозы в диапазоне от 80 до 320 мг. В рандомизированных клинических исследованиях валсартан показал себя как эффективный антигипертензивный препарат в случаях мягкой, умеренной и тяжелой АГ. Результаты РКИ показали, что валсартан эффективен как у мужчин, так и у женщин [5, 49], в том числе в пожилом возрасте [20]. Антигипертензивная эффективность валсартана усиливается при добавлении гидрохлортиазида в дозе от 12,5 до 25 мг. Эффективность комбинированной терапии была продемонстрирована в исследовании [31], в котором сравнивалось снижение АД у пациентов с АГ 2-й и 3-й стадий при титровании валсартана до 160 мг в монотерапии и при комбинации с 12,5 или 25 мг гидрохлортиазида. Снижение САД при монотерапии валсартаном составило 20,7±15,7 мм рт. ст., при комбинированной терапии валсартаном и гидрохлортиазидом – 28,3±13,1 мм рт. ст.
В исследованиях Val-DICTATE (Valsartan Hydrochlorothiazide Diuretic for Initial Control and Titration to Achieve Optimal Therapeutic Effect) [51], MADE -ITT (Metabolic Assessment of Diovan’s Efficacy In Comparison to Thiazide Therapy) [56] также была продемонстрирована эффективность комбинированной терапии валсартаном и гидрохлортиазидом, превышающая эффективность монотерапии у пациентов с различными степенями АГ, в том числе при сочетании АГ с предиабетом и ожирением.
Сравнение с другими антигипертензивными препаратами показало, что валсартан по эффективности снижения АД сопоставим с другими антигипертензивными препаратами: иАПФ, антагонистами кальциевых каналов, ?-адреноблокаторами, диуретиками, но имеет существенно лучшую переносимость [6].
Принципиально важным моментом, характеризующим эффективность любого антигипертензивного средства, является устойчивость гипотензивного эффекта на протяжении всего периода времени между приемами препарата. Для того, чтобы снизить риск сердечно-сосудистых осложнений, антигипертензивная эффективность должна сохраняться на протяжении суток и имитировать нормальный циркадный ритм АД, для которого характерно повышение во время дневной активности и при пробуждении, снижение при отдыхе и во время сна и нарастание во время первых 4–6 часов после пробуждения. Неблагоприятные сердечно-сосудистые события, особенно инфаркты миокарда (ИМ) и цереброваскулярные катастрофы, наиболее часто случаются во время утреннего нарастания АД [29]. Высокое ночное АД или недостаточное снижение АД в ночное время также характеризуется повышенным риском смерти и неблагоприятных сердечно-сосудистых событий [7, 26, 39]. Эти данные подтверждают важность амбулаторного (суточного) мониторирования АД для оценки суточного профиля снижения АД антигипертензивными препаратами, по сравнению с оценкой только офисного АД. Антигипертензивная эффективность монотерапии валсартаном и комбинации валсартан/гидрохлортиазид с использованием суточного амбулаторного мониторирования АД проверена в ряде исследований [12, 22, 41]. Было показано устойчивое снижение АД на протяжении суток как для валсартана, так и для комбинации валсартан/гидрохлортиазид, с сопоставимым уровнем снижения в дневное и ночное время.
Влияние валсартана на сердечно-сосудистые события. В многочисленных РКИ установлено, что валсартан снижает сердечно-сосудистую заболеваемость и смертность у пациентов высокого риска. Так, в исследовании Val-HeFT (Valsartan Heart Failure Trial) [8, 32, 33, 53] у 5010 пациентов с хронической сердечной недостаточностью (ХСН) и документированной дилатацией левого желудочка к получаемой оптимальной терапии ХСН был добавлен валсартан или плацебо. В этом исследовании, продолжавшемся 23 месяца, в группе валсартана на 13% (р=0,009) снизились показатели комбинированной конечной точки (заболеваемость и смертность от всех причин); на 28% (р<0,0001) уменьшилось количество госпитализаций по причине ХСН; достоверно улучшилась сократительная функция левого желудочка и уровень биохимических маркеров ХСН. В исследовании VALIANT (Valsartan in Acute Myocardial Infarction Trial) было показано, что валсартан по сравнению с лечением иАПФ обладает сходным кардиопротективным эффектом у пациентов, перенесших инфаркт миокарда [40]. Так, показатель смертности от всех причин в течение 25 месяцев наблюдения за 14703 пациентами достоверно не различался в группе валсартана и иАПФ. Переносимость терапии в группе АРА оказалась лучшей: достоверно меньше из принимающих валсартан пациентов прекратили терапию по причине побочных эффектов, по сравнению с принимающими каптоприл (5,8% против 7,7%; p<0,05). По результатам исследования VALUE (Valsartan Antihypertensive Long-Term Use Evaluation) [27, 28, 48], группа валсартана и группа амлодипина достоверно не различались (10,6 и 10,4% соответственно) по влиянию на заболеваемость и смертность от сердечно-сосудистых причин в течение 4,2 года наблюдения, несмотря на меньшее снижение АД в группе валсартана (разница на 2,1/1,7 мм рт.ст. на момент окончания исследования; р<0,0001). Однако количество случаев фатальных и нефатальных инфарктов миокарда (ИМ) оказалось несколько выше в группе валсартана (4,8% против 4,1%; р<0,05), что могло быть обусловлено более значимым снижением АД в группе амлодипина (–4,0/–2,1 мм рт.ст., по сравнению с группой валсартана) уже на начальном этапе лечения. Кроме того, максимальная доза валсартана в исследовании была недостаточной и составляла 160 мг, в то время как в настоящее время доза в 320 мг считается наиболее приемлемой; также титрация дозы происходила медленно. Таким образом, недостатки дизайна исследования могли существенно повлиять на полученные результаты. В исследованиях Val-HeFT [34] и VALUE [4, 43] было продемонстрировано достоверное уменьшение случаев возникновения фибрилляции предсердий (ФП).
Влияние валсартана на цереброваскулярные события. Было показано, что валсартан снижает риск инсульта аналогично иАПФ и амлодипину. Как валсартан, так и каптоприл снижали количество неблагоприятных сердечно-сосудистых (в том числе атеросклеротических) событий на 48% у пациентов с перенесенным ИМ в исследовании VALIANT; инсульт случился у 3,6–4,3% пациентов, получавших валсартан, каптоприл или их комбинацию [38, 42]. В исследовании VALUE инсульт случился у 2,9% пациентов, получавших валсартан, и у 2,9% – получавших амлодипин (ОШ 1,02; 95% ДИ 0,81; 1,28; Р=0,899) [48]. Определение когнитивной функции после 18 недель приема валсартана в дозе 160 мг/сут по сравнению с эналаприлом 20 мг/сут у 144 пациентов старческого возраста с АГ показало достоверное повышение индекса (указывающее на улучшение когнитивных функций) у пациентов группы валсартана [16].
Влияние валсартана на функцию почек. Улучшение исхода хронической болезни почек (ХБП) при приеме валсартана заключается в статистически достоверном и клинически значимом уменьшении микроальбуминурии у пациентов с сахарным диабетом 2 типа; причем этот эффект не зависел от степени снижения АД. Нефропротективный эффект валсартана был доказан в исследованиях MARVAL (MicroAlbuminuria Reduction with VALsartan) [47], SMART (Shiga Microalbuminuria Reduction Trial) [46], DROP (Diovan Reduction Of Proteinuria study) [23] и VIVALDI (Study to inVestIgate the efficacy of telmIsartan versus VALsartan in hypertensive type 2 DIabetic patients with overt nephropathy) [19]. Так, в исследовании MARVAL сравнивалось влияние валсартана 80–160 мг/сут и амлодипина 5–10 мг/сут на микроальбуминурию у пациентов с сахарным диабетом 2 типа и АГ. По результатам наблюдения, в течение 24 недель экскреция альбумина с мочой снизилась на 44% в группе валсартана и на 8% в группе альбумина (р<0,001); нормоальбуминурия была достигнута у 30% пациентов в группе валсартана и у 15% в группе амлодипина (р<0,001) при одинаковом уровне снижения АД в группах. Гиперкалиемия при приеме валсартана встречалась редко и не зависела от дозы препарата в диапазоне до 640 мг/сут [23]. Валсартан также эффективен для снижения уровня экскреции белка с мочой у пациентов с почечной недостаточностью, не обусловленной сахарным диабетом. В перекрестном исследовании, в котором пациенты получали валсартан 40–80 мг/сут или плацебо (в течение одного года каждое), в группе валсартана экскреция белка с мочой снизилась на 33% (р<0,001), а в группе плацебо – увеличилась на 32% (р=0,002) [25]. Валсартан не влиял на уровень гемоглобина при ХБП III-IV стадий (при скорости клубочковой фильтрации 15–59 мл/мин/1,73 м2) [14].
Влияние валсартана на метаболизм. В многочисленных РКИ на фоне приема валсартана улучшались или стабилизировались показатели метаболического обмена у пациентов с различными факторами риска и сопутствующими заболеваниями. Так, сенситивность к инсулину улучшалась у пациентов с АГ без ожирения на фоне приема валсартана в дозе 80 мг/сут [45]; у пациентов с АГ и ожирением на фоне приема валсартана в дозе 160 мг/сут [17, 18]; у пациентов с АГ, предиабетом, ожирением и метаболическим синдромом в исследовании MADE -ITT (Metabolic Assessment of Diovan’s Efficacy In Comparison to Thiazide Therapy) [57] на фоне приема валсартана в дозе 320 мг/сут в монотерапии или в комбинации с гидрохлортиазидом в дозе 25 мг/сут. Достоверно улучшались показатели липидного обмена (общий холестерин, холестерин липопротеидов низкой и высокой плотности) у пациентов с АГ или метаболическим синдромом [21, 54]. Также было выявлено уменьшение количества возникновения новых случаев сахарного диабета у пациентов с АГ на 23% в группе приема валсартана по сравнению с группой амлодипина [30, 51]. Последующий анализ исследования VALUE [30] показал, что пациенты, имевшие сахарный диабет на начало исследования, характеризуются двухкратным увеличением сердечно-сосудистой заболеваемости (ИМ и ХСН) и смертности, по сравнению с пациентами без сахарного диабета; пациенты, у которых сахарный диабет развился во время исследования, имели промежуточный риск сердечно-сосудистой заболеваемости и смертности (ОШ 1,43; 95% ДИ 1,16; 1,77, по сравнению с пациентами без сахарного диабета), особенно высоким был риск развития ХСН [3]. Пациенты, у которых развился сахарный диабет во время исследования, имели достоверно более высокий риск возникновения новых случаев ФП и персистирования ФП, чем пациенты без диабета (ОШ 1,49 и 1,87 соответственно; р<0,05 для обоих показателей), что может объяснять увеличение риска развития ХСН.
Актуальность исследования. Уровень контроля АД во всех странах мира оставляет желать лучшего. В странах Европы количество пациентов, не достигающих целевых уровней АД (менее 140/90 мм рт. ст.), варьирует от 59,7% в Англии до 81,3% в Испании. Около 45,5% пациентов с АГ, получающих антигипертензивную терапию в США, не достигают эффективного контроля уровня АД [52]. Согласно Российским данным, только 21,5% леченных пациентов с АГ достигают целевого уровня АД (20,5% мужчин и 22,5% женщин), а у 78,5% пациентов уровень контроля АД остается неэффективным [1, 44].
Для доказательства эффективности и хорошей переносимости широко используемых в западных странах антигипертензивных препаратов и их комбинаций в белорусской популяции было решено провести собственное локальное исследование. В качестве исследуемых антигипертензивных препаратов были выбраны препараты Валсартан (Вальсакор® 80 и 160 мг, KRKA) и фиксированная комбинация Валсартана 80 мг с гидрохлортиазидом 12,5 мг (Вальсакор® Н80, KRKA).
Цель настоящего исследования – оценка антигипертензивной эффективности препаратов Вальсакор® и Вальсакор® Н80 в реальной клинической практике.
Согласно требованиям, предъявляемым к наблюдательным исследованиям, назначение лекарственной терапии осуществлялось строго в соответствии с инструкцией по медицинскому применению препаратов Вальсакор® и Вальсакор® Н80, только по зарегистрированным показаниям к применению и в соответствии с принятой клинической практикой. Решение о назначении лекарственной терапии основывалось только на медицинских показаниях и решении врача и не зависело от желания включить пациента в исследование.
В рамках открытого исследования с последовательным включением пациентов обследовано 50 больных (30 женщин и 20 мужчин) в возрасте 41–77 лет (средний возраст у женщин 64 года, у мужчин 58 лет) с АГ II–III степени, риска 2–4. Критерии исключения из исследования: противопоказания к применению препаратов, указанных в инструкциях к ним (выраженные нарушения функции печени и почек, беременность и период лактации, возраст до 18 лет, повышенная чувствительность к валсартану, гидрохлортиазиду, их производным).
Ишемическую болезнь сердца имели 28 пациентов (18 женщин и 10 мужчин), перенесенный инфаркт миокарда – 10 (6 женщин и 4 мужчин). Хроническая сердечная недостаточность 2–3 функционального класса по NYHA была обнаружена у 7 обследованных (5 женщин и 2 мужчин). Сопутствующие заболевания, такие как сахарный диабет 2 типа имели 6 мужчин, фибрилляцию предсердий – 11 больных (9 женщин и 2 мужчин), заболевания щитовидной железы – 10 пациентов (8 женщин и 2 мужчин).
Медиана САД на момент включения в исследование была 170 мм рт.ст. (25/75 квартили: 160/175 мм рт.ст.), ДАД – 100 мм Hg (100/105 мм рт.ст.). Во всех случаях на фоне комбинированной антигипертензивной терапии (иАПФ, антагонисты кальция, тиазидные диуретики, бета-адреноблокаторы, моксонидин) целевые уровни АД у пациентов не достигались, вследствие чего к лечению добавлялся Вальсакор® (в стартовой дозе 80 мг в сутки – 21 человек; 160 мг в сутки – 18 пациентов) либо Вальсакор® Н80 (при необходимости комбинации с тиазидными диуретиками, 11 человек). Если пациент до включения в исследование принимал иАПФ в оптимальной дозировке в качестве монотерапии либо в комбинации и не достигал целевых цифр АД, то после добавления к лечению валсартана иАПФ отменялись. Средняя длительность наблюдения составила 4 недели. АД измерялось ручным сфигмоманометром-анероидом в положении сидя после пятиминутного отдыха. В отчетные материалы регистрировалось среднее значение АД из трех измерений.
Следующие после включения в исследование контрольные визиты были выполнены на 5–7-е сутки (визит 1), 10–14-е сутки (визит 2) и 28–30-е сутки (визит 3). На каждом визите оценивалось клиническое состояние пациента, величины САД и ДАД, сопутствующая терапия, которая корригировалась при необходимости, а также оценивалась приверженность к лечению, побочные эффекты, нежелательные явления на прием препарата. У трех пациентов на визите 1 и у двух пациентов на визите 2 дозировка Вальсакора® была увеличена с 80 мг до 160 мг в сутки. У остальных пациентов прием препарата продолжался в прежней дозе. Коррекция дозы Вальсакора® Н80 проведена у 2 пациентов на визите 1 путем добавления Вальсакора® в дозировке 80 мг.
Критерием эффективности антигипертензивной терапии являлось достижение целевого уровня АД менее 140/90 мм рт.ст.
Информационная база данных на пациентов была выполнена на основе Excel 2007. Статистический анализ данных выполнен в программе Statistica 7.0 (StatSoft Inc.) с использованием описательной статистики (медиана, 25 и 75 квартили), критерия W Шапиро – Уилка и сравнения двух выборок с помощью критерия Уилкоксона.
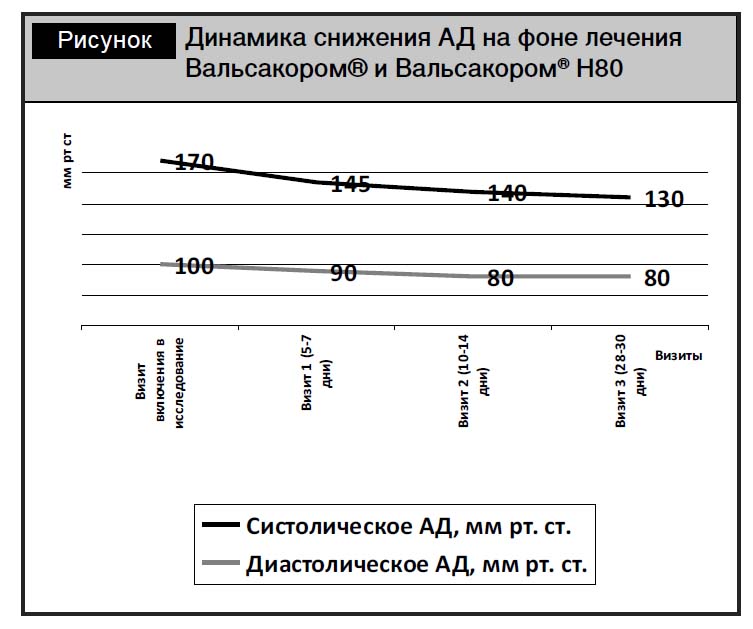
Результаты и обсуждение. При лечении пациентов с АГ II–III степени, риска 2–4 препаратами Вальсакор® и Вальсакор® Н80 удалось добиться выраженного снижения САД и ДАД (рисунок). Уже на визите 1 медиана уровня САД снизилась до 145 (130/150) мм рт. ст., а уровня ДАД – до 90 (80/100) мм рт.ст. При этом у 11 пациентов был достигнут целевой уровень АД. На визите 2 медиана уровня САД составляла 140 (120/140) мм рт. ст., ДАД – 80 (80/90) мм рт. ст. Целевой уровень АД на визите 2 достигнут у 23 пациентов. На визите 3 медиана уровня САД составляла 130 (120/140) мм рт. ст., ДАД – 80 (80/85) мм рт. ст., при достижении целевого уровня АД 38 пациентами. У 12 пациентов целевой уровень АД к окончанию периода наблюдения достигнут не был и составил 140–50/90 –100 мм рт. ст. Исходный уровень АД у этих пациентов составлял 180–190/100–110 мм рт. ст. Это дало основание для дальнейшего наблюдения этих пациентов по окончании исследования для реализации этапной схемы снижения АД, учитывая исходно высокий уровень АД.
В группе пациентов, перенесших ИМ (n=10), контроль АГ был так же эффективен, как и в общей группе.
При анализе достоверности различий при попарном сравнении вариационных рядов (тест Уилкоксона) установлены различия исходного САД и САД на визите 1 (z=6,03; р<0,001); исходного САД и САД на визите 2 (z=6,15; р<0,001); исходного САД и САД на визите 3 (z=6,15; р<0,001). При сравнении аналогичных вариационных рядов по показателю ДАД также установлены достоверные различия на визитах 1 (z=5,235; р<0,001), 2 (z=5,75; р<0,001), и 3 (z=6,09; р<0,001) по сравнению с исходными значениями ДАД.
Гендерных различий в динамике снижения АД обнаружено не было. Феномена «ускользания» антигипертензивного эффекта терапии не отмечалось ни у одного из пациентов. Побочных эффектов и нежелательных явлений в течение 4 недель наблюдения не отмечалось.
Выводы:
1. По результатам проведенного исследования можно сделать заключение, что терапия препаратами Вальсакор® и Вальсакор® Н80 обеспечивает стабильный и длительный антигипертензивный эффект, позволяя в большинстве случаев (76%) достигать целевых уровней артериального давления.
2. Нарастание антигипертензивного эффекта при лечении препаратами Вальсакор® и Вальсакор® Н80 происходит постепенно, достигая максимума на 4-й неделе лечения. В то же время на 5–7-й день назначения препарата наблюдается стабильное и выраженное антигипертензивное действие препарата при отсутствии эпизодов гипотонии.
3. Переносимость препаратов Вальсакор® и Вальсакор® Н80 у всех пациентов была хорошая, приверженность к лечению – высокая.
Л И Т Е Р А Т У Р А
1. Шальнова, С. А. Артериальная гипертония: распространенность, осведом-ленность, прием антигипертензивных препаратов и эффективность лечения среди населения Российской Федерации / С.А. Шальнова, Ю.А. Баланова, В.В. Константинов // Рос. кардиол. журн. – 2006. – Т.60, №4. – С.45–50.
2. 2003 European Society of Hypertension – European Society of Cardiology guidelines for the management of arterial hypertension // J. Hypertens. – 2003. – Vol.21, N6. – P.1011–1053.
3. Aksnes, T.A. Impact of new-onset diabetes mellitus on cardiac outcomes in the Valsartan Antihypertensive Long-term Use Evaluation (VALUE) trial population / T.A.Aksnes, S.E.Kjeldsen, M.Rostrup [et al.] // Hypertension. – 2007. – Vol.50, N3. – P.467–473.
4. Aksnes, T.A. Impact of new-onset diabetes mellitus on development of atrial fibrillation and heart failure in high-risk hypertension (from the VALUE Trial) / T.A.Aksnes, R.E.Schmieder, S.E.Kjeldsen [et al.] // Am. J. Cardiol. – 2008. – Vol.101, N5. –P. 634–638.
5. Black, H.R. Valsartan, a new angiotensin II antagonist for the treatment of hypertension: efficacy, tolerability and safety compared to an angiotensin-converting enzyme inhibitor, lisinopril / H.R.Black, A.Graff, D.Shute [et al.] // J. Hum. Hypertens. – 1997. – Vol.11. – P.483–489.
6. Black, H.R. Valsartan: More Than a Decade of Experience / H.R.Black, J.Bailey, D.Zappe [et al.] // Drugs. – 2009. – Vol.69, N17. – P.2393–2414.
7. Boggia, J. Prognostic accuracy of day versus night ambulatory blood pressure: a cohort study / J.Boggia, Y.Li, L.Thijs [et al.] // Lancet. – 2007. – Vol.370, N9594. – P.1219–1229.
8. Cohn, J.N. A randomized trial of the angiotensin–receptor blocker valsartan in chronic heart failure / J.N.Cohn, G.Tognoni // N. Engl. J. Med. – 2001. – Vol.345, N23. – P.1667–1675.
9. Collins, R. Blood pressure, antihypertensive drug treatment and the risks of stroke and of coronary heart disease / R.Collins, S.MacMahon // Br. Med. Bull. – 1994. – Vol.50. – P.272–298.
10. Corrao, G. Discontinuation of and changes in drug therapy for hypertension among newly treated patients: a population–based study in Italy / G.Corrao, A.Zambon, A.Parodi [et al.] // J. Hypertens. – 2008. – Vol.26. – P.819–824.
11. Dahlöf, B. Cardiovascular morbidity and mortality in the Losartan Intervention For Endpoint reduction in hypertensive study (LIFE): a randomized trial against atenolol / B.Dahlöf, R.B.Devereux, S.E.Kjeldsen [et al.] // Lancet. – 2002. –Vol.359. – P.995–1003.
12. Destro, M. Comparative efficacy of valsartan and olmesartan in mild-to-moderate hypertension: results of 24-hour ambulatory blood pressure monitoring / M.Destro, R.Scabrosetti, A.Vanasia [et al.] //Adv. Ther. – 2005. – Vol.22, N1. – P.32–43.
13. Devereux, R. B. Prognostic signi?cance of left ventricular mass change during treatment of hypertension / R.B.Devereux, K.Wachtell, E.Gerdts [at al.] // JAMA. – 2004. – Vol.292. – P.2350–2356.
14. Durmus, A. Effect of valsartan on erythropoietin and hemoglobin levels in stage III–IV chronic kidney disease patients / A.Durmus, E.Dogan, R.Erkoc, [et al.] // Int. J. Clin. Pract. – 2005. – Vol.59, N9. – P.1001–1004.
15. Elliott, W. J. Persistence, adherence, and risk of discontinuation associated with commonly prescribed antihypertensive drug monotherapies / W.J.Elliott, C.A.Plauschinat, G.H.Skrepnek [et al.] // J. Am. Board. Fam. Med. – 2007. – Vol.20. – P.72–80.
16. Fogari R., Effects of Valsartan compared with enalapril on blood pressure and cognitive function in elderly patients with essential hypertension / R.Fogari, A.Mugellini, A.Zoppi [et al.] // Eur. J. Clin. Pharmacol. – 2004. – Vol.59, N12. – P.863–868.
17. Fogari, R. Comparison of the effects of valsartan and felodipine on plasma leptin and insulin sensitivity in hypertensive obese patients / R.Fogari, G.Derosa, A.Zoppi [et al.] // Hypertens. Res. – 2005. – Vol.28, N3. – P.209–214.
18. Fogari, R. Effect of Valsartan on adiponectine, leptin and resistine in hypertensive obese patients [abstr. no. P-521] / R.Fogari, G.Derosa, A.Mugellini [et al.] // Am. J. Hypertens. –2005. – Vol.18, S4. – P.196A–197A.
19. Galle, J. Antiproteinuric effects of angiotensin receptor blockers: telmisartan versus valsartan in hypertensive patients with type 2 diabetes mellitus and overt nephropathy / J.Galle, E.Schwedhelm, S.Pinnetti [et al.] // Nephrol. Dial. Transplant. – 2008. – Vol.23, N10. – P.3174–3183.
20. Hall, J. Long-term safety, tolerability and efficiacy of valsartan: results from one and two year trials / J.Hall, T.Marbury, J.Grey [et al.] // J. Clin. Res. – 1998. – Vol.1. – P.147–159.
21. Hanefeld, M. Effect of the angiotensin II receptor antagonist valsartan on lipid profile and glucose metabolism in patients with hypertension / M.Hanefeld, C.Abletshauser // J. Int. Med. Res. – 2001. – Vol.29, N4. – P.270–279.
22. Hermida, R.C. Administration time-dependent effects of valsartan on ambulatory blood pressure in hypertensive subjects / R.C.Hermida, C.Calvo, D.E.Ayala [et al.] // Hypertension. – 2003. –Vol.42, N3. – P.283–290.
23. Hollenberg, N. K. Albuminuria response to very high-dose valsartan in type 2 diabetes mellitus / N.K.Hollenberg, H.H.Parving, G.Viberti [et al.] // J. Hypertens. – 2007. –Vol.25, N9. – P.1921–1926.
24. Ibsen, H. Reduction in albuminuria translates to reduction in cardiovascular events in hypertensive patients: losartan intervention for endpoint reduction in hypertension study / H.Ibsen, M.H.Olsen, K.Wachtell [at al.] // Hypertension. – 2005. – Vol.45. – P.198 –202.
25. Ishimitsu, T. Effects of valsartan on the progression of chronic renal insufficiency in patients with nondiabetic renal diseases / T.Ishimitsu, T.Kameda, A.Akashiba [et al.] // Hypertens. Res. – 2005. – Vol.28, N11. – P.865–870.
26. Izzedine, H. Abnormal blood pressure circadian rhythm: a target organ damage? / H.Izzedine, V.Launay-Vacher, G.Deray // Int. J. Cardiol. – 2006. – Vol.107. – P.343–349.
27. Julius S., The Valsartan Antihypertensive Long-Term Use Evaluation (VALUE) trial: outcomes in patients receiving monotherapy / S.Julius, M.A.Weber, S.E.Kjeldsen [et al.] // Hypertension. – 2006. – Vol.48. – P.385–391.
28. Julius, S. Outcomes in hypertensive patients at high cardiovascular risk treated with regimens based on valsartan or amlodipine: the VALUE randomised trial / S.Julius, S.E.Kjeldsen, M.Weber, [et al.] // Lancet. – 2004. – Vol.363, N9426. – P.2022–2031.
29. Kario, K. Morning surge in blood pressure as a predictor of silent and clinical cerebrovascular disease in elderly hypertensives: a prospective study / K.Kario, T.G.Pickering, Y.Umeda [et al.] // Circulation. – 2003. – Vol.107. – P.1401–1406.
30. Kjeldsen, S. E. Effects of Valsartan compared to amlodipine on preventing type 2 diabetes in high-risk hypertensive patients: the VALUE trial / Kjeldsen S.E., Julius S., Mancia G. [et al.] // J. Hypertens. – 2006. – Vol.24. N7. – P.1405–1412.
31. Lacourciere, Y. Antihypertensive efficacy and tolerability of two fixed-dose combinations of valsartan and hydrochlorothiazide compared with valsartan monotherapy in patients with stage 2 or 3 systolic hypertension: an 8-week, randomized, double-blind, parallel-group trial / Y.Lacourciere, L.Poirier, D.Hebert [et al.] // Clin. Ther. – 2005. – Vol.27, N7. – P.1013–1021.
32. Latini, R. Effects of valsartan on circulating brain natriuretic peptide and norepinephrine in symptomatic chronic heart failure: the Valsartan Heart Failure Trial (Val–HeFT) / R. Latini, S. Masson, I. Anand, [et al.] // Circulation. – 2002. – Vol.106, N19. – P.2454–2458.
33. Maggioni, A.P. Effects of valsartan on morbidity and mortality in patients with heart failure not receiving angiotensin–converting enzyme inhibitors / A.P.Maggioni, I.Anand, S.O.Gottlieb [et al.] // J. Am. Coll. Cardiol. – 2002. – Vol.40, Issue 8.– P.1414–1421.
34. Maggioni, A.P. Valsartan reduces the incidence of atrial fibrillation in patients with heart failure: results from the Valsartan Heart Failure Trial (Val–HeFT) / A.P.Maggioni, R.Latini, P.E.Carson [et al.] // Am. Heart. J. – 2005. – Vol.149, N3. – P.548–557.
35. Mancia, G. 2007 Guidelines for the Management of Arterial Hypertension: The Task Force for the Management of Arterial Hypertension of the European Society of Hypertension (ESH) and of the European Society of Cardiology (ESC) / G.Mancia, G.De Backer, A.Dominiczak [at al.] // J. Hypertens. – 2007. – Vol.25. – P.1105–1187.
36. Mancia, G. 2013 ESH/ESC Guidelines for the management of arterial hypertension: the Task Force for the management of arterial hypertension of the European Society of Hypertension (ESH) and of the European Society of Cardiology (ESC) / G.Mancia, R.Fagard, K.Narkiewicz [at al.] // J. Hypertens. – 2013. – Vol.31, N7. – P.1281–1357.
37. Mancia, G. Reappraisal of European guidelines on hypertension management: a European society of hypertension task force document / G.Mancia, S.Laurent, E.Agabiti-Rosei [at al.] // J. Hypertens. – 2009. – Vol.27. – P.2121–2158.
38. McMurray, J. The effect of valsartan, captopril, or both on atherosclerotic events after acute myocardial infarction: an analysis of the Valsartan in Acute Myocardial Infarction Trial (VALIANT) / J.McMurray, S.Solomon, K.Pieper [et al.] // J. Am. Coll. Cardiol. – 2006. – Vol.471, N4. – P.726–733.
39. Pedersen, O.L. Ambulatory blood pressure monitoring after 1 year on valsartan or amlodipine-based treatment: a VALUE substudy / O.L.Pedersen, G.Mancia, T.Pickering [et al.] // J. Hypertens. – 2007. – Vol.25, N3. – P.707–712.
40. Pfeffer, M.A. Valsartan, captopril, or both in myocardial infarction complicated by heart failure, left ventricular dysfunction, or both / M.A.Pfeffer, J.J.McMurray, E.J.Velazquez [et al.] // N. Engl. J. Med. – 2003. – Vol.349, N20. – P.1893–1906.
41. Ruilope, L.M. 24-Hour ambulatory blood-pressure effects of valsartan and hydrochlorothiazide combinations compared with amlodipine in hypertensive patients at increased cardiovascular risk: a VAST sub-study / L.M.Ruilope, D.Heintz, A.A.Brandao [et al.] // Blood Press. Monit. – 2005. – Vol.10, N5. – P.85–91.
42. Sampson, U. K. Predictors of stroke in high-risk patients after acute myocardial infarction: insights from the VALIANT trial / U.K.Sampson, M.A.Pfeffer, J.J.McMurray [et al.] // Eur. Heart. J. – 2007. – Vol.28. – P.685–691.
43. Schmieder, R.E. Reduced incidence of new-onset atrial fibrillation with angiotensin II receptor blockade: the VALUE trial / R.E.Schmieder, S.E.Kjeldsen, S.Julius [et al.] // J. Hypertens. – 2008. – Vol.26, N3. – P.403–411.
44. Shalnova, S.A. Monitoring arterial hypertension in Russia / S.A.Shalnova, A.A.Deev, R.G.Oganov // Circulation. – 2006. – Vol.113, N21. – P.83–84.
45. Top, C. The effects of valsartan on insulin sensitivity in patients with primary hypertension / C.Top, B.Y.Cingozbay, H.Terekeci [et al.] // J. Int. Med. Res. – 2002. – Vol.30, N1. – P.15–20.
46. Uzu, T. Reduction of microalbuminuria in patients with type 2 diabetes: the Shiga Microalbuminuria Reduction Trial (SMART) / T.Uzu, M.Sawaguchi, H.Maegawa [et al.] // Diabetes Care. – 2007. – Vol.30, N6. – P.1581–1583.
47. Viberti, G. Microalbuminuria reduction with valsartan in patients with type 2 diabetes mellitus: a blood pressure-independent effect / G.Viberti, N.M.Wheeldon // Circulation. – 2002. – Vol.106, N6. – P.672–678.
48. Weber, M. A. Blood pressure dependent and independent effects of antihypertensive treatment on clinical events in the VALUE Trial / M.A.Weber, S.Julius, S.E.Kjeldsen, [et al.] // Lancet. – 2004. – Vol.363, N9426. – P.2049–2051.
49. Weir, M.R. Valsartan alone or with diuretic or ACE inhibitor for treatment for African American hypertensives: relation to salt-intake / M.R.Weir, D.H.Smith, J.M.Neutel, [et al.] // Am. J. Hypertens. – 2001. – Vol.14. – P.665–671.
50. Weycker, D. Risk of diabetes in a real-world setting among patients initiating antihypertensive therapy with valsartan or amlodipine / D.Weycker, J.Edelsberg, G.Vincze [et al.] // J. Hum. Hypertens. – 2007. – Vol.21, N5. – P.374–380.
51. White, W. B. Improving blood pressure control: increase the dose of diuretic or switch to a fixed-dose angiotensin receptor blocker/diuretic? The valsartan hydrochlorothiazide diuretic for initial control and titration to achieve optimal therapeutic effect (Val–DICTATE) trial / W.B.White, D.A.Calhoun, R.Samuel [et al.] // J. Clin. Hypertens. (Greenwich). – 2008. – Vol.10, N6. – P.450–458.
52. Wolf-Maier, K. Hypertension prevalence and blood pressure levels in 6 European countries, Canada, and the United States / K. Wolf-Maier, R.S.Cooper, J.R.Banegas, [at al.] // JAMA. – 2003. – Vol.289. – P.2363–2369.
53. Wong, M. Valsartan benefits left ventricular structure and function in heart failure: Val-HeFT echocardiographic study / M.Wong, L.Staszewsky, R.Latini [et al.] // J. Am. Coll. Cardiol. – 2002. – Vol.40, N5. – P.970–975.
54. Yilmaz, M. I. Effect of antihypertensive agents on plasma adiponectin levels in hypertensive patients with metabolic syndrome / M.I.Yilmaz, A.Sonmez, K.Caglar [et al.] // Nephrology (Carlton). – 2007. – Vol.12, N2. – P.147–153.
55. Zanchetti, A. When should antihypertensive drug treatment be initiated and to what levels should systolic blood pressure be lowered? A critical reappraisal / A.Zanchetti, G.Grassi, G.Mancia // J. Hypertens. – 2009. – Vol.27. – P.923–934.
56. Zappe, D. H. Metabolic and antihypertensive effects of combined angiotensin receptor blocker and diuretic therapy in prediabetic hypertensive patients with the cardiometabolic syndrome / D.H.Zappe, J.R.Sowers, W.A.Hsueh [et al.] // J. Clin. Hypertens. (Greenwich). – 2008. – Vol.10, N12. – P.894–903.
Медицинские новости. – 2014. – №12. – С. 33-37.
Внимание! Статья адресована врачам-специалистам. Перепечатка данной статьи или её фрагментов в Интернете без гиперссылки на первоисточник рассматривается как нарушение авторских прав.