Bezrukov S.G., Saenko T.S.
Crimea State Medical University named after S.I. Georgievsky, Simferopol, Ukraine
Clinical evaluation of flow-thermometrical local inflammatory reactions at the site of injection augmentation
of the alveolar ridge in patients with generalized paradontitis
Резюме. Проанализированы показатели локальной термометрии у больных с генерализованным пародонтитом I–II степеней на фоне комплексного лечения с применением обогащенной тромбоцитами плазмы крови – PRP-геля (1-я группа) и комбинации PRP с Биомином ГТлС (2-я группа). Выявлены достоверные различия (P<0,05) в активности и продолжительности местных воспалительных реакций, наименее выраженными они были у пациентов 2-й группы.
Ключевые слова: инъекционная аугментация альвеолярного отростка,локальная термометрия, генерализованный пародонтит, PRP-гель, Биомин ГТлС, комплексное лечение пародонтита.
Современная стоматология. – 2013. – №2. – С. 91–93.
Summary. Analysis of indicators local thermometry in patients with generalized paradontitis I–II degree, conducted against the background of a complex treatment with PRP-gel in the 1st and the combination with PRP Biomin GTlS in the 2nd main groups revealed significant differences (at P<0,05 ) in potency and duration of local inflammatory responses, which were less pronounced in patients 2nd main group.
Keywords: injection augmentation of the alveolar ridge,local thermometry, generalized paradontitis, PRP-gel, Biomin GTlS, complex treatment of paradontitis.
Sovremennaya stomatologiya. – 2013. – N2. – P. 91–93.
Распространенность заболеваний пародонта продолжает демонстрировать тенденцию к росту, и поэтому проблема повышения эффективности составляющих элементов комплексного лечения сохраняет свою значимость. В современной хирургической стоматологической практике активно используются остеопластические материалы. Для оптимизации процессов регенерации все чаще применяется обогащенная тромбоцитами плазма крови (PRP) [6, 4]. Она широко используется при проведении остеопластических операций (синус-лифтинг, аугментация альвеолярного отростка), для обработки операционного ложа перед дентальной имплантацией и др. [4]. Доказано, что PRP оказывает выраженное остеоиндуктивное действие. Также в комплексном лечении генерализованного пародонтита целесообразно использовать остеокондукторы [2], которые позволяют увеличить объем костной ткани. На медицинском рынке расширился выбор отечественных (украинских) синтетических остеопластических (остеокондуктивных) препаратов. Один из них – содержащий серебро материал «Биомин ГТлС».
Все проводимые хирургические манипуляции, в том числе малоинвазивные и инъекционные способы лечения, сопровождаются развитием местного воспалительного процесса, что обусловлено эндо- и экзотермическими биохимическими реакциями в зоне травмы, расстройством механизма терморегуляции в поврежденной области тела, нарушением кровообращения [5]. Активность и длительность воспалительных реакций непосредственно влияют на течение восстановительного процесса, что определяет их диагностическое и прогностическое значение [5]. В связи с этим метод локальной термометрии представляется объективным и информативным для контроля за эффективностью комплексного лечения больных с генерализованным пародонтитом [1].
Цель исследования – проследить динамику показателей локальной термометрии у больных в группах сравнения в процессе комплексного лечения генерализованного пародонтита I–II степеней, включающего инъекционное введение остеопластических материалов.
Материалы и методы
Лечение проводилось амбулаторно, в хирургическом кабинете поликлиники. Анализировали изменения клинических и термометрических показателей, зафиксированных в процессе лечения и обследования 120 пациентов обоего пола в возрасте от 20 до 50 лет (40 больных в 1-й основной группе, 40 – во 2-й основной и 40 – в контрольной).
В контрольной группе проводили традиционное комплексное лечение генерализованного пародонтита I–II степеней с инъекционным введением экстракта алоэ в мягкие ткани по переходной складке в проекции причинных зубов.
В 1-й основной группе традиционный способ лечения усиливали инъекционным точечным под- и наднадкостничным введением PRP.
Во 2-й основной группе комплексное лечение дополняли инъекционной сочетанной остеопластической терапией тканей пародонта PRP-гелем и взвесью препарата «Биомин ГТлС». Их вводили раздельно, точечно, в ткани пародонта из расчета по 0,3 мл в проекции одного зубного сегмента. Манипуляцию выполняли под инфильтрационной анестезией 0,5% раствором лидокаина.
Температурные данные регистрировали до манипуляции, а также на 1-е, 3-и, 5-е и 7-е сутки после нее. Термометрию тканей пародонта выполняли электронным термометром GoldTemp Thermometer MT 1622 (Microlife, Швейцария) с золотым гипоаллергенным покрытием наконечника, позволяющим измерять температуру с точностью до 0,01 градуса C. Измерения проводили в условиях стоматологического хирургического кабинета, к которым пациент предварительно адаптировался в течение 10–15 минут. Температура воздуха в процедурном кабинете составляла 20–22 градуса C [3].
Контакт датчика со слизистой оболочкой альвеолярного отростка (с вестибулярной стороны) в проекции зоны инъекционного введения лекарственных препаратов сохраняли в течение 1–2 минут до появления на жидкокристаллическом дисплее окончательных и неизменяющихся значений температуры и звукового сигнала термометра. Следующее измерение проводили после сброса со шкалы прибора предыдущих данных. Показатели снимали в трех точках, которые располагались на одинаковом расстоянии друг от друга, поочередно с каждой стороны, используя одинаковую силу давления на ткани, по 3 раза в каждой, с интервалом между измерениями 5–7 секунд.
Показатели суммировали и вычисляли среднее значение. Для сравнения полученных данных аналогичные замеры проводили на симметричных участках здоровой слизистой оболочки альвеолярного отростка челюсти с противоположной стороны. В дальнейшем высчитывали средний показатель для всей исследуемой зоны. Результаты выражались в градусах Цельсия (градус C) и заносились в карту наблюдений.
Результаты и обсуждение
При обсуждении результатов термометрии за норму (исходный уровень) принимали средний показатель локальной температуры маргинальной и альвеолярной десны здорового человека в проекции планируемого инъекционного вмешательства, который составил 36,37±0,14°C. Исходя из данных литературы, в норме температура слизистой оболочки десны колеблется в пределах 35,7–37,3 °C [1].
Прогрессирующий рост температуры в зоне инъекции препаратов отмечался у представителей всех групп сравнения уже через сутки после вмешательства. В 1-й основной группе она выросла на 2,22 °C по сравнению с исходным уровнем, составив 38,59±0,09 °C, во второй основной группе – на 2,21 °C (38,52± 0,09 °C), в контрольной – на 2,47 °C (38,89±0,06 °C). Выявленные различия (с исходным уровнем) достоверны (P1<0,05) (табл. 1).
Таблица. Динамика изменений показателя локальной термометрии в двух основных и контрольной группах, М ± m, °C
|
Группа
|
Исходный уровень
|
Сроки наблюдений (сутки после операции)
|
|
1-е
|
3-и
|
5-е
|
7-е
|
|
1-я основная
(БТП)
(n = 40)
|
36,37±0,14
|
38,59±0,09
|
37,05±0,11
|
36,78±0,12
|
36,52±0,09
|
|
Р1<0,05
|
Р1>0,05
|
Р1>0,05
|
Р1>0,05
|
|
Р2>0,05
|
Р2>0,05
|
Р2>0,05
|
Р2>0,05
|
|
Р3>0,05
|
Р3<0,05
|
Р3<0,05
|
Р3>0,05
|
|
2-я основная
(БТП +
Биомин ГТлС)
(n = 40)
|
36,37±0,14
|
38,52±0,09
|
36,40±0,12
|
36,38±0,11
|
36,35±0,10
|
|
Р1<0,05
|
Р1>0,05
|
Р1>0,05
|
Р1>0,05
|
|
Р2>0,05
|
Р2>0,05
|
Р2>0,05
|
Р2>0,05
|
|
Р4>0,05
|
Р4<0,05
|
Р4<0,05
|
Р4>0,05
|
|
Контрольная
(n = 40)
|
36,37±0,14
|
38,89±0,06
|
39,13±0,08
|
38,37±0,12
|
37,06±0,11
|
|
Р1< 0,05
|
Р1< 0,05
|
Р1< 0,05
|
Р1> 0,05
|
|
Р3> 0,05
|
Р3< 0,05
|
Р3< 0,05
|
Р3> 0,05
|
|
Р4> 0,05
|
Р4< 0,05
|
Р4< 0,05
|
Р4> 0,05
|
П р и м е ч а н и е : Р1 – степень достоверности по отношению к исходному уровню; Р2 – степень достоверности между 1-й и 2-й основными группами; Р3 – степень достоверности между 1-й основной и контрольной группами;Р4 – степень достоверности между 2-й основной и контрольной группами.
На 3-и сутки в контрольной группе локальная температура в зоне инъекции составила 39,13±0,08 ?C, т.е., по сравнению с нормой повысилась до максимальной отметки (на 2,76 градус C) (P1<0,05). В первой основной группе показатель снизился до 37,05±0,11 градус C, во второй – до 36,40±0,12 градус C (P1>0,05; P2<0,05). Таким образом, температурные индексы в основных группах существенно приблизились к исходным (P>0,05).
К 5-м суткам температурный показатель в первой основной группе составил 36,78±0,12 градус C, во второй основной группе – 36,38±0,11 градус C, в контрольной – 38,37±0,12 градус C. Различия между 1-й основной и контрольной составили 1,59 градус C (P<0,05), между 2-й основной и контрольной – 0,66 градус C (P< 0,05), между основными группами – 0,4 градус C (P>0,05). В целом цифры стали снижаться (см. таблицу), но динамика изменений была различной. В основных группах температура уже соответствовала нормативному показателю (36,37±0,14 градус C). По сравнению с исходным уровнем различия были недостоверными (P>0,05). В контроле разница (2 градус C) оставалась значимой (P<0,05).
На 7-е сутки цифровые значения практически приблизились к уровням, имевшим место до инъекционной терапии (при P>0,05), причем эта тенденция была больше выражена во второй основной группе (36,35±0,10 градус C), чем в первой (36,52±0,09 градус C) и контрольной (37,06±0,11 градус C).
В первой основной группе колебания локальной температуры в течение 7-дневного послеинъекционного периода находились в пределах 0,15–2,22 градус C, во второй основной группе – 0,02–2,15 градус C, в контрольной – 0,69–2,52 градус C. На 3-й день разрыв между контрольной и 1-й основной группами достиг 2,08 градус C, контрольной и 2-й основной группами – 2,73 градус C, между двумя основными группами – 0,65 градус C. На 5-е сутки между контрольной и основными группами (1-й и 2-й) – 1,59 и 1,99 градус C соответственно, разрыв между двумя основными группами составил 0,4 градус C. Лишь к 7-му дню разница соответствовала 0,54 градус C между контрольной и 1-й основной группами, 0,71 градус C между контрольной и 2-й основной группами и 0,17 градус C между двумя основными группами в пользу 2-й основной группы. Более наглядно эти результаты отображают графические кривые (рисунок).
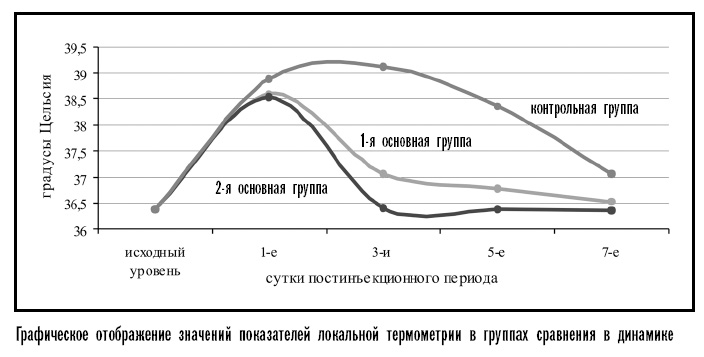
Таким образом, на основании анализа результатов, полученных в этом фрагменте исследования, отмечено, что инъекционное применение PRP-геля (1-я основная группа) и комбинации PRP с Биомином ГТлС (2-я основная группа) сокращает продолжительность периода локальной гипертермии, оптимизируя течение восстановительных процессов в раннем послеинъекционном периоде у больных с хроническим генерализованным пародонтитом I–II степеней тяжести, что более выраженно проявляется во 2-й основной группе.
На наш взгляд, это объясняется тем, что обогащенная тромбоцитами плазма крови позволяет создать в участке ее инъекционного введения высокую концентрацию факторов роста, управляющих местными процессами регенерации. Кроме того, она является биостимулятором, обладает иммунокорригирующим, противовоспалительным и остеоиндуктивным эффектами. Биомин ГТлС – остеопластический материал с остеокондуктивным воздействием, содержит серебро, которое оказывает местное антимикробное и противовоспалительное действие.
Данные, полученные на 3-и и 5-е сутки наблюдений с помощью локальной термометрии, выявили достоверные различия в активности и продолжительности течения развивающихся на фоне инъекционной терапии местных воспалительных реакций у пациентов двух основных и контрольной групп (P<0,05), они наименее выражены у представителей 2-й основной группы. В комплекс лечения этих пациентов была включена инъекционная сочетанная остеопластическая терапия тканей пародонта PRP-гелем и взвесью препарата «Биомин ГТлС».
Л И Т Е Р А Т У Р А
1. Данилевский Н.Ф., Борисенко А.В. Заболевания пародонта. – Киев: Здоров’я, 2000. – 464 с.
2. Павленко А.В., Бугоркова И.А. // Соврем. стоматология. – 2006. – №3. – С.45–48.
3. Подвысоцкий А.А., Лобенко А.А. // Диагностическая и терапевтическая аппаратура рефлексотерапии и биофизические методы диагностики: Сб. тез. – Калинин, 1983. – С.100–105.
4. Робустова Т.Г. Имплантация зубов (хирургические аспекты). – М.: Медицина, 2003. – 560 с.
5. Фенчин К.М. Заживление ран. – К.: Здоров’я, 1979. – 168 с.
6. 16th Annual Meeting Academia Osseointegration, March 22–24, 2001. – Toronto, Canada, 2001. – 354 p.
Статья размещена на сайте www.mednovosti.by (Архив СС) и может быть скопирована в формате Word.
Современная стоматология. – 2013. – №2. – С. 91-93
Внимание! Статья адресована врачам-специалистам. Перепечатка данной статьи или её фрагментов в Интернете без гиперссылки на первоисточник рассматривается как нарушение авторских прав.