Kazayeu S.Ya., Stsepura L.I.
Republic Scientific-Practical Center of Traumatology and Orthopedics, Minsk
Medical device on the basis of hyaluronic acid HI-FLEX in posttraumatic knee joint osteoarthrosis
Резюме. На базе РНПЦ травматологии и ортопедии в 2010–2011 гг. было обследовано 60 пациентов в возрасте от 17 до 56 лет (45 мужчин, 15 женщин) с посттравматическим остеоартрозом коленных суставов I–III стадий по Келлгрену. Всем пациентам Хай-ФЛЕКС вводился внутрь пораженного сустава 1 раз в неделю трехкратно (1-е, 8-е и 15-е сутки) в дозе 20 мг. Клиническая оценка эффективности препарата осуществлялась сразу после курса лечения, через 3 и 6 месяцев. Клинический эффект от внутрисуставного введения Хай-ФЛЕКСа сохранялся на протяжении 3 месяцев наблюдения, а через 6 месяцев, хотя и выявлено незначительное изменение анализируемых показателей,в среднем по группе они были лучше, чем до лечения, что свидетельствует о длительном сохранении терапевтического эффекта. Таким образом, применение раствора для внутрисуставного введения Хай-ФЛЕКС приводит к статистически значимому увеличению физической составляющей качества жизни пациентов, замедлению прогрессирования данного заболевания, а также позволяет в будущем снизить вероятность выхода пациентов на инвалидность.
Ключевые слова: Хай-ФЛЕКС, остеоартроз, коленный сустав, внутрисуставное введение.
Summary. 60 patients aged between 17–56 years (45 men, 15 women) with posttraumatic knee joint OA at I–III stages according to Kellgren were examined at the Republic Scientific-Practical Center of Traumatology and Orthopedics in 2010–2011. Hi-FLEX was administered into an affected joint to all the patients at a dose 20 mg three times once a week (1st, 8th and 15th day). Medical device efficiency was evaluated after therapy at once as well as in 3 and 6 months. The clinical effect after Hi-FLEX intra-articular administration remained during 3 months of observation. Although a slight change in the laboratory parameters was marked after 6 months, on the average for the group they were better than before the therapy. This fact proves a stable therapeutic effect. Thus, solution for intra-articular injections Hi-FLEX increases the physical component of patient life quality significantly, slows down the disease progression as well as in future allows to reduce a probability of patients disability.
Keywords: Hi-FLEX, osteoarthrosis, knee joint, intra-articular administration.
В отечественной медицинской литературе остеоартроз (ОА) определяется как «хроническое прогрессирующее невоспалительное заболевание суставов, характеризующееся дегенерацией суставного хряща и структурными изменениями субхондральной кости, а также явно или скрыто протекающим умеренно выраженным синовитом» [6].
Среди всех нозологических форм патологии суставов остеоартроз составляет 55%. По данным эпидемиологических исследований, остеоартрозом различной локализации страдают 1–2% населения до 45 лет и 15–85% людей старшего возраста [3]. Рентгенологические признаки ОА наблюдаются почти у всех лиц старше 60 лет, а клинические проявления остеоартроза имеют место у 10–20% из них [18].
Актуальность проблемы лечения остеоартроза определяется не только высокой распространенностью заболевания, но и его высокой социально-экономической значимостью: в последнее десятилетие показатель нетрудоспособности населения в связи с артрозом увеличился в 3 раза [4].
Одной из наиболее частых локализаций является остеоартроз коленного сустава (КС), встречающийся, по данным некоторых авторов, у 50–70% пациентов с дегенеративно-дистрофическими заболеваниями суставов, поражая до 10–12% взрослого населения [2]. По тяжести нарушения функции опорно-двигательного аппарата и ухудшению качества жизни остеоартроз КС занимает одно из ведущих мест. Повреждения этой локализации приводят к стойкой утрате трудоспособности в 9–11% случаев (Sutton A.J., 2001), причём две трети случаев составляют лица трудоспособного возраста от 40 до 60 лет [2].
В структуре причин ОА КС одну из ведущих позиций занимают травмы коленного сустава, составляющие до 68% всех случаев ОА коленного сустава [2].
Независимо от этиологии ОА (первичный или вторичный) в коленном суставе отмечается однотипность биохимических изменений, приводящих к стойким нарушениям механической резистивности пораженного сустава и развитию вторичного хронического воспалительного процесса в синовиальной оболочке и параартикулярных тканях [3]. Возникновение боли – один из ведущих симптомов ОА. Так, при поражении субхондральной кости боль развивается из-за возникновения внутрикостной гипертензии и микропереломов, сформировавшиеся остеофиты травмируют чувствительные нервы, а поражение периартикулярных мышц сопровождается их спазмом. Однако ведущая причина боли – воспаление, которое имеет первостепенное значение в развитии и прогрессировании ОА [1].
В настоящее время сформулированы основные принципы лечения остеоартроза коленного сустава [26]. Оптимальное лечение данной патологии требует комбинации медикаментозных и немедикаментозных методов.
Как правило, применяется поэтапный подход к терапии больных ОА [16, 17]. На первом этапе осуществляется снижение массы тела с использованием нефармакологических методов лечения: лечебной физкультуры в комбинации с физиотерапевтическими методиками. При отсутствии эффекта назначаются нестероидные противовоспалительные средства (НПВС).
Для пациентов с ОА, у которых НПВС не купируют болевой синдром, альтернативой может служить вискосапплементарная терапия гиалуроновой кислотой [7]. Вискосапплементарная терапия (от англ. viscosupplementation) – лечение, направленное на улучшение вязко-упругих свойств синовиальной жидкости. По сути, единственной группой препаратов, обеспечивающих такое влияние на синовиальную жидкость, являются препараты гиалуронана. Поэтому термин «вискосапплементарная терапия» рассматривается как синоним лечения препаратами гиалуронана [5].
Впервые термин «гиалуроновая кислота» предложили Карл Майер и Джон Палмер в 1934 г. для описания гликозаминогликана, выделенного ими из стекловидного тела глаза [23]. В синовиальной жидкости неповрежденного сустава гиалуроновая кислота содержится в концентрации 2,5–3,5 мг/мл и имеет среднюю молекулярную массу 4000–7000 kDa. В условиях повреждения суставного хряща и других структур сустава, в той или иной степени всегда имеющихся при остеоартрозе, в синовиальной жидкости отмечается снижение концентрации и молекулярной массы гиалуронана, что сопровождается изменениями функциональных свойств синовиальной жидкости, приводящими к усилению повреждения хрящевой ткани, стимуляции активности воспалительных клеток, увеличению синовиальных по-вреждений [9, 10, 12].
Экзогенный гиалуронан может стимулировать образование собственного полноценного гиалуронана [28]. Наряду с этим при введении препаратов гиалуроновой кислоты отмечается подавление секреции медиаторов воспаления, снижение чувствительности нервных окончаний, воспринимающих боль. Реализация данных механизмов гиалуронана обеспечивает его клинические эффекты: уменьшение выраженности болевого синдрома, улучшение функций КС и, как следствие, улучшение качества жизни пациента [19, 21, 27].
Впервые применение гиалуронана было предложено в 1942 г. E.A. Balazs [11]. Но только в 70-х годах XX века появились препараты, пригодные для использования у человека. Коммерческие продукты для внутрисуставного введения, получившие одобрение для клинического применения, были выведены на фармрынок в конце 80-х годов в Японии, Италии, затем в Канаде [11]. В 1998 г. применение гиалуронана для внутрисуставного введения при ОА было одобрено FDA в США [11].
В настоящее время препараты гиалуроновой кислоты широко используются во всем мире. В Великобритании около 15% пациентов с ОА коленного сустава получают внутрисуставные инъекции таких препаратов [20]. Стоимость подобного лечения очень высока, затраты на одно введение составляют от 110 до 230 долларов США [20]. В Австрии социальной страховой системой ежегодно на компенсацию расходов на лечение препаратами гиалуронана тратится более 10 млн евро [8]. В США данные затраты также покрываются страховыми системами и стоимость разового курса лечения у одного пациента может превышать 1000 долларов США [24].
Из множества препаратов гиалуронана можно выделить две группы средств, отличающихся по своим физико-химическим и биологическим свойствам [25]. Первая группа – это препараты гиалуроновой кислоты (натрия гиалуронат). Они содержат длинные несульфатированные прямые полимерные цепи из повторяющихся дисахаридов N-ацетилглюкозамина и глюкуроновой кислоты различной длины, в физиологических растворителях образуют петли случайной формы, имеют различную молекулярную массу, не превышающую 4000–5000 кДа. Вторая группа – это гиланы. Они содержат перекрестно-сшитые молекулы гиалуронана, у которых карбоксильные и N-ацетиловые группы свободны, могут быть плохо растворимы в воде и представлены в виде геля, имеют высокий молекулярный вес (6000 кДа для гилана G-F 21).
Обоснованность применения препаратов гиалуроновой кислоты для лечения ОА КС подтверждается систематическими обзорами и метаанализами, обобщающими результаты рандомизированных клинических исследований (РКИ). К началу 2007 г. было опубликовано 5 метаанализов [5, 8, 14, 22, 24, 29]. Наиболее полным рассмотрением всех доказательств эффективности вискосапплементарной терапии ОА КС является Кокрановский обзор, который был опубликован в 2005 г. и обновлен в апреле 2006 г. [5, 14]. Он содержит обзор и анализ РКИ, проведенных до января 2006 г., в которых изучалось применение одного или более препаратов гиалуронана у пациентов с ОА коленного сустава. Результаты анализа в Кокрановском систематическом обзоре подтверждают эффективность внутрисуставного введения гиалуронана как терапевтического класса для лечения остеоартроза КС. Гиалуронан уменьшает болевой синдром и улучшает функцию сустава, клинический эффект сохраняется до 13 недель после завершения курса введения, а в ряде случаев – и до 6 месяцев. Следует подчеркнуть, что эффективность разных препаратов данной группы неодинакова по ряду параметров в различные сроки после лечения, что не позволяет экстраполировать данные, полученные при изучении одного из них, на другие.
Таким образом, появление на фармацевтическом рынке новых препаратов гиалуроновой кислоты требует предварительной клинической оценки их эффективности и безопасности.
В Республике Беларусь представлено несколько производителей препаратов гиалуроновой кислоты, при регистрации каждого из которых были проведены клинические испытания. При этом в первую очередь оценивались эффективность и безопасность выводимых на рынок продуктов.
В 2009 г. в Республике Беларусь появился новый производитель препаратов данной группы: Ханкук Корус Фарм Ко. Лтд., Республика Корея. Изделие медицинского назначения было выведено под торговым названием – Хай-ФЛЕКС раствор для внутрисуставного введения (натрия гиалуронат 1%) стерильный, в одноразовых шприцах (20 мг/2 мл), регистрационное удостоверение МЗ РБ: ИМ-7.95773 от 15.09.2009 г., срок действия – до 15.09.2014 г. В ходе регистрации препарата Министерством здравоохранения Республики Беларусь было организовало проведение клинических испытаний на базе двух крупнейших учреждений здравоохранения: 9-я городская клиническая больница г. Минска (отделение ревматологии) и РНПЦ травматологии и ортопедии. В процессе исследований специалисты оценили высокую клиническую эффективность и безопасность Хай-ФЛЕКСа. Недостатков и замечаний по применению препарата обнаружено не было.
В связи с тем, что препараты гиалуроновой кислоты появились на белорусском фармацевтическом рынке сравнительно недавно и на сегодняшний день в стране практически отсутствуют клинические исследования такого аспекта данной группы продуктов, как длительность сохранения клинического эффекта у пациентов с остеоартрозом, специалистами РНПЦ травматологии и ортопедии было принято решение изучить продолжительность сохранения клинического эффекта у пациентов с посттравматическим ОА КС I–III стадии по Келлгрену, достигаемого после введения раствора для внутрисуставного введения Хай-ФЛЕКС.
Материалы и методы
Обследовано 60 пациентов в возрасте от 17 до 56 лет (45 мужчин, 15 женщин) с посттравматическим ОА коленного сустава I–III стадий по Келлгрену из числа обратившихся в приемное отделение Республиканского научно-практического центра травматологии и ортопедии в 2010–2011 гг. За 6–48 месяцев до начала лечения препаратом Хай-ФЛЕКС всем пациентам была выполнена диагностическая или оперативная артроскопия по поводу повреждения внутрисуставных структур.
Критерии включения пациентов в исследование:
1. Посттравматический ОА I-III стадий по Келлгрену;
2. Уровень боли при ходьбе по визуально-аналоговой шкале (ВАШ) более 40 мм.
Критерии исключения:
1. Другие (кроме посттравматического) виды ОА (системные заболевания соединительной ткани, болезни накопления, эндокринные заболевания);
2. Некорригированные ортопедические нарушения: варусная, вальгусная, ротационная деформация КС, некомпенсированная нестабильность КС, наличие поврежденных внутрисуставных структур, вызывающих динамические биомеханические нарушения;
3. Внутрисуставное введение хондропротекторов в течение 6 месяцев до включения в исследование и на период исследования;
4. Внутрисуставное введение глюкокортикостероидов в течение 2 месяцев до включения в исследование и на период исследования;
5. Наличие противопоказаний для проведения пункции суставов;
6. Индивидуальная непереносимость препарата;
7. Указание на психическое заболевание в анамнезе и в настоящее время;
8. Отсутствие согласия пациента на участие в исследовании.
Всем пациентам, включенным в исследование, Хай-ФЛЕКС вводился внутрь пораженного сустава 1 раз в неделю трехкратно (1-е, 8-е и 15-е сутки) в дозе 20 мг. По показаниям пациенты получали НПВС, физиотерапию.
Клиническая оценка эффективности препарата осуществлялась до начала лечения, после курса лечения, через 3 и 6 месяцев после курса лечения по следующим критериям:
1. Объективная оценка состояния пациента – осмотр специалиста;
2. Профиль шкалы исхода травмы и ОА КС (Knee Injury and Osteoarthritis Outcome Score – KOOS);
3. Динамика индекса WOMAC (Wes-tern Ontario and McMaster Universities);
4. Динамика индекса Лекена;
5. Уровень боли по ВАШ.
С помощью опросника KOOS оценивались: Б – боль, ФПЖ – функции повседневной жизни, СО – спорт и отдых, КЖ – качество жизни, связанное с коленным суставом по 100-балльной шкале (100 баллов в этом тесте свидетельствовали об отсутствии симптомов, 0 баллов – о том, что симптомы резко выражены).
Индекс WOMAC определяли по трем разделам: выраженность боли в коленном суставе (5 вопросов), ограничение подвижности в суставе (2 вопроса), затруднения в выполнении повседневной деятельности (17 вопросов), которые пациент оценивал в баллах от 0 до 100 (0 баллов – без затруднений, 100 баллов – невозможно) [12]. При анализе учитывали суммарный индекс WOMAC (сумма баллов по трем разделам).
Индекс Лекена (индекс тяжести гонартроза) определялся по пяти показателям, оцениваемым пациентом в баллах от 0 до 6:
– степень выраженности боли в течение ночи (отсутствие боли – 0 баллов, боль при движении в суставе – 1 балл, боль в покое – 2 балла),
– степень выраженности боли при ходьбе (отсутствие боли – 0 баллов, боль при прохождении определенного расстояния – 1 балл, боль в начале движения – 2 балла),
– степень выраженности боли в положении сидя более двух часов (отсутствие боли – 0 баллов, наличие боли – 1 балл);
– продолжительность утренней скованности (отсутствие – 0 баллов, меньше 15 минут – 1 балл, больше 15 минут – 2 балла);
– усиление боли в положении стоя в течение 30 минут (отсутствие боли – 0 баллов, наличие боли – 1 балл);
– ограничение дистанции ходьбы (нет ограничений – 0 баллов; больше 1000 м, но c трудом – 1 балл; 1000 м – 2 балла; 500–900 м – 3 балла; 300–500 м – 4 балла; 100–300 м – 5 баллов; менее 100 м – 6 баллов).
С помощью ВАШ оценивалась выраженность боли в КС в покое и при ходьбе, определяемая пациентом от 0 до 100 баллов (0 баллов – отсутствие боли, 100 баллов – невыносимая боль).
Кроме клинических методов обследования пациентов использовался ультразвуковой метод визуализации внутрисуставных структур. Ультразвуковое исследование (УЗИ) выполнялось на приборе VolusonI компании GE (2007 г.) линейным датчиком с частотой 7–12 МГц.
Оценивалась следующие показатели:
– толщина синовиальной оболочки,
– степень васкуляризации синовиальной оболочки,
– наличие выпота в полости сустава,
– толщина гиалинового хряща на мыщелках бедренной кости (в стандартных областях),
– степень деформации хряща,
– контуры суставных поверхностей бедренной и большеберцовой костей.
Ультразвуковыми критериями эффективности проводимой терапии считались: утолщение гиалинового хряща, восстановление однородности его эхоструктуры, отсутствие синовиального выпота в полости сустава, восстановление нормальной толщины синовиальной оболочки.
Результаты и обсуждение
Проведен анализ результатов лечения. Ни у одного из пациентов не было зарегистрировано осложнений внутрисуставного введения препарата (таких как инфекция, повреждения иглой, дискомфорт (боль) в месте введения, развитие синовита, проявления побочных реакций) как непосредственно после введения препарата, так и на протяжении 6 месяцев наблюдения.
Динамика основных показателей, характеризующих клиническую эффективность внутрисуставного введения препарата Хай-ФЛЕКС при ОА КС, представлена в таблице и на рис. 1–3.
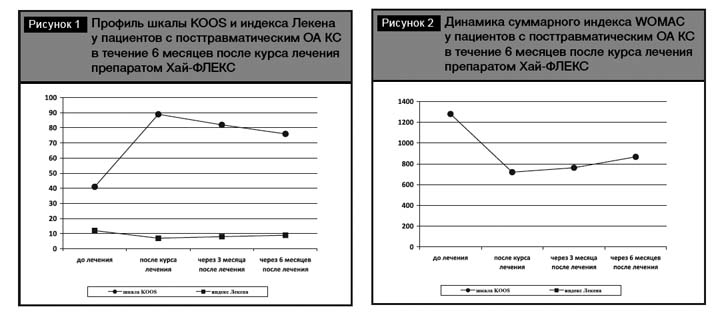
После проведения курса лечения препаратом Хай-ФЛЕКС (через 4 недели после первого введения препарата) выявлена положительная динамика показателей, оцениваемых по KOOS у всех пролеченных пациентов. Так, если до лечения сумма баллов составляла от 18 до 57 (в среднем 41,2±4,7), то через 4 недели после первого введения препарата она повысилась до 73–100 баллов (в среднем 89,3±3,6), в первую очередь, за счет показателя боли и показателя активности повседневной жизни (таблица, рис. 1).
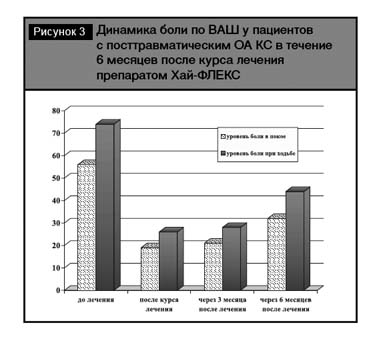
Положительная динамика отмечена также по индексу WOMAC (суммарный индекс по 3 разделам 1280,4±12,4 до лечения, 719,5±10,3 – после курса лечения (таблица, рис. 2)) и индексу Лекена (12,6±0,9 до лечения, 7,6±0,3 – после курса лечения соответственно (таблица, рис. 1)).
Динамика основных показателей, характеризующих функцию коленного сустава
в течение 6 месяцев после курса лечения препаратом Хай-ФЛЕКС
|
Показатель
|
До лечения
|
После курса лечения
|
Через 3 месяца
|
Через 6 месяцев
|
|
Шкала KOOS
|
41,2±4,7
|
89,3±3,6
|
82,4±4,3
|
76,4±3,9
|
|
Суммарный индекс WOMAC
|
1280,4±12,4
|
719,5±10,3
|
763,4±11,2
|
867,4±12,4
|
|
Индекс Лекена
|
12,6±0,9
|
7,6±0,3
|
8,2±0,6
|
9,8±0,7
|
|
Уровень боли в покое по ВАШ
|
56±2,3
|
19±1,6
|
21±1,5
|
32±1,8
|
|
Уровень боли при ходьбе по ВАШ
|
74±1,3
|
23±1,9
|
28±2,3
|
44±1,9
|
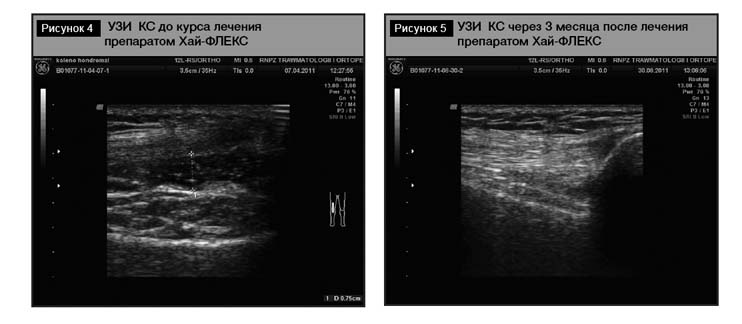
Наряду с вышеуказанными показателями значительно снизилась выраженность болевого синдрома по ВАШ как в покое (уменьшение суммы баллов с 56±2,3 до начала лечения до 19±1,6 после курса лечения), так и при ходьбе (с 74±1,3 до начала лечения до 23±1,9 после курса лечения (таблица, рис. 3).
Через 3 месяца после курса лечения не выявлено отрицательной динамики ни по одному из анализируемых показателей (таблица), то есть клинический эффект от внутрисуставного введения препарата Хай-ФЛЕКС сохранялся на протяжении 3 месяцев наблюдения.
Через 6 месяцев наблюдения хотя и выявлено незначительное ухудшение анализируемых показателей в сравнении с результатом, достигнутым непосредственно после курса лечения (таблица), в то же время в среднем по группе эти показатели были лучше, чем до лечения, что свидетельствует о сохранении терапевтического эффекта препарата Хай-ФЛЕКС на протяжении 6 месяцев после курса лечения.
Значение сопутствующего воспаления синовиальной оболочки как ведущего механизма развития боли при остеоартрозе в настоящем исследовании подтверждается данными УЗИ. При проведении УЗИ КС после курса лечения у 35 (43,8%) пациентов отмечено уменьшение признаков воспалительного процесса: уменьшение количества (вплоть до полного исчезновения) синовиального выпота в полости сустава, уменьшение толщины синовиальной оболочки, повышение однородности структуры хряща. При цветном энергетическом картировании васкуляризация не определяется.
На рис. 4 представлены данные УЗИ пациента с посттравматическим остеоартрозом правого коленного сустава до курса лечения препаратом Хай-ФЛЕКС. Определяется верхний заворот КС с наличием дополнительной жидкости, а также признаки хондромаляции (наличие в синовиальной жидкости гипер-эхогенных ярких точечных включений, свободно перемещающихся при компрессии датчиком).
При повторном исследовании (через 3 месяца после курса лечения) жидкость в полости сустава не лоцируется (рис. 5).
Таким образом, раствор для внутрисуставного введения Хай-ФЛЕКС (натрия гиалуронат 1%) стерильный, в одноразовых шприцах (20 мг / 2 мл), производства компании Ханкук Корус Фарм Ко. Лтд., Республика Корея, является эффективным и безопасным средством вискос-апплементарной терапии посттравматических артрозов коленных суставов. Применение данного препарата приводит к статистически значимому увеличению физической составляющей качества жизни пациентов (снижению, а в некоторых случаях к полному купированию боли в пораженном суставе, восстановлению его функций, объема движений), замедлению прогрессирования данного заболевания. Включение в комплексную терапию посттравматических ОА КС препарата Хай-ФЛЕКС позволит в будущем снизить вероятность выхода пациентов на инвалидность.
Л И Т Е Р А Т У Р А
1. Бадокин В.В. // Cons. med. – 2009. – № 11(9). – С. 91–95.
2. Баитов В.С. Современные возможности диагностики и консервативного лечения остеоартроза коленного и тазобедренного суставов: дис. ... канд. мед. наук. – Новосибирск, 2007. – 192 с.
3. Денисов-Никольский Ю.И., Миронов С.П., Омельяненко Н.П., Матвейчук И.В. Актуальные проблемы теоретической и клинической остеоартрологии. – М.. 2005. – С. 302–324.
4. Лучихина Л.В. Артроз. Ранняя диагностика и патогенетическая терапия. – М., 2001.
5. Сущук Е.А. Оценка эффективности препаратов гиалуроновой кислоты в лечении остеоартрита с позиций доказательной медицины Digestforours. 2009. – Прилож. 1. http://rheumatoligy.org.ua/blog/
6. Цветкова Е.С. Насонова В.А., Бунчук Н.В. Остео-артроз. Ревматические болезни: руководство для врачей. – М.: Медицина, 1997. – С. 385–396.
7. American College of Rheumatology Subcommittee on Osteoarthritis Guidelines // Arthrit. Rheum. – 2000. – Vol. 43. – P. 1905 –1515.
8. Arrich J., Piribauer F., Mad P. et al. // CMAJ. – 2005. – Vol. 172, N 8. – P.1039–1043.
9. Balazs E.A., Denlinger J.L. // J. Rheumatol. – 1993. – Vol. 20 (suppl. 39). – P.3–9.
10. Balazs E.А. Disorders of the Knee / ed. A.J.Helfet. – Philadelphia, 1982. – P.61–74.
11. Balazs E.A. // Surg. Technol. Int. – 2004 – Vol.12. – P.278–289.
12. Belcher C., Yaqub R., Fawthrop F. et al. // Ann. Rheum. Dis. – 1997 – Vol.56, N 5. – P.299 –307.
13. Bellamy N., Buchanan W.W., Goldsmith C.H. et al. // J. Rheumatol. – 1988. – Vol.15 – P.1833 –1840.
14. Bellamy N., Campbell J., Robinson V. et al. // Cochrane Database Syst. Rev. – 2006. – N 2. – P.CD005321.
15. Cefalu C.A., Waddell D.S. // Geriatrics. – 1999. – Vol. 54, N 10. – P.51–57.
16. Creamer P. // Curr. Opin. Rheumatol. – 2000. – Vol.12, N 5 – P.450–455.
17. Doherty M., Dougados M. // Best. Pract. Res. Clin. Rheumatol. – 2001. – Vol.15, N4. – P.517–525.
18. Felson D.T. // Epidemiol. Rev. – 1988 – Vol.10. – P.1–28.
19. Homandberg G.A., Hui F., Wen С. et al. // Osteoarthrit. Cartilage. – 1997. – Vol.5 – P.309 –319.
20. Jordan K.M., Sawyer S., Coakley P. et al. // Rheumatology (Oxford). – 2004. – Vol.43 – P.381 –384.
21. Kirchner M., Marshall D. // Osteoarthrit. Cartilage. – 2006. – Vol.14. – P.154 –162.
22. Lo G.H., LaValley M., McAlindon T., Felson D.T. // JAMA. – 2003. – Vol.290, N 23. – P.3115–3121.
23. Meyer K., Palmer J.W. // J. Biol. Chem. – 1934. – Vol.107. – P.629 –634.
24. Modawal A., Ferrer M., Choi H.K., Castle J.A. // J. Fam. Pract. – 2005. – Vol.54, N9. – P.758 –767.
25. Moreland L.W. // Arthritis. Res. Ther. – 2003 – Vol.5, N2. – P.54 –67.
26. OARSI recommendations for the management of hip and knee osteoarthritis. Part III. changes in evidence following systematic cumulative update of research publ. Jan. 2009 / W.Zhang, G.Nuki, R.W.Moskowitz, S.Abramson еt al. // Osteoarthrit. Cartilage. – 2010. –Vol.18, Issue 4. – P.476–499.
27. Raynauld J.P., Torrance G.W., Band P.A. // Osteoarthrit. Cartilage. – 2002 – Vol.10. – P.506 –517.
28. Smith M.M., Ghosh P. // Rheumatol. Int. – 1987. – Vol.7 – P.113–122.
29. Wang C.T., Lin J., Chang C.J. et al. // J. Bone Joint. Surg. Am. – 2004. – Vol.86, A (3). – P.538–545.
Медицинские новости. – 2011. – №11. – С. 46-50.
Внимание! Статья адресована врачам-специалистам. Перепечатка данной статьи или её фрагментов в Интернете без гиперссылки на первоисточник рассматривается как нарушение авторских прав.