Хроническая цереброваскулярная недостаточность (ХЦВН) – одна из наиболее частых патологий, встречающихся в ежедневной практике врача невролога. ХЦВН представляет собой синдром прогрессирующего многоочагового или диффузного поражения голов-ного мозга, проявляющийся клинически неврологическими, нейропсихологическими и/или психическими нарушениями, обусловленный хронической сосудистой мозговой недостаточностью и/или повторными эпизодами острых нарушений мозгового кровообращения. В нашей стране наиболее часто для обозначения данной нозологии используется термин дисциркуляторная энцефалопатия (ДЭ), который, возможно, более точно отражает сущность заболевания – структурное поражение головного мозга вследствие нарушения церебрального кровообращения.
Диагноз хроническая цереброваскулярная недостаточность устанавливается на основании следующих критериев:
1) наличие неврологических и нейропсихологических признаков поражения головного мозга;
2) наличие анамнестических, клинических, инструментальных признаков церебральной дисциркуляции;
3) причинно-следственная связь между вышеизложенными признаками, а также наличие клинических и параклинических признаков прогрессирования сосудистой мозговой недостаточности;
4) исключение других причин, способных объяснить имеющуюся клиническую картину.
Не останавливаясь детально на этио-логии ХЦВН (церебральный атеросклероз, гипертоническая болезнь, сахарный диабет, васкулиты, коагулопатии и др.), отметим, что центральным звеном патогенеза данной патологии является нарушение функционирования нейронов головного мозга вследствие персистирующей гипоксии. В связи с чем для лечения больных с ХЦВН оправдано применение препаратов, направленных на метаболическую защиту мозга – нейропротекторов.
Цель настоящего исследования – изучение терапевтической эффективности и переносимости препарата «Тиоцетам» («Артериум», Украина).
Тиоцетам относится к группе цереброактивных средств. Проявляет ноотропные, противоишемические, антиоксидантные и мембраностабилизирующие свойства. Тиоцетам ускоряет утилизацию глюкозы в реакциях аэробного и анаэробного окисления, нормализует биоэнергетические процессы, стабилизирует метаболизм в тканях мозга и повышает стойкость мозга к гипоксии. Его эффект обусловлен взаимопотенциирующим эффектом входящих в его состав пирацетама и тиотриазолина. Данный препарат имеет две формы выпуска: в виде раствора для инъекций, 1 мл которого содержит 0,1 г пирацетама и 0,025 г тиотриазолина, и в форме таблеток, содержащих по 0,2 пирацетама и 0,05 тиотриазолина. Наличие двух форм препарата позволяет использовать его как на стационарном, так и на амбулаторном этапе лечения.
В исследовании участвовало 130 пациентов (67 женщин и 63 мужчин), имеющих клинические и параклинические проявления ХЦВН. Возраст больных варьировал от 53 до 72 лет (в среднем 63,2 ± 3,9 года).
Критерии включения в исследование: наличие ХЦВН в соответствии с вышеописанными критериями; наличие информированного письменного согласия на участие в исследовании; возраст до 75 лет.
Критерии исключения: наличие установленных психических заболеваний; сопутствующая соматическая патология в стадии декомпенсации; наличие установленного онкологического заболевания.
Включенные в исследование пациенты были разделены на две группы. В первую группу вошел 71 человек с дисциркуляторной энцефалопатией I степени. Пациенты этой группы методом простой рандомизации были разделены на основную (56 пациентов) и контрольную (15 больных) подгруппы. Вторая группа, состоящая из 59 пациентов с диагнозом ДЭ II степени, аналогичным образом была разделена на основную и контрольную подгруппы, состоящие из 44 и 15 человек соответственно. Больные основной подгруппы получали тиоцетам согласно протоколу. Пациентам, вошедшим в контрольную подгруппу, проводилось лечение пирацетамом в соответствующих дозировках.
Всем пациентам в динамике проводилось неврологическое обследование, контролировалось артериальное давление и частота сердечных сокращений, общеклинические анализы, биохимические и коагулометрические показатели крови. Протокол обследования также включал электрокардиографию, электроэнцефалографию, дуплексное сканирование брахиоцефальных артерий, рентгеновскую компьютерную и/или магниторезонансную томографию головного мозга, исследование когнитивных вызванных потенциалов (Р-300), нейропсихологическое обследование. Больные осматривались терапевтом, нейроофтальмологом и отоневрологом, при необходимости – другими узкими специалистами.
Каждый пациент проходил обследование до начала лечения и дважды в течение курса лечения. Первой контрольной точкой был выбран 14-й день терапии (К 1). И второй раз пациенты подвергались комплексному обследованию на 60-й день лечения (К 2).
Курс лечения тиоцетамом состоял из двух этапов. Начало терапии тиоцетамом проводилось в виде в/мышечного введения по 5 мл в течение 14 дней. Затем терапия тиоцетамом была продолжена в виде приема внутрь по 2 таблетки 3 раза в день в течение 45 дней.
При проведении исследования пациенты продолжали получать соматическую терапию, преимущественно гипотензивные, антиагрегантные, сердечнососудистые препараты в индивидуально подобранных дозировках. Из базового лечения исключались как ноотропные, так и психотропные средства.
Эффективность лечения оценивалась по данным клинического статуса (данные неврологического осмотра), субъективной оценки пациентом своего самочувствия, нейропсихологических и нейрофизиологических методов исследования, а также с помощью оценки двигательных нарушений.
Клинический эффект оценивался неврологом по 5-балльной шкале: 0 – ухудшение, 1 – отсутствие улучшений, 2 – минимальное улучшение, 3 – умеренное улучшение, 4 – значительное улучшение, 5 – регресс большинства симптомов.
Субъективная оценка эффективности лечения проводилась с помощью шкалы общего клинического впечатления (–3 – значительное ухудшение, –2 – умеренное ухудшение, –1 – минимальное ухудшение, 0 – отсутствие изменений, 1 – минимальное улучшение, 2 – умеренное улучшение, 3 – значительное улучшение).
В процессе нейропсихологического исследования использовались:
1) шкала краткого исследования психического статуса (Mini Mental State Examination – MMSE);
2) тест Шульте для изучения параметров произвольного внимания и его функций;
3) тест на запоминание 10 слов, который помимо функции механического запоминания отражает утомляемость и активность внимания.
Нейрофизиологическое исследование включало оценку когнитивных вызванных потенциалов (Р-300) и ЭЭГ.
Для выявления двигательных нарушений использовалась шкала равновесия и двигательной активности Тинетти и кинетический тест (время трех переборов). При выполнении данного теста пациент большим пальцем руки по очереди дотрагивается до 2, 3, 4, 5-го пальца той же руки, а затем перебирает пальцы в обратном порядке, начиная с 5-го. Фиксируется время выполнения трех полных переборов.
Переносимость лечения оценивали при помощи структурированной шкалы побочных эффектов (UKU). Для оценки безопасности терапии в начале и в конце исследования проводили общеклинические и биохимические анализы крови и мочи.
Оценка динамики неврологических симптомов неврологами. Положительный эффект выявлен у 52 (93%) пациентов с ДЭ I степени и у 40 (91%) пациентов с ДЭ II степени. Заметный регресс неврологических симптомов (3–4 балла) отмечен у 34 (61%) и 23 (52%) пациентов в каждой из групп соответственно. Умеренный эффект (2 балла) наблюдался у 18 (32%) больных ДЭ I степени и у 17 (39%) пациентов с ДЭ II степени. Существенная динамика отсутствовала у 8 пациентов (по 4 пациента в каждой из групп). Среди неврологических нарушений, уменьшавшихся на фоне лечения, в первую очередь отмечался регресс выраженности статической и динамической атаксии, глазодвигательных нарушений, расстройств чувствительности.
Положительная динамика в двигательной сфере была подтверждена результатами оценки по шкале равновесия и двигательной активности Тинетти (табл. 1) и динамикой времени выполнения кинетического теста (табл. 2).
Таблица 1. Динамика нарушений ходьбы и постуральной устойчивости, баллы
|
Диагноз
|
Подгруппа
|
До лечения
|
К 1
|
К 2
|
|
ДЭ I ст.
|
Основная
|
31,2 ± 2,9
|
33,8 ± 2,7*
|
34,2 ± 2,9*
|
|
Контрольная
|
31,4 ± 2,5
|
32,7 ± 2,2
|
33,3 ± 2,3*
|
|
ДЭ II ст.
|
Основная
|
30,6 ± 2,6
|
32,9 ± 2,8*
|
33,1 ± 2,6*
|
|
Контрольная
|
30,3 ± 2,7
|
31,6 ± 2,5
|
32,1 ± 2,2*
|
П р и м е ч а н и е : *различия с исходным уровнем статистически значимы (р<0,05).
Таблица 2. Динамика выполнения кинетического теста, секунды
|
Диагноз
|
Подгруппа
|
До лечения
|
К 1
|
К 2
|
|
ДЭ I ст.
|
Основная
|
11,6 ± 1,7
|
8,7 ± 1,2*
|
8,8 ± 1,5*
|
|
Контрольная
|
11,9 ± 1,6
|
10,7 ± 1,4
|
9,7 ± 1,3*
|
|
ДЭ II ст.
|
Основная
|
13,2 ± 2,3
|
11,5 ± 2,1
|
10,4 ± 2,3*
|
|
Контрольная
|
13,4 ± 1,8
|
12,2 ± 1,6
|
11,2 ± 2,2*
|
П р и м е ч а н и е : *различия с исходным уровнем статистически значимы (р<0,05).
В группе пациентов, использующих в комплексной терапии препарат «Тиоцетам», отмечается достоверное улучшение показателей двигательной активности. Улучшение наблюдалось и у пациентов, получавших пирацетам, но процент улучшения в группах, принимающих тиоцетам, был выше, чем в контрольной группе. Таким образом, степень выраженности двигательных нарушений в основных группах уменьшилась в большей степени по сравнению с контрольной.
Подавляющее большинство пациентов как основных, так и контрольной групп отмечали улучшение самочувствия. При этом пациенты, использующие в комплексной терапии препарат «Тиоцетам», отметили более значительное улучшение самочувствия по сравнению с контрольной группой. Данная тенденция наблюдалась уже на 14-й день терапии и сохранялась при обследовании по окончании курса лечения.
Результаты субъективной оценки пациентами результатов лечения на 14-й и 60-й дни приведены на рис. 1 и 2.
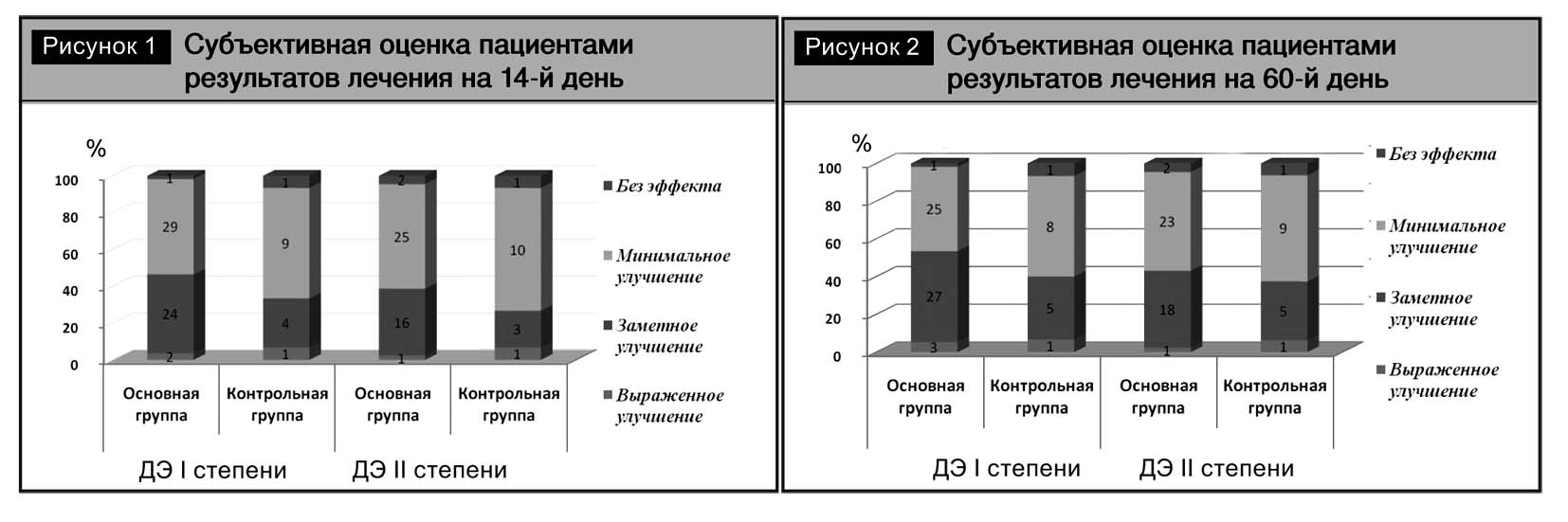
Результаты динамического исследования нейропсихологических тестов в изучаемых группах больных представлены в табл. 3–5.
Таблица 3. Динамика показателей шкалы краткого исследования психического статуса (MMSE), баллы
|
Диагноз
|
Подгруппа
|
До лечения
|
К 1
|
К 2
|
|
ДЭ I ст.
|
Основная
|
23,6 ± 1,27
|
26,5 ± 0,87*
|
26,6±1,07*
|
|
Контрольная
|
23,9 ± 1,19
|
25,6 ± 1,19
|
25,9±1,14*
|
|
ДЭ II ст.
|
Основная
|
22,3 ± 1,13
|
25,1 ± 1,03
|
25,8±0,98*
|
|
Контрольная
|
22,1 ± 1,12
|
24,2 ± 1,21
|
24,8±1,13*
|
П р и м е ч а н и е: в табл. № 3–5 – *различия с исходным уровнем статистически значимы (р<0,05).
Таблица 4. Динамика выполнения теста запоминания 10 слов, %
|
Диагноз
|
Подгруппы
|
До лечения
|
К 1
|
К 2
|
|
ДЭ I ст.
|
Основная подгруппа
|
63,2 ± 3,36
|
69,8 ± 2,72*
|
70,3 ± 3,24*
|
|
Контрольная подгруппа
|
62,9 ± 2,47
|
66,1 ± 2,16
|
66,4 ± 2,24*
|
|
ДЭ II ст.
|
Основная подгруппа
|
60,6 ± 2,42
|
65,4 ± 2,39
|
65,6 ± 3,16*
|
|
Контрольная подгруппа
|
60,7 ± 2,93
|
64,3 ± 2,32
|
64,8 ± 2,84
|
Таблица 5 Динамика времени выполнения таблиц Шульте, %
|
Диагноз
|
Подгруппа
|
До лечения
|
К 1
|
К 2
|
|
ДЭ I ст.
|
Основная
|
48,5 ± 2,62
|
39,6 ± 2,37*
|
38,8 ± 3,41*
|
|
Контрольная
|
48,3 ± 1,65
|
44,2 ± 1,91*
|
43,9 ± 1,87*
|
|
ДЭ II ст.
|
Основная
|
52,6 ± 1,24
|
47,9 ± 2,12*
|
44,3 ± 3,21*
|
|
Контрольная
|
51,9 ± 2,42
|
48,1 ± 1,87*
|
46,7 ± 2,13*
|
Как следует из представленных данных, на фоне курсового приема тиоцетама отмечаются статистически достоверные изменения когнитивных функций. Анализ динамики выполнения нейропсихологических тестов свидетельствует о значительном улучшении памяти и внимания у пациентов с ДЭ I и II степени на фоне нейропротекторной терапии. При этом у пациентов, получавших тиоцетам, выявлены более выраженное улучшение времени выполнения таблиц Шульте (на 20 и 15% в группах с ДЭ I и II степени соответственно) по сравнению с контрольными группами (улучшение на 10%). Аналогичные тенденции наблюдались и в динамике выполнения теста запоминания 10 слов. При исследовании показателей шкалы краткого исследования психического статуса (MMSE) позитивная динамика на фоне терапии тиоцетамом отмечалась в отношении концентрации внимания, памяти и речи. При подсчете суммы показателей данной шкалы выявлено статистически достоверное положительное влияние курсового лечения тиоцетама на психомнестический статус больных.
Динамику биоэлектрической активности головного мозга на фоне терапии тиоцетамом показало ЭЭГ исследование. Так, уже на 14-й день лечения тиоцетамом было отмечено уменьшение выраженности медленноволновой активности и признаков дезорганизации коркового ритма. Подобные изменения были обнаружены и на 60-й день терапии. Таким образом, контроль ЭЭГ продемонстрировал положительное влияние тиоцетама на биоэлектрическую активность головного мозга.
При исследовании когнитивных вызванных потенциалов Р-300 у пациентов с ДЭ I и II степени отмечались изменения их составляющих на фоне проводимого лечения во всех группах. Через 14 дней на фоне терапии тиоцетамом у 68% обследованных с ДЭ I степени наблюдалось улучшение амплитудных и временных параметров Р-300. В группе с ДЭ II степени у 45%. В контрольной группе улучшение когнитивных вызванных потенциалов Р-300 было отмечено только у 28% обследованных. После двухмесячного курса терапии тиоцетамом у пациентов с ДЭ I и II степени наблюдалось достоверное увеличение амплитуды компонента Р-300 по сравнению с его исходным фоном, также было зарегистрировано статистически значимое укорочение латентностей Р-300. Динамика данных показателей коррелировала с улучшением психомнестического статуса по данным нейропсихологического тестирования.
Все пациенты, включенные в исследование, завершили курс терапии в установленный срок. Ни один пациент не прекратил прием тиоцетама преж-девременно. За время исследования у пациентов, принимавших тиоцетам, не было выявлено побочных реакций или осложнений. По субъективным ощущениям пациентов в группах, получавших тиоцетам, отмечена хорошая его переносимость.
Актуальность проблемы хронической цереброваскулярной недостаточности не вызывает сомнений. Десятки миллионов лиц пожилого возраста имеют ХЦВН и требуют постоянного не только внимания, но и лечения. Тиоцетам – препарат с нейропротекторным, нейрометаболическим действием – зарекомендовал себя как эффективное средство терапии пациентов с ХЦВН.
Выводы:
1. Курсовое лечение тиоцетамом пациентов с дисциркуляторной энцефалопатией I–II стадий привело к достоверному улучшению когнитивных и интегративных функций и психоэмоционального состояния пациентов с хронической цереброваскулярной недостаточностью.
2. Важный аспект применения тиоцетама – хорошая переносимость. Побочные эффекты и аллергические реакции отсутствовали, что говорит о безопасности препарата.
3. Полученные данные позволяют рекомендовать тиоцетам для широкого использования в практической деятельности неврологов, терапевтов, психиатров и геронтологов.
Медицинские новости. – 2010. – №11. – С. 105-108.
Внимание! Статья адресована врачам-специалистам. Перепечатка данной статьи или её фрагментов в Интернете без гиперссылки на первоисточник рассматривается как нарушение авторских прав.