Актуальность проблемы остеопороза (ОП) на современном этапе обусловлена, как изменением демографической ситуации (увеличение продолжительности жизни населения и числа лиц старше 50 лет), так и внедрением новых лечебно-диагностических технологий (остеоденситометрия, биохимические маркеры костного метаболизма, микрокомпьютерная томография, внедрение новых лекарственных средств), позволяющих выявлять ранние патологические изменения скелетно-мышечной системы и своевременно рекомендовать лечебно-профилактические мероприятия, обеспечивающие эффективное снижение риска остеопоротических переломов [1–7].
Согласно заключению Комитета по контролю за качеством продуктов и лекарственных средств (FDA, 2007) в США средствами фармакотерапии ОП являются [8]:
• антирезорбенты (ингибирование костной резорбции):
- бисфосфонаты (алендронат, ризедронат, ибандронат)
- кальцитонин
- эстрогены (ЗГТ)
- ралоксифен
• анаболические препараты (стимуляция костеобразования):
- терапия паратиреоидным гормоном ПТГ (ПТГ 1-34, терипаратид)
Одной из официально рекомендуемых ведущими организациями, разрабатывающими стратегию профилактики и лечения ОП групп лекарственных средств, направленных на патогенетическую коррекцию ОП, является группа бисфосфонатов (БС) [1, 3, 6–11].
Алендронат по своей химической структуре относится к аминобисфосфонатам [3, 9]. Ранние исследования показали, что главный компонент алендроната — фрагмент P-C-P, определяющий его сродство к костной ткани. Фрагмент R1 определяет дополнительную аффинность: замена атома водорода гидроксильной группой в положении R1 увеличивает сродство к гидроксилапатиту примерно в 2 раза. Введение компонентов азота в положение R2 увеличивает антирезорбтивный потенциал аледроната в 3 раза по сравнению с БС, не содержащими азот. Показано, что присутствие молекулы азота в боковой цепи структуры аледроната увеличивает его возможности и специфичность, направленные на подавление костной резорбции [3, 9].
Среди всех представителей группы БС наиболее широкие официальные показания в профилактике и лечении ОП в настоящее время имеет алендронат. Рекомендации Национальной федерации ОП (NOF, 2007) США представлены в табл. 1 [8]:
Таблица 1. Показания для назначения алендроната согласно рекомендациям Национальной федерации ОП (NOF, 2007)
|
Цель
|
Доза
|
Целевые группы
|
|
Профилактика остеопороза
|
5 мг/сут или
35 мг/нед.
|
Постменопаузальные женщины
|
|
Лечение остеопороза
|
10 мг/сут или
70 мг/нед.
|
Постменопаузальные женщины *
Остеопороза у мужчин*
Глюкокортикоид-индуцированный остеопороз*
|
* В виде монотерапии или в комбинации с витамином Д – 800 МЕ/сут (20 мкг/сут)
Доказательная база по оценке эффективности алендроната в лечении постменопаузального ОП начала формироваться более 15 лет назад, однако наиболее значимые результаты получены в конце 90-х годов ХХ столетия [1, 3, 12, 16, 17].
С целью улучшения комплайенса лечения и снижения риска развития побочных эффектов со стороны ЖКТ была создана форма алендроната с дозировкой 70 мг. Сравнительное исследование эффективности и переносимости препарата в дозе 10 мг в сутки и 70 мг в неделю в лечении постменопаузального ОП подтвердила эффективность ретардной формы при меньшей частоте побочных эффектов [3, 9, 13–15].
Результаты мета-анализа исследований, изучавших эффективность применения алендроната в комплексной терапии (в сочетании с препаратами кальция) постменопаузального ОП представлены в табл. 2 [9, 12, 23–28].
Таблица 2. Мета-анализ исследований по изучению эффективности алендроната в лечении постменопаузального остеопороза
|
Авторы, год
|
Число наблюдений, зона контроля
|
Дозы, длительность
|
Результаты
|
|
U.A. Liberman и соавт., 1995
|
994 пациента в 37 центрах, МПК поясничного отдела позвоночника
|
5, 10 или 20 мг/день 20 мг/день, 5 мг/день на 3-м году исследования 3 года
|
Повышение МПК на 16%
|
|
D.M. Black и соавт., 1996
|
2027 пациентов в 11 центрах
|
5 мг/день, доза увеличивалась до 10 мг/день на 24 мес. 2,9 года
|
Снижение риска переломов на 11–13%
|
|
S.R. Cummings и соавт., 1998
|
4432 пациента в 11 центрах, МПК шейки бедра
|
5 мг/день, доза увеличивалась до 10 мг/день на 24 месяца 4,2 года
|
Повышение МПК шейки бедра на 17–19%
|
|
H.A. Pols и соавт., 1999
|
1908 пациентов в 153 центрах, МПК позвоночника
|
10 мг/день 1 год
|
Повышение МПК поясничного отдела позвоночника 11%
|
|
R.D. Chapurlat и соавт., 2004
|
6459 пациент, МПК позвоночника
|
5–10мг/день
|
Снижение риска переломов на 57%
|
|
G. Gvaraldi и соавт., 2004
|
41 пациент, МПК шейки бедра и позвоночника
|
70 мг 1 раз в неделю
|
Достоверное повышение МПК
|
|
C.J. Rosen и соавт., 2005
|
520 пациент, МПК шейки бедра и позвоночника
|
70 мг 1 раз в неделю 1 год
|
Повышение МПК на 3,4% за 12 месяцев в области трохантера и на 1,2% в области позвоночника
|
В клинической практике в Республике Беларусь широко используется алендронат «Остеотаб», производства фармацевтической компании «PharmacareInt. Co.», который выпускается в виде таблеток по 10 мг и 70 мг.
Цель исследования – оценка эффективности алендроната и комбинированного препарата кальция и витамина Д в комплексной терапии постменопаузального остеопороза.
Материалы и методы
Рандомизированное проспективное исследование проведено на базе ГУ «Республиканский центр медицинской реабилитации и бальнеолечения», УЗ «6-я городская клиническая больница г. Минска», УЗ «1-я городская клиническая больница г. Минска».
Обследовано 15 женщин с верифицированным диагнозом постменопаузальный остеопороз. В ходе работы проводилось анкетирование пациенток на наличие факторов риска остеопороза, в том числе вторичных форм заболевания; оценка суточного потребления кальция и витамина Д с использованием программного комплекса «I-Nutrition».
Состояние минеральной плотности кости (МПК) оценивалось на основании двойной рентгеновской абсорбциометрии (ДРА) осевого скелета на денситометре «PRODIGY LUNAR» фирмы General Electric Medical Systems (США) 2004 года выпуска. Рентгеновская нагрузка в одной проекции составляет 0,04 мЗв. Проводилось исследование BMD-bone mineral density (г/см2); Z-критерия (Z-score), T-критерия (T-score) в области поясничного отдела позвоночника (L1-L4) и проксимального отдела бедра (шейка бедра – neck, область Варда – upper neck, область большого вертела – trochanter, проксимальный отдел бедра (ПОБ) – total hip).
Для количественной оценки МПК у обследованных женщин использовался Т- критерий [1, 2, 6, 18–22].
В исследование не включались женщины с наличием сопутствующих заболеваний и состояний, ассоциированных со снижением МПК.
Статистический анализ данных проводился с помощью программы STATISTICA (версия 6,0) с предварительной проверкой соответствия рассматриваемых переменных нормальному распределению по критерию Шапиро–Уилка. Отклонения от нормального распределения считали существенными при значении р>0,05. Для анализа различий подгрупп, выделенных по качественным клинико-диагностическим признакам использовались непараметрические методы Вилкоксона. Различия считали статистически значимыми при p<0,05. Данные приведены в виде среднего значения (M) ± стандартное отклонение (SD), или медианы (Ме) и межквартильного размаха [LQ-UQ], в зависимости от нормальности распределения.
Результаты и обсуждение
Клиническая характеристика, обследованных пациенток, представлена в табл. 3.
Таблица 3. Клиническая характеристика пациенток, включенных в исследование
|
Параметр
|
m±(SD) или Ме [LQ-UQ] (n=15)
|
Критерий Шапиро-Уилка, р1
|
|
Возраст, лет
|
155,43 (±4,14)
|
0,314
|
|
Длительность менопаузы, лет
|
7,0 [3,00-7,50]
|
0,025
|
|
Рост, см
|
160,00 [150,00-163,00]
|
0,000
|
|
Вес, кг
|
64,2 (±10,01)
|
0,863
|
|
ИМТ, кг/м2
|
25,16 (±3,73)
|
0,368
|
|
МПК (LI-LIV), г/см2
|
0,819 [0,799-0,845]
|
0,021
|
|
Т-критерий (LI-LIV)
|
-3,0 [-3,2/-2,8]
|
0,013
|
|
МПК (ШБ), г/см2
|
0,94 (±0,14)
|
0,876
|
|
Т-критерий (ШБ)
|
-1,79 (±0,49)
|
0,842
|
|
МПК (ПОБ), г/см2
|
0,798 (±0,074)
|
0,339
|
|
Т-критерий (ПОБ)
|
-1,686 (±0,617)
|
0,287
|
Данные о среднесуточном потреблении кальция и витамина Д у обследованных пациенток на момент включении в исследование, согласно результатам анкетирования, представлены в табл. 4.
Таблица 4. Суточное потребление кальция и витамина Д с продуктами питания пациентами, включенными в исследование
|
Параметр
|
m±(SD) или Ме [LQ-UQ] (n=15)
|
Критерий Шапиро-Уилка, р1
|
|
Суточное потребление кальция, мг/сут
|
594,429 (±90,75)
|
0,608
|
|
Суточное потребление вит Д, мкг/сут
|
5,4 (±1,55)
|
0,478
|
Рекомендуемая норма суточного потребления кальция для женщин в постменопаузе – 1500 мг/сут, витамина Д – 800 МЕ (20 мкг/сут) [1, 3, 6, 8, 11, 14].
Таким образом, у женщин с постменопаузальным остеопорозом, включенных в исследование, выявлено наличие дефицита потребления кальция и витамина Д с продуктами питания.
Со всеми пациенткам проводилось индивидуальное обучение, включающее обсуждение особенностей питания, физической нагрузки, режима приема лекарственных средств в ходе лечения остеопороза. Были рекомендованы упражнения для укрепления мышц спины («кошечка»), ходьба в течение 60 минут в день. Пациентки получали комбинированный препарат кальция и витамина Д – «Кальцивид» фармацевтической компании «Pharmacare Int.Co.» (2 таблетки в сутки – в обед и ужин), что составило 1200 мг кальция карбоната и 400 МЕ витамина Д3 (холекациферола), а также алендронат (Остеотаб) в дозе 70 мг 1 раз в неделю на протяжении 12 месяцев.
С целью повышения приверженности к лечению пациенткам было рекомендовано вести дневник самоконтроля, отмечать регулярность выполнения физических упражнений, прием лекарственных средств, наличию нежелательных явлений.
Контроль данных МПК осевого скелета проведен через 12 месяцев терапии (табл.5).
Таблица 5. Показатели МПК осевого скелета исходно и через 12 месяцев терапии
|
Параметр
|
Исходно m±(SD) или Ме [LQ-UQ] (n=15)
|
Критерий Шапиро-Уилка, р1
|
Через 12 мес лечения m±(SD) или Ме [LQ-UQ] (n=15)
|
Критерий Шапиро-Уилка, р2
|
р3
|
|
МПК (LI-LIV), г/см2
|
0,819 [0,799-0,845]
|
0,021
|
0,856 (±0,059)
|
0,39
|
0,29
|
|
Т-критерий (LI-LIV)
|
-3,0 [-3,2/-2,8]
|
0,013
|
-2,744 (±0,482)
|
0,24
|
0,21
|
|
МПК (ШБ), г/см2
|
0,94 (±0,14)
|
0,876
|
0,79 (±0,076)
|
0,997
|
0,06
|
|
Т-критерий (ШБ)
|
-1,79 (±0,49)
|
0,842
|
-1,35 [-1,9/-0,6]
|
0,000
|
0,33
|
|
МПК (ПОБ), г/см2
|
0,798 (±0,074)
|
0,339
|
0,85 (±0,055)
|
0,212
|
0,028
|
|
Т-критерий (ПОБ)
|
-1,686 (±0,617)
|
0,287
|
-1,2 (±0,467)
|
0,146
|
0,028
|
Сравнительный анализ (тест Вилкоксона) показателей МПК в области позвоночника (L1-L4), шейки бедра и проксимального отдела бедра до и после проведения комплексной терапии остеопороза выявил достоверное (р=0,028) повышение Т-критерия (рис. 1) и МПК (р=0,028) (рис. 2) в области проксимального отдела бедра.
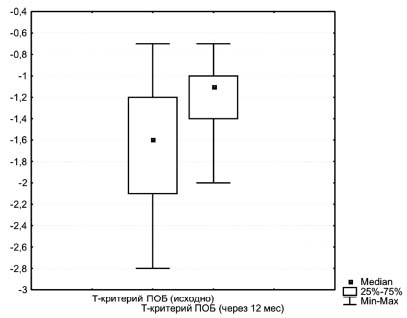
Рис. 1. Данные Т-критерия в области проксимального отдела бедра исходно и через 12 месяцев лечения
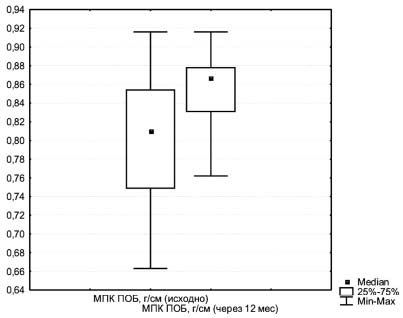
Рис. 2. Показатели МПК в области проксимального отдела бедра исходно и через 12 месяцев лечения
Основная причина причина, обусловливающая выбор области проксимального отдела бедра для исследования – его высокая подверженность переломам [1,2,3,6,14]. Кроме того, различные области проксимального отдела бедра не однородны по содержанию трабекулярного и кортикального компонента костной ткани. Так, МПК в области зоны Варда, расположенной в основании шейки бедра, ассоциирована с ранними изменениями костной плотности и тесно коррелирует с МПК тел поясничных позвонков, что может служить маркером риска их переломов [1–3, 6] (рис. 3).
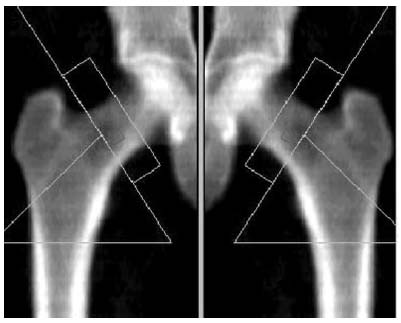
Рис. 3. Денситограмма проксимального отдела бедренной кости
Выделение зоны шейки бедра и проксимального отдела бедренной кости наиболее значимо в оценке состояния МПК кортикальной кости [1–3, 6].
Таким образом, результаты проведенного проспективного рандомизированного клинического исследования, подтвердили эффективность применения алендроната (Остеотаб) в сочетании с комбинированным препаратом карбонатом кальция и холекальциферола (Кальцивид) в комплексной терапии постменопаузального остеопороза с преимущественным увеличением показателей МПК в области проксимального отдела бедра.
ЛИТЕРАТУРА
1. Руководство по остеопорозу /Л.И. Алексеева [и др.]; под общ. ред. Л.И. Беневоленской. – М.: БИНОМ. Лаборатория знаний, 2003. – 524 с.
2. Kanis J.A. on behalf of the World Health Organization Scientific Group (2007). Assessment of osteoporosis at the primary health care level. Technical Report. World Health Organization Collaborating Center for Metabolic Bone Diseases, University of Sheffield, UK. – Printed by the University of Sheffield, 2007. – 287 p.
3. РиггзБ.Л. Остеопороз. Этиология, диагностика, лечение / Б.Л. Риггз, III Л.Дж. Мелтон. – Пер с англ. – М. – СПб.: ЗАО «Издательство БИНОМ», «Невский диалект», 2000. – 560 с.
4. National Osteoporosis Foundation. NOF’s Clinician’s Guide to Prevention and Treatment of Osteoporosis [электронный ресурс]. – Режим доступа: http://www.nof.org/professionals/ NOF_Clinicians_Guide.pdf. – Дата доступа: 23.08.2008.
5. Джонел О. Остеопороз: заболевание, которому все еще уделяется недостаточно внимания / О. Джонел. // Медикография. – 2004. – № 3, Том. 26. – С.1–3.
6. Клинические рекомендации. Остеопороз. Диагностика, профилактика и лечение /Л.И. Беневоленская [и др.]; под общ. ред. Л.И. Беневоленской, О.М. Лесняк. – М.: ГЭОТАР-Медиа, 2005. – 176 с.
7. European guidelines for the diagnosis and management of osteoporosis in postmenopausal women. On behalf of the European Society for Clinical and Economic Aspects of Osteoporosis and Osteoarthritis (ESCEO) / J.A. Kanis [et al.] // Osteoporos. Int. – 2008. – N19. – P. 339–428.
8. National Osteoporosis Foundation. NOF’s Clinician’s Guide to Prevention and Treatment of Osteoporosis [электронный ресурс]. – Режим доступа: http://www.nof.org/professionals/ NOF_Clinicians_Guide.pdf. – Дата доступа: 23.08.2008.
9. Поворознюк В.В. Бисфосфонаты: роль ибандроновой кислоты в лечении постменопаузаль-ного остеопороза / В.В. Поворознюк // Здоров’я України. – 2007. – № 5. – С. 57–58.
10. Fleish H. Bisphosphonates in Bone Disease. From the laboratory to the patients / H. Fleish. – Acadimic Press, 2000. – 212 p.
11. Руденко Э.В. Остеопороз. Диагностика, лечение и профилактика / Э.В. Руденко. – Минск: Бел. наука, 2001. – 153 с.
12. Cummings S.R. Effect of alendronate on risk of fracture in women with low bone density but without vertebral fractures / S.R. Cummings [et al.] // JAMA. – 1998. – N 280, Vol. 11. – P. 2077-2082.
13. Harrison’s Principles of Internal Medicine. Chapter: Osteoporosis / L. Kasper [et al.]. – McGraw-Hill, 2005. – 1452 p.
14. Холодова Е.А. Эндокринные остеопатии: особенности патогенеза, диагностики и лечения: практ. рук–во для врачей / Е.А. Холодова, А.П. Шепелькевич, З.В. Забаровская – Минск: Белпринт, 2006. – 88 с.
15. Шепелькевич А.П. Проблема остеопороза при заболеваниях эндокринной системы / А.П. Шепелькевич, З.В. Забаровская // Мед. новости. – 2008. – № 7. – С.55–60.
16. Johnell O. An estimate of the worldwide prevalence and disability associated with osteoporotic fractures / O. Johnell, J.A. Kanis // Osteoporos Int. – 2006. – Vol.17. – P.1726–1733.
17. Burge R. Incidence and economic burden of osteoporosis–related fractures in the United States 2005–2025 / R. Burge [et al.] // J. Bone Miner. Res. – 2007. – Vol. 22. – P. 465–475.
18. Roux C. The living bone / C. Roux [et al.]. – Wolter Kruwer Health France, 2007. – Р. 113.
19. Hemenway D. Body height and hip fracture: a cohort study of 90000 women / D. Hemenway, D. Feskanich, G.A. Colditz // Int. J. Epidemiol. – 1995. – N 24, Vol. 4. – P.783–786.
20. Garnero P. Markers of bone resorption predict hip fracture in elderly women: the EPIDOS Prospective Study / P. Garnero [et al.] // J. Bone Miner. Res. – 1996. – N 11, Vol. 10. – P.1531–1538.
21. Storm Т. Effect of intermittent cyclical etidronate therapy on bone mass and fracture rate in postmenopausal osteoporosis / T. Storm [et al.] // New Engl. J. Med. – 1990. – N 322, Vol. 19. – P. 1265–12671.
22. Ettinger В. Reduction of vertebral fracture risk in postmenopausal women with osteoporosis treated with raloxifene: results from a 3 year randomized controlled trial / B. Ettinger [et al.] // JAMA. – 1999. – N 282, Vol. 4. – P.637–645.
23. Meta–analysis of the efficacy of alendronate for the prevention of hip fractures in postmenopausal women / S. Papapoulos [et al.] // Osteoporos. Int. – 2005. – N 16, Vol. 5. – P.468–474.
24. Randomized trial of effect of alendronate on risk of fracture in women with existing vertebral fractures. Fracture Intervention Trial Research Group / D.M. Black [et al.] // Lancet. – 1996. – N 7, Vol. 348. – P. 1535–1541.
25. Multinational placebo-controlled randomized trial of the effects of alendronate on bone density and fracture risk in postmenopausal women with low bone mass: results of the FOSIT study. Fosamax International Trial Study Group / H.A. Pols [et al.] // Osteoporos. Int. – 1999. – N 9, Vol.5. – P. 461–468.
26. Alendronate reduces the risk of multiple symptomatic fractures: results from the fracture intervention trial /S. Levis [et al.] // J. Am. Geriatr. Soc. – 2002. – N50, Vol. 3. – P. 409–415.
27. Wimalawansa S.J. A four-year randomized controlled trial of hormone replacement and bisphosphonate, alone or in combination, in women with postmenopausal osteoporosis / S.J.Wimalawansa // Am. J. Med. – 1998. – N 104, Vol. 3. – P. 219–226.
28. Alendronate prevents loss of bone density associated with discontinuation of hormone replacement therapy: a randomized controlled trial / B.N. Ascott–Evans [et al.] // Arch. Intern. Med. – 2003. – N 163, Vol. 7. – P.789–794.
Медицинские новости. – 2009. – №12. – С. 47-50.
Внимание! Статья адресована врачам-специалистам. Перепечатка данной статьи или её фрагментов в Интернете без гиперссылки на первоисточник рассматривается как нарушение авторских прав.