Актуальность проблемы остеопороза (ОП) на современном этапе обусловлена как изменением демографической ситуации (увеличение продолжительности жизни населения и численности лиц старше 50 лет), так и внедрением новых лечебно-диагностических технологий (остеоденситометрия, биохимические маркеры костного метаболизма, микрокомпьютерная томография), позволяющих выявлять ранние патологические изменения скелетно-мышечной системы и своевременно рекомендовать лечебно-профилактические мероприятия, которые обеспечивают эффективное снижение риска остеопоротических переломов [1, 4, 6, 11, 17, 19, 22].
Помимо первичного ОП (постменопаузального и сенильного), целый ряд хронических заболеваний и состояний связан с развитием вторичного остеопороза (глюкокортикоидиндуцированный, ревматоидный артрит, гиперпаратиреоидная остеодистрофия, иммобилизация, ОП на фоне тиреотоксикоза, гипогонадизма, синдрома мальабсорбции, генетических синдромов и др.) [2, 6, 25].
Эффективность применения различных лекарственных средств в лечении ОП оценивается на основании результатов проспективных (не менее 3 лет) плацебоконтролируемых исследований, учитывающих снижение риска переломов (позвоночных, шейки бедра, внепозвоночных) как основного клинического показателя [2, 4, 9, 16]. Кроме того, важны повышение минеральной плотности кости (МПК) осевого скелета, нормализация костного метаболизма, улучшение гистоморфометрических показателей костной ткани, а также улучшение качества жизни пациентов [4, 9]. В качестве средств для лечения постменопаузального ОП экспертами ВОЗ рекомендованы препараты, представленные в табл. 1 [18].
|
|
Доказанное снижение риска переломов
|
|
|
|
|
|
|
|
|
|
|
+
|
|
|
|
|
–
|
|
|
|
|
+
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Таблица 1. Лечение остеопороза с учетом данных медицины, основанной на доказательствах
Согласно заключению Комитета по контролю за качеством продуктов и лекарственных средств США (FDA , 2007) средствами фармакотерапии остеопороза являются [22]:
- антирезорбенты (ингибирование костной резорбции):
- бисфосфонаты (алендронат, ризендронат, ибандронат),
- кальцитонин,
- эстрогены (ЗГТ),
- ралоксифен;
- анаболические препараты (стимуляция костеобразования):
- паратиреоидный гормон ПТГ (ПТГ 1-34, терипаратид).
Как следует из рекомендаций ведущих организаций, разрабатывающих стратегию профилактики и лечения ОП, одной из групп лекарственных средств, направленных на патогенетическую коррекцию ОП, являются бисфосфонаты (БС) [4, 6–8, 15, 20].
Историческая справка. Бисфосфонаты представляют собой устойчивые аналоги встречающихся в природе соединений пирофосфата. Первый представитель БС был синтезирован в 1865 г. в Германии. Свойство бисфосфонатов угнетать осаждение карбоната кальция позволяло использовать их в промышленности в качестве ингибиторов коррозии или комплексных агентов при изготовлении тканей, минеральных удобрений, а также при нефтепереработке [3, 14] .
Биологические свойства БС были описаны в 1968 г. [14]. Поскольку бисфосфонаты уменьшали эктопическую кальцификацию in vivo, высказано предположение, что они могут выступать в роли физиологического регулятора процесса кальцификации, а также, возможно, декальцификации. Бисфосфонаты селективно присоединяются к костной ткани, так как имеют высокую степень сродства к гидроксилапатиту, где они уменьшают резорбцию и ремоделирование костной ткани путем влияния на активность остеокластов. Данное обстоятельство послужило основанием для их эффективного использования в лечении заболеваний костной ткани (болезнь Педжета и метастатические поражения костной ткани) [14]. В настоящее время БС занимают лидирующие позиции в лечении и профилактике как первичного (постменопаузального), так и вторичного ОП (глюкокортикоидиндуцированного, при ревматоидном артрите, ОП у мужчин) [3, 4, 9, 14].
Биологические свойства БС реализуются за счет особой структуры этого соединения (рис. 1) [14].
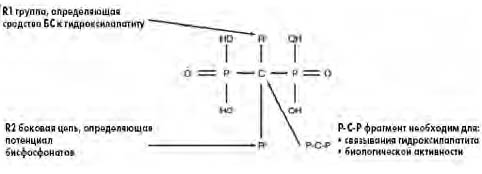
Рис.1. Химическая структура бисфосфонатов
На основе использования замещения азота в боковой цепи бисфосфонаты могут быть разделены на четыре химические группы [3, 14]:
- БС без замещения атома азота (этидронат, клодронат, тилудронат);
- аминобисфосфонаты (памидронат, алендронат, неридронат);
- аминобисфосфонаты с замещением атома азота (олпадронат, ибандронат);
- БС с основными гетероциклическими соединениями, содержащими азот (ризендронат, золендронат).
Химическая структура бисфосфонатов, применяемых в качестве антирезорбтивных средств, представлена на рис. 2 [14].
Рис. 2. Химическая структура бисфосфонатов, используемых для лечения ОП
Сравнительная активность БС и особенности их применения в качестве антирезорбтивного средства в профилактике и лечении ОП представлены в табл. 2 [3, 5, 6, 14].
|
|
|
|
|
|
|
|
|
400 мг/сут внутрь две недели каждого квартала, 10 мг/кг/сут
|
|
|
|
|
|
5–10 мг/сут внутрь или 35–70 мг 1 раз в неделю
|
|
|
|
|
|
5 мг/сут внутрь или 35 мг 1 раз в неделю
|
|
|
|
|
|
3 мг в/в 1 раз в 3 мес или 2,5–5 мг/сут внутрь 150 мг 1 раз в месяц
|
|
|
|
|
|
4 мг в/в 1 раз в 4 недели или 5 мг 1 раз в 12 мес
|
|
|
* Препараты, зарегистрированные в Республике Беларусь для лечения ОП.
Таблица 2. Сравнительная активность и особенности назначения БС для профилактики и лечения ОП
Алендронат по своей химической структуре относится к группе аминобисфосфонатов [2–4, 9, 14]. Ранние исследования показали, что главным компонентом алендроната является фрагмент P-C-P, определяющий его сродство к костной ткани. Фрагмент R1 обусловливает дополнительную аффинность: замена атома водорода гидроксильной группой в положении R1 увеличивает сродство к гидроксилапатиту примерно в два раза. Введение компонентов азота в положение R2 повышает антирезорбтивный потенциал алендроната в три раза по сравнению с БС, не содержащими азот. Показано, что присутствие молекулы азота в боковой цепи структуры алендроната повышает его возможности и специфичность, направленные на подавление костной резорбции [3, 14].
В настоящее время алендронат имеет наиболее широкие официальные показания в профилактике и лечении ОП.
Рекомендации Национальной федерации остеопороза США (NOF, 2007) для назначения алендроната:
профилактика остеопороза (5 мг/сут или 35 мг/нед.) у женщин в постменопаузе;
лечение остеопороза (10 мг/сут или 70 мг/нед. в виде монотерапии или в комбинации с витамином D – 800 МЕ/сут):
у женщин в постменопаузе,
у мужчин,
при глюкокортикоидиндуцированном ОП.
В клинической практике в Республике Беларусь широко используется алендронат — «Остеотаб» производства фармацевтической компании «Pharmacare Int. Co.», который выпускается в виде таблеток по 10 мг и 70 мг.
Клинико-фармакологические характеристики. Биодоступность алендроната у женщин при приеме внутрь в дозе 70 мг натощак не позднее, чем за 2 часа до стандартного завтрака, составляет 0,64%, у мужчин — 0,6% [4, 6, 14]. Биодоступность снижается (приблизительно на 40%) при приеме алендроната натощак за 1–1,5 часа до стандартного завтрака. Биодоступность алендроната незначительна при его приеме вместе с пищей или в течение 2 часов после еды. Совместный прием алендроната с кофе или апельсиновым соком снижает его биодоступность приблизительно на 60% [4, 6, 14].
Таким образом, эффективность алендроната максимальна при приеме натощак не позднее, чем за 30 минут до первого приема пищи либо жидкости.
После приема внутрь в терапевтических дозах концентрация алендроната в плазме крови незначительна (менее 5 нг/мл). Связывание алендроната с белками плазмы составляет приблизительно 78%. Препарат временно распределяется в мягких тканях, затем быстро перераспределяется в кости и выводится с мочой. У человека кажущийся объем распределения алендроната, исключая костную ткань, составляет около 28 л [4, 6].
Алендронат не метаболизируется в организме. В экспериментах установлено, что после внутривенного введения он экскретируется с мочой; выведение меченого препарата с калом не определялось или было незначительным. После однократного внутривенного введения 10 мг алендроната его почечный клиренс составлял 71 мл/мин, системный клиренс не превышал 200 мл/мин. Через 6 часов после внутривенного введения концентрация в плазме крови снижается более чем на 95%. Период полувыведения из плазмы крови — не более 10 часов [4].
Всасывание алендроната может нарушаться, если он принимается одновременно с препаратами кальция (включая пищевые добавки), железа и антацидами. Прием алендроната с аминогликозидами повышает риск развития гипокальциемии. Нестероидные противовоспалительные средства повышают гастротоксичность алендроната.
Анализ исследований по оценке эффективности алендроната в лечении постменопаузального остеопороза. Доказательная база по оценке эффективности алендроната в лечении постменопаузального ОП начала формироваться более 15 лет назад, однако наиболее значимые результаты получены в конце 90-х годов прошлого столетия [2–4, 9, 14].
В исследовании Early Postmenopausal Intervention Cohort (EPIC) изучалась эффективность двух доз алендроната (2,5 и 5 мг) в течение 4 лет [4, 6, 14]. Полученные результаты выявили достоверное увеличение МПК (4% – в поясничном отделе позвоночника и 3% – в шейке бедра) у пациенток, принимавших препарат в дозе 5 мг/сут.
Внимания заслуживает работа D.M. Black et al. [10] — трехлетнее слепое плацебоконтролируемое исследование, включавшее 3000 женщин в постменопаузе. Результаты применения алендроната в лечении постменопаузального ОП свидетельствовали о достоверном повышении МПК в поясничном отделе позвоночника в зависимости от дозы (5–20 мг) на 6–10 % (оптимальная доза 10 мг повышала МПК на 8,8%), в шейке бедра — на 4–6%, во всем теле — на 2,5% при сравнении с группой плацебо. За три года лечения на 48% снизился риск возникновения новых переломов тел позвонков и уменьшилось количество новых переломов костей других локализаций. За первые 3 месяца терапии отмечено достоверное снижение уровней биохимических маркеров костного метаболизма, которые оставались стабильными в последующие месяцы лечения. Гистоморфометрические данные подтвердили отсутствие нарушений минерализации и ухудшения качества кости. Частота возникновения побочных эффектов не отличалась от таковой у пациентов, получавших плацебо, хотя несколько чаще встречались осложнения со стороны ЖКТ (эзофагиты, обострение гастрита или язвенной болезни желудка), что объяснялось низкой всасываемостью БС. Исходя из полученных результатов было рекомендовано назначение лекарственного средства строго натощак за 30 минут до еды, запивая только водой [4, 6, 10].
Результаты масштабных проспективных исследований FOSIT (Fosamax International Trial) и FIT (Fracture Intervention Trial) с высокой степенью достоверности подтвердили, что прием алендроната в дозе 10 мг в сутки у женщин в постменопаузе повышает МПК поясничного отдела позвоночника и бедра на 5–14% и снижает риск переломов позвонков на 47%, множественных переломов позвоночника – на 90%, проксимального отдела бедра – на 51–56%, предплечья – на 48%. У 64% пациентов отмечено замедление темпов прогрессирования деформаций позвонков [24].
В исследовании FIT-1, включавшем 6459 женщин в постменопаузе с низкой МПК и переломами позвонков в анамнезе, установлено, что алендронат снижает риск последующих переломов бедра на 51% (Р=0,047), новых компрессионных переломов позвонков – на 47% (Р<0,001), множественных (2 и более) переломов позвонков – на 90% (Р<0,001) [6].
В исследовании FIT-2, в котором принимали участие 4432 пациентки с ОП без вертебральных переломов в анамнезе, отмечено снижение риска переломов бедра на 56% (относительный риск RR=0,44 (0,18-0,97) 95% ДИ), морфометрически установленных переломов позвонков – на 44% (RR=0,56 (0,39-0,80) 95% ДИ) и переломов различной локализации – на 36% (RR=0,64 (0,50-0,82) 95% ДИ)[4, 6].
С целью улучшения комплекса лечения и снижения риска развития побочных эффектов со стороны ЖКТ была создана форма алендроната с дозировкой 70 мг один раз в неделю. Сравнительное исследование эффективности и переносимости препарата в дозе 10 мг в сутки и 70 мг в неделю в лечении постменопаузального ОП подтвердило эффективность ретардной формы при меньшей частоте побочных эффектов [3–6].
Результаты исследования, проведенного S. Levis et al. в 2002 г. [21], показали, что алендронат в дозе 5 мг через 6 мес лечения снижает риск множественных симптоматических переломов у пациенток с ОП (с и без вертебральных переломов в анамнезе). За 4,3 года алендронат снизил риск возникновения переломов тел позвонков на 84% (RR=0,16 (0,05-0,042) 95% ДИ) и множественных вертебральных переломов – на 42% (RR=0,58 (0,41-0,81) 95% ДИ). Таким образом, частота переломов была на 63 и 34% ниже, чем в группе плацебо.
Интересными представляются исследования аддитивного эффекта БС и заместительной гормональной терапии (ЗГТ) в лечении постменопаузального ОП [4,13, 15, 26].
S.J. Wimalawansa et al. в 1998 г. установили, что комбинированное назначение ЗГТ и этидроната у постменопаузальных женщин в течение 4 лет приводит к более выраженному увеличению МПК в поясничном отделе позвоночника и шейке бедра по сравнению с монотерапией каким-либо одним препаратом [27].
R. Lindsay et al. изучали эффективность комбинированного применения ЗГТ и алендроната (10 мг/сут) у 428 женщин с постменопаузальным ОП. Пациентки в течение 1 года принимали ЗГТ, а далее были рандомизированы на две группы: первая продолжала ЗГТ в сочетании с плацебо, а вторая получала ЗГТ и алендронат. Во второй группе выявлено достоверное увеличение МПК в поясничном отделе позвоночника (3,6% vs 1,0%; Р<0,001) и шейке бедра (2,7% vs 0,5%; Р<0,001) [4].
В исследовании, проведенном H.G. Bone et al., изучалась эффективность сочетанной терапии алендронатом (10 мг/сут) и конъюгированными эстрогенами (0,625 мг/сут) в течение 2 лет без предшествующего применения ЗГТ [6]. Установлено более выраженное положительное влияние комбинированной терапии на МПК и уровень маркеров костного ремоделирования.
B.M. Ascott-Evans et al. в 2003 г. в проспективном плацебоконтролируемом исследовании оценили эффективность применения алендроната после прекращения курса ЗГТ [9]. Пациентки были рандомизированы на две группы: в первой принимали алендронат (10 мг/день), во второй – плацебо (в виде пластыря) в течение 1 года. Установлено снижение МПК на 3,2% в поясничном отделе позвоночника у женщин, принимавших плацебо, по сравнению с достоверным увеличением МПК у получавших алендронат (на 3,2%).
В рандомизированном двойном плацебоконтролируемом исследовании О. Johnell et al. [17] изучали применение алендроната (10 мг/сут) в комбинации с представителем группы селективных модуляторов эстрогеновых рецепторов (СЭРМ) – ралоксифеном (60 мг/сут). В группе, получавшей монотерапию ралоксифеном, установлено увеличение МПК в поясничном отделе позвоночника на 1,9%, среди принимавших алендронат – на 4,4%, в группе пациенток, получавших комбинированное лечение в течение 1 года, – на 5,3%.
Результаты метаанализа исследований эффективности применения алендроната в комплексной терапии (в сочетании с препаратами кальция) постменопаузального ОП представлены в табл. 3.
|
|
Число наблюдений, зона контроля
|
|
|
U.A. Liberman et al., 1995
|
994 пациента в 37 центрах МПКТ поясничного отдела позвоночника
|
|
|
|
|
2027 пациентов в 11 центрах
|
доза увеличивалась до 10 мг/сут на 24 мес
|
Снижение риска переломов на 11–13%
|
S.R. Cummings et al., 1998
|
4432 пациента в 11 центрах МПК шейки бедра
|
доза увеличивалась до 10 мг/сут на 24 месяца
|
Повышение МПК шейки бедра на 17–19%
|
|
|
1908 пациентов в 153 центрах МПК позвоночника
|
|
Повышение МПК поясничного отдела позвоночника на 11%
|
R.D. Chapurlat et al., 2004
|
6459 пациентов МПК позвоночника
|
|
Снижение риска переломов на 57%
|
|
|
41 пациент МПК шейки бедра и позвоночника
|
|
Достоверное повышение МПК
|
|
|
520 пациентов МПК шейки бедра и позвоночника
|
|
Повышение МПК на 3,4% за 12 мес в области трохантера и на 1,2% в области позвоночника
|
Таблица 3. Метаанализ исследований по изучению эффективности алендроната в лечении постменопаузального остеопороза
Сотрудниками БГМУ и Республиканского центра медицинской реабилитации и бальнеолечения в настоящее время проводится исследование эффективности алендроната (Остеотаба) в комплексной терапии постменопаузального остеопороза и остеопороза у пациентов с СД 2 типа. Результаты планируется представить в 2009 г.
Таким образом, представитель группы бисфосфонатов — алендронат имеет обширную доказательную базу в отношении эффективности лечения постменопаузального ОП как в виде монотерапии, так и в комбинации с другими антирезорбтивными препаратами. Официальные рекомендации по применению алендроната включают возможность его использования в качестве профилактического средства у женщин в менопаузе, а также для лечения глюкокортикоид-индуцированного остеопороза и ОП у мужчин. Хорошая переносимость и умеренная стоимость делают алендронат препаратом первой линии выбора в лечении постменопаузального остеопороза в Республике Беларусь.
1. Джонел О. // Медикография. – 2004. –Т. 26, № 3. – С.1–3.
2. Клинические рекомендации. Остеопороз. Диагностика, профилактика и лечение / под общ. ред. Л.И. Беневоленской, О.М. Лесняк. – М.: ГЭОТАР–Медиа, 2005.
3. Поворознюк В.В. // Здоров’я України. – 2007. – № 5. – С. 57–58.
4. Риггз Б.Л., Мелтон Л.Дж. Остеопороз. Этиология, диагностика, лечение / пер. с англ. – М.; СПб.: ЗАО «Изд-во БИНОМ», «Невский диалект», 2000.
5. Руденко Э.В. Остеопороз. Диагностика, лечение и профилактика.– Минск: Белорусская наука, 2001.
6. Руководство по остеопорозу / под общ. ред. Л.И. Беневоленской. – М.: БИНОМ. Лаборатория знаний, 2003.
7. Холодова Е.А. и др. Эндокринные остеопатии: особенности патогенеза, диагностики и лечения. Практическое руководство для врачей. – Минск: Белпринт, 2006.
8. Шепелькевич А.П., Забаровская З.В. // Мед. новости. – 2008. – № 7. – С.55–60.
9. Ascott–Evans B.N. et al. // Arch. Intern. Med. – 2003. –Vol. 7, N 163. – P.789–794.
10. Black D.M. et al. // Lancet. – 1996. –Vol. 348, N 7. – P. 1535–1541.
11. Burge R. et al. // J. Bone Miner. Res. – 2007. – Vol. 22. – P. 465–475.
12. Cummings S.R. et al. // JAMA. – 1998. – Vol. 11, N 280. – P. 2077–2078.
13. Ettinger В. et al. // JAMA. – 1999. –Vol. 4, N 282. – P.637– 645.
14. Fleish H. Bisphosphonates in Bone Disease. From the laboratory to the patients. – Academic Press, 2000.
15. Garnero P. et al. // J. Bone Miner. Res. – 1996. – Vol. 10, N 11. – P.1531–1538.
16. Hemenway D., Feskanich D., Colditz G.A. // Intern. J. Epidemiol. – 1995. – Vol. 4, N 24. – P.783–786.
17. Johnell O., Kanis J.A. // Osteoporos. Intern. – 2006. – Vol. 17. – P.1726–1733.
18. Kanis J.A. et al. // Osteoporos. Intern. – 2008. – Vol. 19. – P. 339–428.
19. Kanis J.A. on behalf of the World Health Organization Scientific Group (2007). Assessment of osteoporosis at the primary health care level. Technical Report. World Health Organization Collaborating Center for Metabolic Bone Diseases, University of Sheffield, UK. – Printed by the University of Sheffield, 2007.
20. Kasper L. et al. Harrison’s Principles of Internal Medicine. Chapter: Osteoporosis. – McGraw–Hill, 2005.
21.Levis S. et al. // J. Amer. Geriatr. Soc. – 2002 –Vol. 3, N 50. – P. 409–415.
22. National Osteoporosis Foundation. NOF’s Clinician’s Guide to Prevention and Treatment of Osteoporosis [электронный ресурс]. – Режим доступа: http://www.nof.org/professionals/ NOF_Clinicians_Guide.pdf. – Дата доступа: 23.08.2008.
23. Papapoulos S. et al. // Osteoporos. Intern. – 2005. –Vol. 5, N 16. – P.468–474.
24. Pols H.A. et al.// Osteoporos. Intern. – 1999. – Vol.5, N 9. – P. 461–468.
25. Roux C. et al. // The living bone. – Wolter Kruwer Health France, 2007. – Р. 113.
26. Storm Т. et al. // New Engl. J. Med. – 1990. – Vol. 19, N 322. – P. 1265–12671.
27. Wimalawansa S.J. // Amer. J. Med. – 1998. –Vol. 3, N 104. – P. 219–226.
Медицинские новости. – 2008. – №12. – С. 87-91.
Внимание! Статья адресована врачам-специалистам. Перепечатка данной статьи или её фрагментов в Интернете без гиперссылки на первоисточник рассматривается как нарушение авторских прав.