Внимание! Статья адресована врачам-специалистам
Boikа A.V.1, Tarasik Zh.G.2
1Institute for Advanced Training and Retraining of Healthcare Personnel of the Belarusian State Medical University, Minsk
25th City Clinical Hospital, Minsk, Belarus
Lysinate in the prevention of cerebral edema development in ischemic stroke
Резюме. Инфаркт головного мозга характеризуется рядом характерных патофизиологических изменений. Отек головного мозга является грозным его осложнением, приводит к летальному исходу в ряде случаев. Совершенствование дегидратирующей терапии – актуальная задача сосудистой неврологии. В статье отражены современные патофизиологические механизмы патогенеза отека головного мозга. Авторы приводят результаты, демонстрирующие эффективность раннего назначения препарата Лизинат в комбинированной терапии ишемического инсульта.
Ключевые слова: ишемический инсульт, дегидратирующая терапия, раннее назначение, отек мозга, Лизинат.
Медицинские новости. – 2025. – №2. – С. 47–50.
Summary. Stroke is characterized by a number of characteristic pathophysiological changes. Cerebral edema is a formidable complication, which leads to death in some cases. Improving dehydrating therapy is an urgent task of vascular neurology. The article reflects modern pathophysiological mechanisms of cerebral edema pathogenesis. The authors present results reflecting the effectiveness of early administration of the drug Lysinate in the combined therapy of ischemic stroke.
Keywords: ischemic stroke, dehydration therapy, early administration, cerebral edema, Lysinate.
Meditsinskie novosti. – 2025. – N2. – P. 47–50.
Во всем мире инсульт является основной причиной инвалидности взрослых и второй по значимости причиной смерти после ишемической болезни сердца, ежегодно поражая более 13,7 миллиона пациентов [1]. Злокачественный отек мозга является грозным осложнением ишемического инфаркта, на долю которого приходится от 10% до 78% пациентов со всеми типами ишемического инсульта [2]. Он может привести к массивному отеку мозга, последующему повышению внутричерепного давления (ВЧД), быстрому неврологическому ухудшению и транстенториальному вклинению [3]. Уровень смертности у пациентов со злокачественным отеком мозга приближается к 80% [3]. Несмотря на внедрение в медицинскую практику большого количества методов медикаментозной и немедикаментозной терапии, варианты лечения отека мозга остаются ограниченными, а доступные методы лечения не являются оптимальными. Считается, что понимание основных молекулярных и клеточных механизмов формирования отека имеет решающее значение для существенного прорыва в данном направлении [4].
В статье представлена современная научно-практическая информация по дифференцированному подходу к коррекции отека головного мозга при ишемическом инсульте и собственные данные по эффективности применения препарата Лизинат у пациентов.
Многочисленные научные исследования позволили обнаружить, что отек головного мозга протекает в три отдельные фазы, которые развиваются последовательно во времени и пространстве: 1) ранний цитотоксический отек, 2) последующая фаза ионного отека и 3) фаза вазогенного отека [5]. Цитотоксический отек возникает уже в течение нескольких минут после ишемического инсульта. При этом еще нет нарушения проницаемости гематоэнцефалического барьера (ГЭБ). Однако из-за истощения АТФ определяется набухание астроцитов и дендритов. Хотя цитотоксический отек не вызывает отека тканей, ионный градиент между сосудистым отделом и интерстициальной жидкостью обеспечивает движущую силу для последующего ионного и вазогенного отека. Термин ионный отек (интерстициальный отек) был введен для объяснения формы отека головного мозга в первые часы ишемического инсульта, тогда как разрушение ГЭБ происходит не раньше чем через 4–6 ч после начала ишемии [6]. Здесь стоит особо подчеркнуть, что, несмотря на анатомическую целостность нейронов в зоне ишемии, на данной стадии отека уже страдает функциональная активность клеток, так как нарушаются процессы де- и реполяризации, что может проявляться клинически значимой очаговой неврологической симптоматикой. С распадом ГЭБ ионный отек сменяется вазогенным отеком, который характеризуется избыточным проникновением воды и белков плазмы (альбумин и IgG) в интерстициальную ткань головного мозга. Источником воды для ионного отека мозга может быть не только кровь, но и спинномозговая жидкость [7]. Гипотеза о том, что местная перфузия крови действует как источник воды для ионного отека мозга, подтверждена многочисленными экспериментами. Кроме того, отечная жидкость в первую очередь обнаруживается и располагается в основном в периинфарктных зонах, которые активно кровоснабжаются.
Использование осмотических агентов для медикаментозной коррекции отека мозга основано на идее создания градиента осмотического давления над полупроницаемой мембраной ГЭБ и тем самым вытягивания интерстициальной и внутриклеточной воды из набухшего мозга во внутрисосудистые пространства. Для лечения прогрессирующего отека головного мозга после инсульта в настоящее время наиболее широко используются маннит, глицерин, гидроксиэтилкрахмал и гипертонический раствор [8, 9]. Согласно большинству научно-обоснованных рекомендаций, осмотерапию следует начинать при повышении ВЧД. Рекомендуется применение маннита (100 мл 20% раствора или 0,5–1,0 г/кг каждые 4–6 часов; максимальная суточная доза 2,5 г/кг), глицерина (250 мл 10% раствора 4 раза в день) или гидро-ксиэтилкрахмала (6% гетакрахмал в 0,9% растворе NaCl для инъекций, от 100 до 250 мл каждые 8 часов; максимальная суточная доза 750 мл). Начало действия этих веществ наступает через несколько минут, а продолжительность составляет от 4 до 8 часов. При повторном применении доза зависит от осмоляльности сыворотки, которая должна составлять от 315 до 320 мОсмоль. В качестве альтернативы можно использовать гиперосмолярные солевые растворы (10% NaCl, 75 мл, многократные дозы), вводимые через центральный венозный катетер. Преимущество гиперосмолярного физиологического раствора состоит в том, что он активно исключается из интактного гематоэнцефалического барьера, то есть не повреждает его и, соответственно, может использоваться на всех стадиях отека [10]. Еще одним преимуществом является то, что его можно комбинировать с маннитом, поскольку он противодействует индуцированной маннитом гипонатриемии, которая развивается почти у каждого пациента, получающего повторные дозы маннита.
Отечественные требования к терапии отека головного мозга при инфаркте мозга отражены в постановлении №8 от 18.01.2018 г. «Об утверждении клинического протокола «Диагностика и лечение пациентов с заболеваниями нервной системы (взрослое население)». Так, при стационарном лечении пациента с диагнозом «Инфаркт мозга (I63)» при клинических и КТ-признаках нарастающего отека мозга, повышении ВЧД более 15 мм рт. ст. (по данным мониторинга), не снижающегося на фоне седации и(или) аналгезии, уровне натрия плазмы менее 150 ммоль/л (контроль электролитов не реже 2 раз в сутки): растворы с осмодиуретическим действием в/в: сормантол, маннитол, с последующим введением в/в мочегонных средств: фуросемид. Введение указанных средств повторяют каждые 4–5 часов с учетом клинических проявлений и уровня осмолярности плазмы (не более 295 ммоль/кг). Введение осмотических диуретиков противопоказано при почечной недостаточности, отеке легких и декомпенсированной сердечной недостаточности.
Перспективным для комбинированной терапии инфаркта мозга может быть назначение на ранних стадиях развития ишемии препарата Лизинат (водорастворимая соль сапонина эсцина из плодов каштана конского и аминокислоты L-лизина). Препарат удобен для применения, поскольку его введение осуществляется внутривенным путем, максимальная суточная доза составляет 25 мл (22 мг эсцина), что позволяет назначать его несколько раз в сутки, а также комбинировать с другими препаратами, использующимися для терапии отека (маннит, сормантол, фуросемид и др.). Именно эсцин обладает противовоспалительными, противоотечными, мембраностабилизирующими и капилляропротекторными свойствами [11, 12], что определяет протективные фармакологические свойства препарата и научно обосновывает его эффективность при использовании в терапии инфаркта мозга, начиная уже с первых часов от развития ишемии.
Несмотря на большое количество исследований, посвященных применению Лизината при ЧМТ, вертеброгенной патологии и др., данные об эффективности Лизината в противоотечной терапии при ишемическом инсульте немногочисленны. С целью изучения эффективности противо-отечного действия препарата Лизинат у пациентов с инфарктом головного мозга на стационарном лечении нами были ретроспективно проанализированы истории болезни неврологического отделения для лечения пациентов с ОНМК (одномоментное одноцентровое поперечное исследование). Отобранные, согласно соответствующим критериям включения и исключения, пациенты были распределены на две группы: 1) пациенты, получившие Лизинат; 2) пациенты, не получившие Лизинат за время стационарного лечения. Комбинированная медикаментозная терапия у лиц обеих групп была представлена следующими группами препаратов: антиагрегантная, антикоагулянтная терапия, противогипертонические и антиангинальные препараты, антигипоксанты, антиоксиданты и ноотропные препараты.
Критерии включения: 1) возраст от 18 до 70 лет; 2) шкала комы Глазго при поступлении от 10 баллов и выше; 3) шкала NIHSS при поступлении не выше 15 баллов.
Критерии исключения: 1) тромболитическая терапия при поступ-лении; 2) инфаркт мозга в течение 12 месяцев перед поступлением; 3) внутримозговое кровоизлияние в течение 12 месяцев перед поступ-лением; 4) тяжелые соматические (аутоиммунные) и/или инфекционные заболевания в течение одного месяца перед поступлением; 5) травмы головного и/или спинного мозга в течение 12 месяцев перед поступлением; 6) тяжелые неврологические заболевания в течение одного месяца перед поступлением; 7) лакунарный инфаркт мозга по данным нейровизуализации, проведенной во время госпитализации, и/или клинически.
За факт отсутствия клинической противоотечной эффективности Лизната у пациента в данном исследовании было принято наличие маннита в листе назначений. При обработке полученных данных использовали непараметрические методы биомедицинской статистики. Результаты представлены в виде медианы, 25 и 75 перцентиля (Ме, Q25–Q75). Уровень значимости р приняли равным 0,1, что является достаточным при проведении пилотных медико-биологических исследований.
Всего для сбора необходимой информации нами было отобрано 80 историй пациентов, которые поступали на стационарное лечение с 2021 по 2024 год и которым был назначен препарат Лизинат. Ими оказались 44 женщины и 36 мужчин, возраст 58,8 [50,1; 65,6] года. В 23 случаях (28,75% пациентов) потребовалось последующее назначение маннита для лечения отека головного мозга, а в 57 случаях (71,25% пациентов) – нет.
В группу сравнения вошли 86 человек, которые также поступали в неврологическое отделение с диагнозом ишемический инсульт, но им не был назначен Лизинат. Группа сравнения была сформирована таким образом, чтобы не было статистически значимых отличий с основной группой по полу и возрасту (рманна-уитни > 0,05). В 32 случаях (37,2%) таким пациентам потребовалось назначение маннита, а в 54 случаях (62,8%) – нет. Несмотря на большую долю пациентов основной группы, которым не потребовалось назначения маннита на фоне применения Лизината, разница между группами не имела статистически значимый характер (U=3149, Z=0,9, p=0,34).
С учетом полученных результатов и принимая во внимание профилактическое действие Лизината, нами было принято решение изучить данные по назначению маннита в группе пациентов, получивших Лизинат, в зависимости от длительности между примерным началом ишемического инсульта (по данным анамнеза) и временем начала использования Лизината. В группу пациентов, получивших первую инфузию Лизината в течение двух суток от начала ишемического инсульта, вошло 29 человек, из них 5 пациентам (17,2%) требовалось назначение маннита в дальнейшем, а 24 (82,8%) – нет. 51 пациент был в группе, где Лизинат был назначен после двух суток от момента развития инфаркта мозга. При этом 18 пациентам (35,3%) в дальнейшем потребовалось назначение маннита, а 33 (64,7%) – нет. Соотношение пациентов, которым потребовалось назначение маннита (столбцы 1) и которые в нем не нуждались (столбцы 2), представлено на рисунке 1.
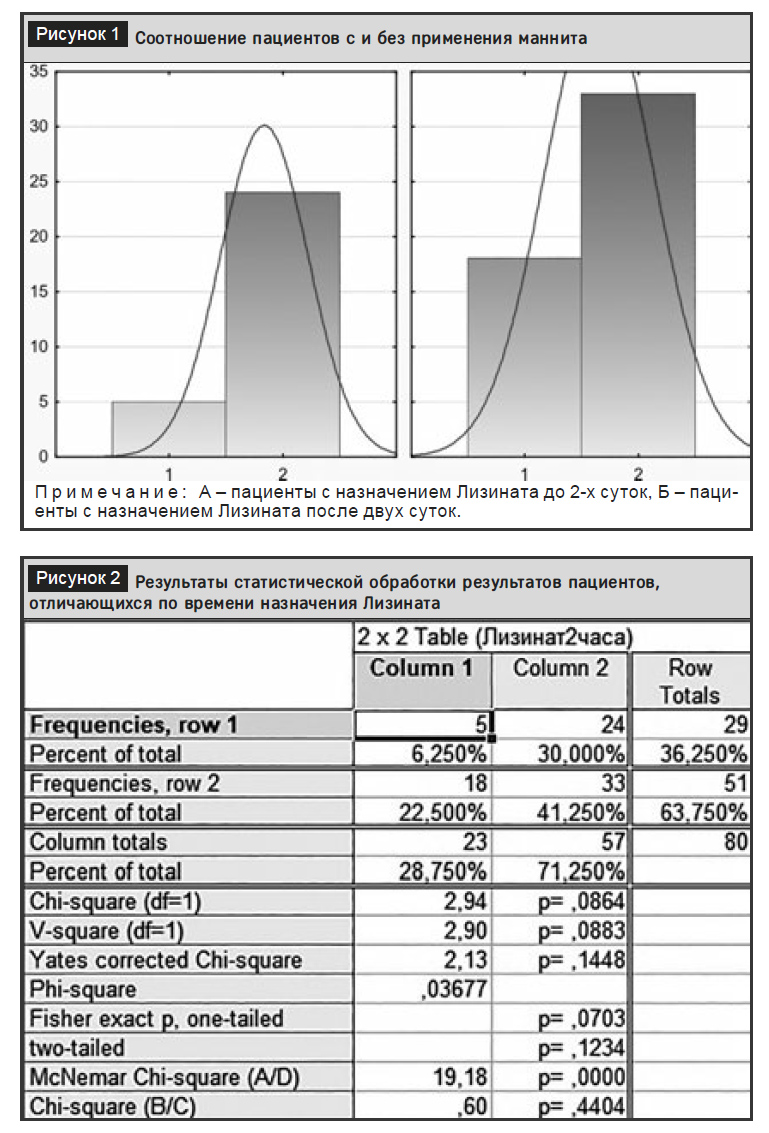
При дальнейшей обработке полученных данных были получены статистически значимые отличия между группами с разным временным интервалом назначения Лизината (U=606, Zadjusted=1,7, p=0,09). На рисунке 2 показаны результаты обработки этих же данных другими методами статистики в программе STATISTICA при использовании четырехпольной таблицы (таблица 2 на 2).
Результаты проведенной работы свидетельствуют о клинической эффективности Лизината при его назначении в более раннем периоде времени от начала инфаркта головного мозга. Так, в группе лиц, которым был назначен Лизинат в течение первых двух суток от начала ишемии мозговой ткани, число случаев последующего назначения Маннита было в 2 раза меньше, по сравнению с группой, где он был назначен в поздних сроках (17,2% и 35,3% соответственно). Полученные данные позволяют рекомендовать его широкое клиническое использование преимущественно на ранних стадиях развития ишемии мозговой ткани (догоспитальный этап и/или сразу при поступлении в стационар). Мембраностабилизирующие и капилляропротекторные свойства Лизината требуют его дальнейшего активного научного изучения не только в профилактике развития отека головного мозга, но и в профилактике прогрессирования ишемии (уменьшении зоны некроза мозговой ткани) при ишемическом инсульте.
Заключение
Прогрессирование отека головного мозга на фоне ишемического инсульта связано с неблагоприятным прогнозом. В настоящее время существует ограниченное количество эффективных вариантов лечения отека мозга, доступных для широкого клинического применения. Современные осмотические методы лечения сосредоточены на лечении отека, а не на его предотвращении, и доказательств их эффективности по-прежнему недостаточно. Традиционная осмотическая терапия не специфична для молекулярного механизма отека мозга. Ее основная роль заключается в снижении внутричерепной гипертензии и купировании смещения мозговых структур. Препараты могут вызывать серьезные осложнения, такие как водно-электролитные нарушения и поражение почек, поэтому обычно используются только при достижении высокого уровня внутричерепной гипертензии и угрозе церебральной перфузии, а также развития вклинения. Эффективное лечение отека головного мозга во время ранней фазы инсульта особенно важно. Действие Лизината на патофизио-логические механизмы формирования отека головного мозга, а также благоприятный профиль безопасности препарата позволяют его широко использовать уже в дебюте заболевания, при оказании медицинской помощи как на стационарном, так и на догоспитальном этапах.
ЛИТЕРАТУРА
1. Phipps M.S., Cronin C.A. // BMJ. – 2020. – Vol.368. – P.l6983.
2. Wu S., Yuan R., Wang Y., et al. // Stroke. – 2018. – Vol.49. – P.2918–2927.
3. Huttner H.B., Schwab S. // Lancet Neurol. – 2009. – Vol.8. – P.949–958.
4. Chen S., Shao L., Ma L. // Front. Cell. Neurosci. – 2021. – Vol.15. – P.716825.
5. Stokum J.A., Gerzanich V., Simard J.M. // J. Cerebr. Blood Flow Metab. – 2016. – Vol.36. – P.513–538.
6. Simard J.M., Kent T.A., Chen M.K., Tarasov K.V., Gerzanich V. // Lancet Neurol. – 2007. – Vol.6. – P.258–268.
7. Broocks G., et al. // Journal of stroke. – 2019. – Vol.21, N3. – P.347–349.
8. Hofmeijer J., van der Worp H.B., Kappelle L.J. // Crit Care Med. – 2003. – Vol.31. – P.617–625.
9. Steiner T., Ringleb P., Hacke W. // Neurology. – 2001. – Vol.57. – P.61–68.
10. Schwarz S., Georgiadis D., Aschoff A., Schwab S. // Stroke. – 2002. – Vol.33. – P.136–140.
11. Богачев В.Ю., Болдин Б.В., Дженина О.В. Эскузан: фармакология, фармакокинетика и терапевтические характеристики. https://doi.org/10.21518/1995-1477-2019-1-2-19-25
12. Экспериментальная оценка цитотоксического, цитопротекторного и антиоксидантного действия экстракта каштана конского с 50% содержанием эсцина / Т.А. Федотчева, А.И. Матюшин, А.Н. Усенко, О.П. Шейченко, А.Ю. Радимич, В.И. Шейченко, Н.И. Федотчева, Н.Л. Шимановский // Экспериментальная и клиническая фармакология. – 2019. – Т.82, №11. – С.15–19.
Медицинские новости. – 2025. – №2. – С. 47-50.
Внимание! Статья адресована врачам-специалистам. Перепечатка данной статьи или её фрагментов в Интернете без гиперссылки на первоисточник рассматривается как нарушение авторских прав.